Supporting materials
Download
Download this article as a PDF

Tradotto dalla classe 5 A LSSA IIS Badoni 2018/2019. Non sarebbe affascinante osservare e manipolare le singole molecole? Patrick Theer e Marlene Rau del Laboratorio Europeo di Biologia Molecolare (European Molecular Biology Laboratory) spiegano come lo si possa fare, usando un microscopio a…
L’idea di osservare le singole molecole o gli atomi ha affascinato gli scienziati per oltre un secolo. Questo ambizioso obiettivo è stato raggiunto per la prima volta nel 1981 con l’invenzione della microscopia a scansione ad effetto tunnel, per la quale Gerd Binning e Heinrich Rohrer del Laboratorio di Ricerca dell’IBM di Rüschlikon, in Svizzera, sono stati insigniti del Premio Nobel per la Fisica qualche tempo dopo, nel 1986w1. Questo microscopio presenta tuttavia una grave limitazione: funziona solo su oggetti che conducono elettricità, quindi non è possibile studiare molti materiali interessanti, tra cui le biomolecole. Binning e i suoi colleghi hanno continuato a cercare soluzioni migliori, e nel 1986, hanno presentato il microscopio a forza atomica (AFM), che può essere utilizzato per visualizzare sia materiali conduttori che non conduttori.

Lo strumento funziona non diversamente da un giradischi, nel quale un ago appuntito scansiona un disco di vinile per riprodurre il suono (vedere l’immagine a destra). L’AFM ‘sente’ gli atomi, piuttosto che ‘vederli’: la struttura di una superficie viene scansionata con un cono molto appuntito (solitamente di silicio o di nitruro di silicio) all’estremità di una microleva flessibile, chiamata cantilever, che può seguire anche i più piccoli dettagli della superficie. Quando la punta, costituita da un singolo atomo, si avvicina alla superficie del campione, viene deviata dalle forze che si esercitano tra i due: queste possono essere forze di contatto meccaniche, forze di van der Waals, forze capillari, legami chimici, forze elettrostatiche, forze magnetiche, forze dovute all’effetto Casimir, forze di solvatazione o altre, a seconda della natura del campione.
Per poter misurare tutta questa varietà di forze, l’AFM è molto versatile, ed ha portato ad un’esplosione del numero di scienziati che ne fanno uso – principalmente, ma non solo, per la scienza dei materiali e la biologia. In entrambi i casi, la forza che causa la deflessione è minuscola, e proporzionale alla distanza della punta dalla superficie.
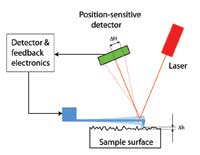
Come possono essere misurate queste minuscole deflessioni? Gli inventori hanno usato un astuto espediente: un fascio laser viene focalizzato sulla parte superiore del cantilever, da cui viene riflesso su un rivelatore di luce sensibile alla posizione. Il cambiamento della posizione del fascio laser sul detector (vedere il diagramma sulla sinistra, ∆H) dovuto alla deflessione del cantilever (vedere il diagramma a pagina 61, ∆h) è proporzionale alla distanza tra rivelatore e cantilever. Con distanze abbastanza grandi tra i due, possono essere misurate anche minime deflessioni, rendendo così possibile studiare le strutture delle superfici atomo per atomo.

Le applicazioni dell’AFM sono moltissime. Facciamone una breve rassegna. Originariamente, l’AFM fu sviluppato per osservare e analizzare nei minimi dettagli le strutture delle superfici – questo è interessante non solo per scopi di ricerca, ma può avere benefici economici diretti: la bioincrostazione è l’accumulo indesiderato di micro-organismi, piante, alghe e/o animali (come cirripedi, Cirripedia) su strutture bagnate. Sugli scafi delle navi, strati elevati di incrostazioni possono aumentare l’attrito dell’acqua e quindi aumentare notevolmente il consumo di carburante, ma questo è anche un problema che si presenta nei bioreattori a membrana, nei cicli dell’acqua di raffreddamento delle centrali elettriche e in alcuni oleodotti. Gli scienziati usano l’AFM per misurare il grado di bioincrostazione e quindi confrontare l’attività anti-bioincrostante di diverse sostanze, in modo da individuare il materiale ideale (Finlay et al., 2010).

Analogamente, l’AFM viene utilizzato in agricoltura: spesso le piante di ananas sono affette da un’infezione fungina chiamata fusariosi. Gli scienziati hanno confrontato la struttura superficiale delle cellule di coltivazioni di ananas che sono resistenti a questa malattia, con quelle di specie provenienti da coltivazioni che invece ne sono soggette, e hanno scoperto che presentano proprietà meccaniche differenti. Questo può essere usato ora per selezionare e migliorare le coltivazioni resistenti che hanno le proprietà meccaniche necessarie (de Farias Viégas Aquije et al., 2010).
La struttura superficiale è rilevante anche per la salute dell’uomo? La risposta è sì: gli studi con AFM sono spesso usati in odontoiatria, per esempio per confrontare l’efficacia dei diversi metodi per rimuovere placca e macchie; per misurare la rugosità della superficie degli apparecchi ortodontici, e vedere come questa influenzi l’efficacia con la quale i denti vengono portati nella disposizione corretta; oppure per quantificare l’erosione dello smalto dentale causato dall’acidità delle bibite, e testare l’efficacia dei vari dentifrici nella riparazione di questo danno (Kimyai et al., 2011; Lee et al., 2010; Poggio et al., 2010).
Altre applicazioni mediche includono lo sviluppo di nuovi biomateriali utilizzati nella medicina rigenerativa: le loro proprietà superficiali come bagnabilità, ruvidezza, energia superficiale, carica superficiale, funzionalità e composizione chimiche possono determinare il comportamento delle cellule con cui verranno in contatto. Perciò l’AFM può essere usato, per esempio, per aiutare a progettare biomateriali che sono tollerati dal corpo e possono essere usati per impianti biomedici come le anche artificiali (Al-Ahmad et al., 2010; Kolind et al., 2010; Padial-Molina et al., 2011).
Un altro rilevante campo di applicazione per l’AFM in biologia medica sono il misfolding, o ripiegamento errato, e l’aggregazione di proteine come l’a-sinucleina, l’insulina, i prioni, il glucagone e il b-amiloide. Questi fenomeni sono stati a lungo implicati in malattie degenerative come il diabete di tipo II, il Parkinson, l’encefalopatia spongiforme (morbo della mucca pazza), i morbi di Huntington e di Alzheimer. In questo campo l’AFM ha già fornito importanti informazioni sulla struttura nanometrica degli aggregati, e si spera che gli scienziati saranno in grado di utilizzare l’AFM per individuare, in primo luogo perché la proteina si ripieghi in modo errato, e in seguito come la proteina stessa incoraggi le proteine circostanti ad assumere la medesima struttura erroneamente ripiegata. (Lyubchenko et al., 2010; per una spiegazione del misfolding del prione, vedere Tatalovic, 2010).

Ulteriori interazioni biologiche che sono state studiate con l’AFM riguardano il modo in cui i trofoblasti umani (le cellule che compongono lo strato esterno dei blastocisti che forniscono nutrienti all’embrione e si sviluppano in gran parte della placenta) interagiscono con le cellule epiteliali dell’utero – le basi di un proficuo impianto embrionale (Thie et al., 1998).
Il passaggio dall’uso dell’AFM per le sole osservazioni al suo utilizzo per manipolare atomi, molecole o altre strutture nanometriche, è stato breve. Ad esempio, usando la punta a mo’ di nano-pinzette, è possibile esaminare precise regioni della membrana plasmatica della cellula; singoli loop proteici possono essere rimossi per rivelare la struttura proteica all’interno della molecola; e singole molecole possono essere allungate in nuove conformazioni per determinarne l’elasticità.
Il prossimo grande passo sarà usare l’AFM per la nanochirurgia: introducendo o estraendo singole molecole dal citoplasma delle singole cellule, per studiare l’omeostasi cellulare o per il rilascio subcellulare di farmaci (Lamontagne et al., 2008; Müller et al., 2006).
Punte per AFM modificate possono anche essere utilizzate come trapani o penne: la nano-fresatura rimuove il materiale sotto forma di trucioli lunghi e arricciati (Gozen & Ozdoganlar, 2010), mentre la nanolitografia dip-pen (letteralmente “a penna intinta “) è il rilascio controllato di “inchiostro” molecolare o liquido. Nella chimica e nelle scienze naturali, una tecnologia di questo tipo viene utilizzata per produrre sensori su scala nanometrica o, mediante la deposizione di nanostrutture metalliche, di semiconduttori e di ossidi di metalli, nanocircuiti o nanodispositivi funzionali (Basnar & Willner, 2009). Questo, combinato con l’uso della punta AFM per spingere fisicamente le particelle di dimensioni nanometriche nella posizione desiderata, dovrebbe aprire la strada alla miniaturizzazione dei circuiti elettronici e di altre strutture.
Nonostante il suo vasto numero di applicazioni – questi sono solo un piccolo esempio – le possibilità dell’AFM non sono ancora esaurite. Le tendenze future prevedono punte ottimizzate e combinazioni con altre tecniche, ad esempio per determinare simultaneamente la struttura superficiale e la fluorescenza o le proprietà elettriche (Müller et al., 2006). La velocità è un altro problema: recentemente è stato sviluppato un AFM con cui i processi biologici come replicazione e segregazione cromosomica, fagocitosi e sintesi proteica possono essere visualizzati in tempo reale, fino a 1000 volte più velocemente di quanto non fosse possibile in precedenza (Ando et al., 2008).
Non vedete l’ora di trovare le vostre applicazioni per l’AFM? Allora potreste provare a seguire le istruzioni w2 di Philippe Jeanjacquot per costruire il vostro strumento a scuola. È un progetto che richiede molto tempo, ma lui e i suoi studenti sono riusciti a creare un microscopio realizzabile a basso costo. Tuttavia, c’è un aspetto importante: per installarlo è necessario un ambiente privo di vibrazioni, ad esempio una cantina silenziosa. Se riuscite a trovarlo, entusiasmo e ingegno sono le vostre uniche limitazioni.
Questo articolo è adatto per una vasta gamma di lezioni di scienze – non solo per la fisica, ma anche per la fisiologia animale o le scienze biomediche, per esempio.
Gli studenti possono fare ricerche sulla microscopia a forza atomica e su suoi ulteriori impieghi, poiché in Internet c’è abbondanza di materiale su vantaggi e svantaggi delle varie tecniche microscopiche. Potrebbero anche fare ricerche sul gruppo di scienziati che hanno inventato il microscopio a forza atomica (che avevano vinto un premio Nobel per una precedente invenzione) e scoprire di più su di loro e il loro lavoro.
Potenziali domande per saggiare la comprensione dell’argomento sono:
L’articolo può essere usato con gruppi di studenti più grandi o con studenti particolarmente abili nel pensiero creativo, magari per un compito scritto più articolato, congiuntamente alla visione del film Tesoro, mi si sono ristretti i ragazzi (che racconta di uno scienziato che lavora ad una macchina che miniaturizza gli oggetti e – accidentalmente – le persone), per fare immaginare agli studenti di poter vedere le singole molecole. Per che cosa vorrebbero utilizzare il microscopio a forza atomica? Userebbero le loro immagini come forma d’arte o per la ricerca scientifica? Userebbero le loro conoscenze per curare malattie o per vedere quanto possa essere affascinante la scienza a questo livello?
Jennie Hargreaves, UK
Download this article as a PDF