Die Chemie vergrünen Understand article
Übersetzt von Daniel Busch. Die Chemie ist nicht immer komplett umweltfreundlich; die grüne Chemie arbeitet daran, dies zu ändern.
Die Chemie hat einen gemischten Ruf. Wir profitieren alle von den Verbrauchsgütern und Medikamenten, die die chemische Industrie produziert, aber dann ist da auch noch die dunkle Seite – wie der immense Energiebedarf der Industrie, sowie die Produktion von toxischen Lösungsmitteln, Reagenzen und Abfallprodukten. Seit über 20 Jahren versuchen Chemiker die Chemie zu säubern, mithilfe des wachsenden Forschungsfeldes der grünen Chemie.
Auch bekannt als nachhaltige Chemie oder umweltverträgliche Chemie, ist die grüne Chemie ein Konzept, das langsam auf der Schulebene eingeführt wird. Zwei ihrer frühestens Vorreiter, Paul Anastas und John Warner, definieren die grüne Chemie als “das Herstellen chemischer Produkte und Prozesse die die Verwendung und Produktion gefährlicher Substanzen reduziert oder eliminiert”.
Die Entfernung oder Reduzierung von chemischem Abfall, die Verringerung des Gesamtenergiebedarfs und ein Anstieg eines Sicherheitsbewusstseins sind die Interessen der Menschheit und der Umwelt. Die Industrie selber ist auch interessiert; ein Bericht von 2011 vermutet, dass die Industrie durch die grüne Chemie 65.5 Milliarden US$ bis 2020 sparen könnte.
Die Hauptideen, die der grünen Chemie zugrunde liegen, können in wenigen einfachen Punkten zusammengefasst werden, die interessante Themen für allgemeine Diskussionen im Klassenraum bieten oder eine tiefergehende Behandlung chemischer Prozesse, die traditionell an Schulen unterrichtet werden, erlauben können. An dieser Stelle werden wir einen Blick aus der Perspektive der Klimachemie auf die Thematik werfen. Eine komplette Liste mit 12 Prinzipien der grünen Chemie können onlinew1 abgerufen werden, wir werden uns hier jedoch auf jene Aspekte beschränken, die in der Schul-Chemie angewendet werden können: Atomökonomie, die Herkunft von Reagenzien, die Nutzung umweltverträglicher Substanzen und die Verringerung des Energieverbrauchs.
Verringerung des Abfalls
Eine Frage der grünen Chemie ist, welcher Anteil der Reagenzien und Lösungsmittel im gewünschten Produkt enden, anstatt als Abfall oder Nebenprodukt. Die Verringerung des Abfalls vermindert die dazugehörigen Umweltprobleme. Die Idee der ‘Atomökonomie’ und die einfachen Übungen, die die Lernenden durchführen können (siehe Kasten) werden diese Ideen verdeutlichen. Die Herkunft der Ausgangsmaterialien sollte ebenfalls bedacht werden. Reagenzien sollten möglichst erneuerbar sein oder von Quellen bezogen werden, die ausreichend und leicht verfügbar sind.
Insbesondere pharmazeutische Mittel werden oftmals in einer vielschrittigen Synthese produziert, anstatt einfach in einem Reagenzglas Reagenz A mit Reagenz B reagieren zu lassen, um das Medikament zu kreieren. In einer vielschrittigen Synthese wird das Produkt des einen Schrittes im nächsten Schritt weiterverwendet, allerdings ist der Ertrag jeweils deutlich geringer als 100%, sodass Material, Lösungsmittel und Energie auf dem Syntheseweg verloren gehen.
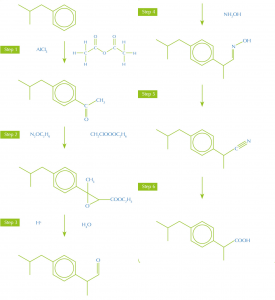
Synthesewege mit weniger und produktiveren Schritten, unter Berücksichtigung der anderen grünen Prinzipien, produzieren weniger Abfall. Das Schmerzmittel Ibuprofen wurde beispielsweise ursprünglich in einem Sechsschritt vom Ausgangsmaterial Isobutylbenzen synthetisiert, aber eine neue, effizientere Synthese benötigt nur drei Schritte (Abbildung 1).
Verringerung der Toxizität
Grüne Chemiker versuchen außerdem nur Substanzen zu verwenden, die der Umwelt nicht schaden. In einer der größten Industriedesaster weltweit, ist im Jahr 1984 Methylisocyanatgas (CH3NCO), das für die Herstellung von Pestiziden verwendet wird, aus der Anlage der Union Carbide India Limited in Bhopal, Indien ausgetreten. Tausende Menschen waren dem Stoff ausgesetzt. Die unmittelbare Zahl der Todesopfer wurde mir mehreren Tausend angegeben, und ca. eine halbe Million Menschen wurde verletzt und erlitt temporäre oder permanente Behinderungen.
Zusätzlich zur Wahl weniger toxischer Reagenzien, versuchen grüne Chemiker außerdem, nicht-organische Lösungsmittel wie Wasser oder superkritisches Kohlendioxid zu verwenden. Die bislang verwendeten Kohlenwasserstoff-Lösungsmittel sind toxisch und emittieren Dämpfe, die Treibhausgase sind, während halogenisierte Lösungsmittel oftmals sowohl Karzinogene, als auch Treibhausgase und Quellen von freien Radikalen sind – die die Ozonschicht zerstören.
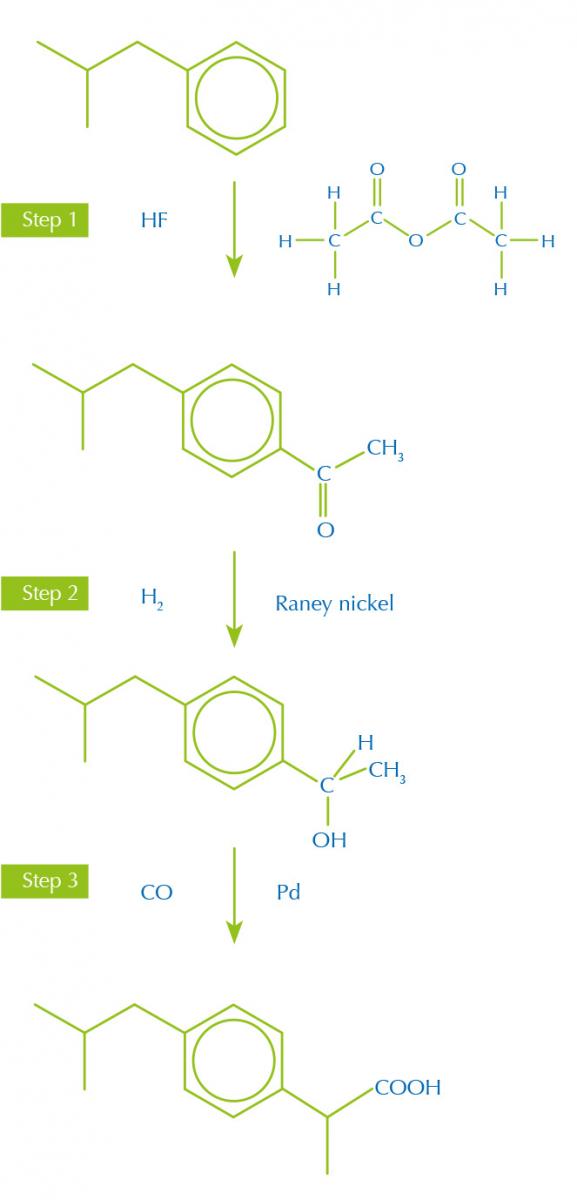
Synthese von Ibuprofen
Mit freundlicher Genehmigung
von Nicola Graf
Verringerung der Emissionen
Die chemische Industrie benötigt immense Mengen Elektrizität; die Verringerung dieses Bedarfs ist sowohl ökonomisch, als auch ökologisch wichtig. Forscher nutzen die Energie zum Erhitzen und zur Erhöhung des Drucks von Reaktionen und für den Stofftransport. Wissenschaftler suchen nach alternativen Reaktionswegen, die bei niedrigerer Temperatur und Druck ablaufen, was die Menge an durch das Verbrennen von fossilen Brennstoffen produziertem Kohlendioxid reduziert.
Effektivere Katalysatoren für existierende Reaktionen zu finden wird den Verbrauch an Reagenzien und Energie ebenfalls verringern. Idealerweise würden Katalysatoren weitverbreitete Metalle wie Eisen verwenden, anstatt exotischerer wie Platin, das selten vorkommt und eine bedeutende Menge Energie für die Gewinnung benötigt. Einige Katalysatoren werden während der Reaktion ‘vergiftet’, was bedeutet, dass Chemikalien an die aktiven Zentren der Katalysatoren binden und an der Oberfläche Produkte bilden, die toxisch und nur schwer auf sichere Weise entsorgt werden können können.
Die Anwendung der grünen Chemie auf grüne Treibstoffe
Wenn Energie verwendet wird, sind Bio-Treibstoffe ein erwünschter Ersatz für fossile Brennstoffe. Ethanol ist ein gut-bekannter Biotreibstoff, der während vielen Gährungsprozessen gebildet wird. Ethanol kann aus pflanzlicher Materie, wie einigen Grasarten und Maishülsen, gewonnen werden. Umgewandelte Fahrzeuge können hundertprozentiges Ethanol (E100) verwenden oder ein Ethanol-Benzin-Gemisch, bekannt als Gasohol, im Bereich von E5 bis E25. Allerdings ist Ethanol kein besonders guter Treibstoff da es:
- nicht so leicht verdunstet wie Benzin
- nur etwa 70% der Energiedichte von Benzin aufweist
- die Tendenz Wasser anzuziehen aufweist
- bei den Temperaturen im Motor sauer ist und somit Korrosion auslösen kann
- Motoren benötigt, die an den Verbrauch größerer Mengen Ethanol angepasst sind.
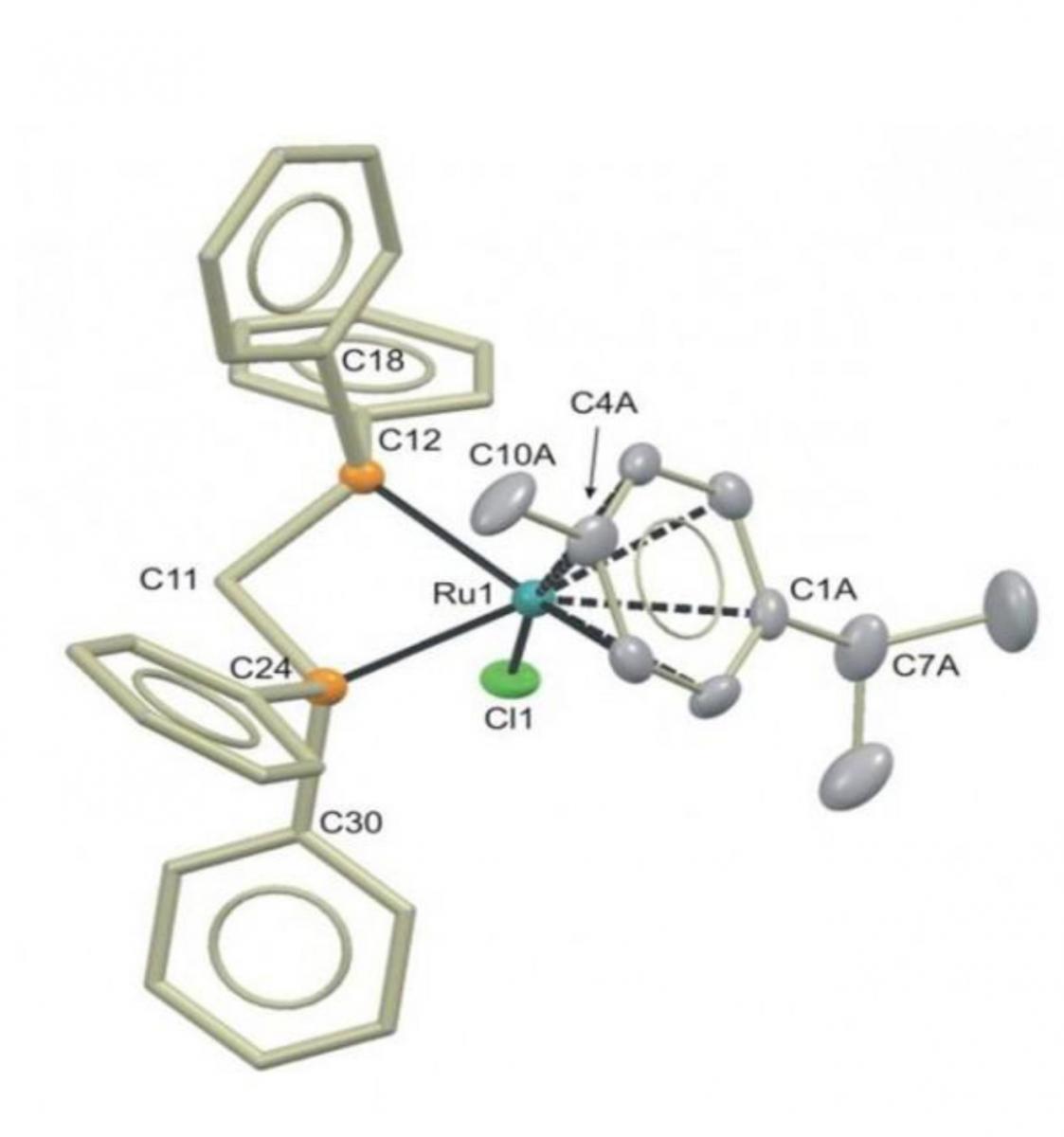
Katalysator, der verwendet
wird um Butan-1-ol aus
Ethanol herzustellen
Mit freundlicher Genehmigung
von Duncan Wass /Universtät
Bristol
Butan-1-ol (das eine Energiedichte von 29.2 MJ/l hat) wäre eine deutlich besserer Treibstoffzugabe als Ethanol (19.6 MJ/l), da es Eigenschaften hat, die dem Benzin (32.0 MJ/l) ähnlicher sind. Butan-1-ol kann aus Biomasse (Biobutanol) oder fossilen Brennstoffen (Petrobutanol) produziert werden. Allerdings benötigen die Prozesse entweder große Mengen Energien oder sind auf Biokatalysatoren (Enzyme) angewiesen und ergeben nur einen geringen Ertrag. Die Isolierung von Butan-1-ol aus einem Gemisch hat auch einen sehr hohen Energiebedarf.
Es ist schon lange ein Ziel der chemischen Industrie Butan-1-ol durch die Kondensation zweier Ethanolmoleküle herzustellen:
CH3CH2OH + HOCH2CH3 → CH3CH2CH2CH2OH + H2O
Im Jahr 2013 ermöglichte ein Durchbruch diese Prozedur mit einem Ertrag von mehr als 95% bei Verwendung eines Ruthenium Katalysators. Die Herausforderung besteht jetzt darin, diesen Prozess auf Industriemaß zu vergrößern.
Die Umweltprobleme werden sich nicht in Luft auflösen, daher wird die grüne Chemie immer wichtiger. Intelligente junge Menschen werden gebraucht, um die Prinzipien der grünen Chemie großflächig in den Chemiewissenschaften und der Chemietechnik anzuwenden.
Atomökonomie
Traditionell haben Chemiker die Effizienz einer chemischen Reaktion durch eine prozentuale Ertragsrechnung kalkuliert.
Prozentualer Ertrag = (Mol des erhaltenen Produktes / Mol des erwarteten Produktes) x 100
Barry Trost von der Stanford University, USA hat das Konzept der Atomökonomie als alternativen Weg der Effizienzbetrachtung einer Reaktion eingeführt. Die Artomökonomie stellt einen Zusammenhang zwischen der Masse der Ausgangsmaterialien und der Masse des gewünschten Produkts her. Dadurch verdeutlicht die Rechnung die verschwendeten Ressourcen: wenn sich nur ein kleiner Teil der Ausgangsmaterialien im Produkt findet, muss der Rest im Abfall sein.
Prozentuale Atomökonomie = (Masse des gewünschten Produkts / Masse aller Reagenzien) x 100
Es ist einfach, rechnerisch zu demonstrieren dass ein Chemiker, der die Atomökonomie verwendet, einfache Ausgangsstoffe verwenden würde, um ein Produkt aufzubauen, anstatt große Moleküle aufzuspalten und dabei viele Abfallprodukte zu produzieren.
Betrachten Sie die Reaktionen, in denen Magnesiumoxid das gewünschte Produkt ist:
2Mg + O2 → 2MgO
2 x 24 = 48 g 32 g 2 x 40 = 80 g
Atomökonomie = (80 / (48 + 32)) x 100 = 100%
MgCO3 → MgO + CO2
84 g 40 g 44 g
Atomökonomie = (40 / 84) x 100 = 48%
Leistungsstärkere Schülerinnen und Schüler möchten vielleicht nachrechnen, wie die Veränderungen in der Produktion von Ibuprofen die Atomökonomie verbessernw2.
References
- Anastas PT, Warner C (1998) Green Chemistry Theory and Practice. New York, NY, USA: Oxford University Press. ISBN: 0198502346
- Trost BM (1991) The atom economy – a search for synthetic efficiency, Science 254: 1471–1477
Web References
- w1 – Die 12 principles of green chemistry können auf der Homepage der American Chemistry Society nachgelesen werden.
Die ACS Homepage bietet außerdem große Menge Unterrichtsressourcen zu grüner Chemie, inklusive Büchern, Weblinks und Versuchsprotokolle für alle Altersstufen (von Sekundarstufe I bis zum Bachelorstudium). - w2 – Die Lernhomepage der Royal Society of Chemistry bietet eine Unterrichtsstunde zur Synthese von Ibuprofen, die auch die Struktur und Bindungen des Medikaments betrachtet.
Resources
- Für praktische Unterrichtsaktivitäten verbunden mit Klimawandel, verwenden Sie:
- Shallcross D, Harrison T (2008) Practical demonstrations to augment climate change lessons. Science in School 10: 46–50.
- Shallcross D, Harrison T, Henshaw S, Sellou L (2009) Brennstoffe im Blickpunkt: Experimente zum Klimawandel. Science in School 11: 38–43.
- Shallcross D, Harrison T, Henshaw S, Sellou L (2009) Looking to the heavens: climate change experiments. Science in School 12: 34–39.
Review
Wie die Autoren herausstellen, ist die Chemie unter Studenten und der Öffentlichkeit von einer negativen Aura umgeben, aber die Chemie hinter Gegenständen und Materialien ist aus unserem täglichen Leben nicht wegzudenken. Das ist der Grund, weshalb ich diesen Artikel für den Einstieg in einen Chemiekurs in der Sekundarstufe empfehle.
Die Ideen hinter der grünen Chemie werden klar präsentiert, unter Verwendung eines einfachen Stils mit Beispielen aus dem Alltag, von der Synthese von Medikamenten bis hin zu Bio-Kraftstoffen. Das Thema ist natürlich wert, tiefergehend betrachtet zu werden und profitiert, wenn möglich, von praktischen Anwendungen.
Beide Möglichkeiten stehen durch die zitierten Weblinks zur Verfügung (ACS Website und Lern-Homepage der Royal Society of Chemistry).
Darüber hinaus kann die Geschichte von chemischen Unfällen, wie dem Bhopal Desaster, Lehrern und Schülern Diskussionsanlässe zur chemischen Sicherheit, Nachhaltigkeit und die Rolle der grünen Chemie eröffnen.
Gulia Realdon, Italien





