Neutronen zur Bekämpfung von HIV Understand article
Übersetzt von Korinna Kochinke. Die am häufigsten benutzte Form der Strukturanalyse ist sicherlich die Röntgenstrukturanalyse, aber Neutronen können gleichermaßen zu diesem Zweck genutzt werden – und könnten darüber hinaus noch im Kampf gegen HIV helfen.
Erwähnt man Kristallographie denken die meisten gleich an Röntgenstrahlen. Dies ist nicht weiter verwunderlich, wenn man bedenkt, dass die Strukturen von mehr als 88 000 Proteinen, Nukleinsäuren, Viren und Makromolekülen durch die Verwendung von Röntgenstrahlen bestimmt worden sind. Aber durch die Verbesserung der Neutronenstreuung wird diese immer häufiger als Hilfe zur Herstellung von Medikamenten herangezogen. Wissenschaftler am Institut Laue-Langevin (ILL) in Grenoble, Frankreich, haben diese Möglichkeit genutzt um zu verstehen, wie ein antiretrovirales Medikament HIV angreift.

Mit freundlicher Genehmigung von ILL
Seit der Entdeckung der Röntgenstrahlung vor rund 100 Jahren hat die Technik eine dramatische Entwicklung durchgemacht und ist mittlerweile weit verbreitet. Durch hochintensive Röntgenstrahlen, die von synchrotonen Strahlungsquellen erzeugt werden, ist es möglich, routinemäßig Daten von winzigen Kristallen im Durchmesser von wenigen Mikrometern in Sekundenschnelle zu erheben (siehe Cornuejols, 2009).
Im Gegensatz dazu ist die Neutronenstrahlung für die Strukturanalyse von Makromolekülen weit weniger stark entwickelt worden und ihre Anwendung ist deswegen auch nicht so weit verbreitet. Dies ist hauptsächlich dadurch begründet, dass die Anzahl der Partikel per Quadratzentimeter pro Sekunde (die Teilchenflussdichte) selbst der stärksten Neutronenquellen mehrere Größenordnungen unter denen vergleichbarer Röntgenstrahlquellen liegen.
Dies hatte zur Folge, dass bis vor kurzem große Kristalle und monatelange Expositionsdauern erforderlich waren um aussagekräftige Daten sammeln zu können. Jedoch haben jüngste Weiterentwicklungen die Datenerhebung unter Verwendung wesentlich kleinerer Kristalle in nur wenigen Tagen ermöglicht. Allerdings ist das immer noch länger, als die meisten auf Röntgenstrahlung basierenden Experimente dauern. Warum also sollte man Neutronenstrahlung benutzen? Einer der Gründe stellt das kleinste Atom des Universums dar: Wasserstoff.
Die Bedeutung von Wasserstoff
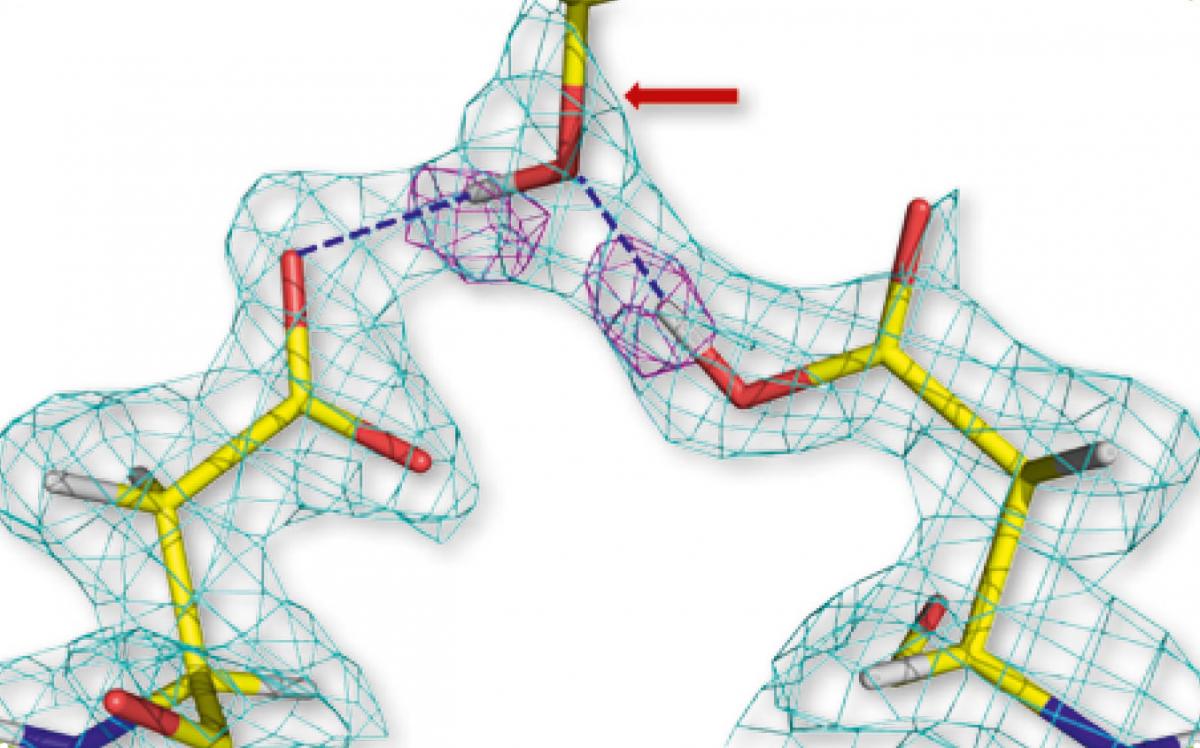
Asparaginsäurereste zweier
HIV-1 Proteasen (links und
rechts) sind über
Wasserstofbrückenbindungen
mit der Hydroxylgruppe des
Medikamentes Aprenavir
(Mitte) verbunden. In Pink
sind Wasserstoffatome
dargestellt
Mit freundlicher Genehmigung
von Andrev Kovalevsky
Die meisten Medikamente entfalten ihre Wirkung dadurch, dass sie an ein spezifisches, an der Krankheit beteiligtes Enzym (Target) binden und dieses damit blockieren. Deswegen konzentriert sich ein großer Teil der modernen Medikamentenentwicklung darauf, die Interaktionen zwischen Medikament und Ziel zu analysieren und zu verbessern. Zur Bestimmung struktureller Details wurde meistens die Röntgenstrahlung eingesetzt, aber diese hat einen Nachteil: Sie kann die Position der Wasserstoffatome in einem Molekül nicht wiedergeben. Wasserstoffatome spielen aber oft eine entscheidende Rolle, da sie zwar schwache, aber wichtige Interaktionen, die sogenannten Wasserstoffbrückenbindungen, ausbilden.
Im Gegensatz dazu können Neutronen die Positionen aller Atome, und damit eben auch die von Wasserstoff, lokalisieren. Folglich stellt die Neutronenstrahlung ein bedeutendes Instrument für die Analyse der Interaktionen zwischen Medikamenten und Targets dar. Dies konnte kürzlich für ein antiretrovirales Medikament gegen HIV (Amprenavir) und seinem Zielenzym, die HIV-1 Protease, gezeigt werden. Diese Protease ist ein Schlüsselenzym im HIV-Lebenszyklus: sie spaltet virale Polypeptide von neu synthetisierten Proteinen ab und überführt sie somit in ihre funktionelle Form, so dass die Proteine reifen und die Produktion neuer infektiöser Viruspartikel erfolgen kann.
Wissenschaftler haben Neutronen auf ein winziges Kristall von an Amprenavir gebundener HIV-1 Protease (nur 0,2 mm3 groß) gefeuert, um Daten in der Auflösung von gerade mal 0,2 Nanometern zu erhalten. Diese Daten erlaubten den Wissenschaftlern die Wasserstoffatome im Enzym-Medikamenten-Komplex zu lokalisieren, und darüber hinaus diejenigen Atome zu identifizieren, die an der Ausbildung von Wasserstoffbindungen beteiligt sind.
Höhere Auflösung
Basierend auf vorherigen Röntgenstrahlen-Analysen haben Wissenschaftler spekuliert, dass mehrere Wasserstoffbindungen ausschlaggebend für die Bindung zwischen HIV-1 Protease und Amprenavir sein müssten. Jedoch offenbarte die Neutronenstudie, dass tatsächlich nur zwei starke direkte Wasserstoffbrückenbindungen zwischen dem Medikament und dem Enzym existieren (siehe Abbildung 1). Diese Ergebnisse eröffnen den Entwicklern von Medikamenten nun neue Wege um die Bindung zu verstärken, in dem sie die Molekularstruktur des Medikaments leicht verändern. Dies könnte die Effektivität des Arzneimittels erhöhen, so dass die notwendige Einnahmedosis verringert werden könnte.
Medikamentenentwickler könnten zum Beispiel die beiden Wasserstoffbindungen stärken, in dem sie ein reaktives Atom wie Fluor in das Medikament einbauen. Alternativ könnten sie weitere direkte Wasserstoffbrückenbindungen erzeugen, in dem sie zum Beispiel größere Gruppen an Atomen in die Struktur inkorporieren, die die Wassermoleküle, die sich in der jetzigen Form innerhalb der Bindungsstelle befinden, hinausdrängten.
Die einmalige Sensitivität der auf Neutronenstrahlen basierenden Strukturanalyse für Wasserstoffatome bietet der pharmazeutischen Industrie ein neues, leistungsstarkes Werkzeug für die strukturbasierte Entwicklung von Medikamenten. Aufgrund der hohen Auflösung wird die Bedeutung der Röntgenstrukturanalyse für die nächsten Jahre sicherlich hoch bleiben, aber die Nutzung beider Methoden, Röntgen- und Neutronenstrahlung, hat das größte Potential um die Interaktion zwischen Medikament und Zielprotein zu enthüllen. Somit besteht die Aussicht, dass zukünftig die Effizienz vieler Arzneimittel verbessert werden kann.
Neutronenstrahlung
Platziert man einen Kristall in einen Röntgenstrahl, interagieren die Röntgenstrahlen mit den Elektronenwolken der Atome in dem Kristall. Dies veranlasst eine Diffraktion (=Streuung) der Strahlung in spezifische Richtungen. Misst man die Winkel und Intensitäten dieser Beugungspunkte (auch Reflektion genannt), kann man ein dreidimensionales Bild der Elektronendichte im Kristall erzeugen. Aus diesem kann man dann auf die Positionen des Atome im Kristall rückschließen.
Konzeptionell ist die Neutronenbeugung diesem sehr ähnlich, mit der Ausnahme, dass die Neutronen von dem Nukleus der Atome im Kristallgitter gebeugt werden, und nicht von den Elektronenwolken um die Atome. Deswegen korreliert die Stärke der Streuung für unterschiedliche Atomtypen auch nicht mit der Elektronenkonfiguration, sondern mit den Kräften im Nukleus. Diese wiederum können bereits zwischen unterschiedlichen Isotopen eines Elementes variieren.
Aufgrund ihrer kleinen Elektronenwolken haben Wasserstoff- und Deuteriumatome keinen großen Effekt auf Röntgenstrahlen. Bei Neutronenstrahlung hingegen zeigen sie ähnlich starke Effekte wie andere weit verbreitete Elemente in biologischen Makromolekülen: Kohlenstoff, Stickstoff, Sauerstoff und Schwefel. Dies ist die Ursache, warum Wasserstoff und Deuterium bei der Verwendung von Röntgenstrahlung nicht sichtbar sind, bei Neutronenbeugung aber sehr wohl.
Die Sichtbarkeit von Wasserstoff und Deuterium bei der Neutronenbeugung ermöglicht es, ihre Positionen bei einer Auflösung von circa 1,5 und 2,5 Å (1.5 x 10-10 m and 2.5 x 10-10 m) zu bestimmen. Ein Wasserstoffatom hat einen ungefähren Durchmesser von 1 Å. Dies macht die makromolekurare Kristallographie basierend auf Neutronenbeugung besonders nützlich für Studien, in denen die Position von Wasserstoffatomen wichtig ist, wie zum Beispiel Untersuchungen zu Enzymmechanismen oder Bindungsstudien von Arzneimitteln. Bei letzteren können Details über die Interaktionen der Wasserstoffbrückenbindungen bei der Entwicklung der Medikamente entscheidend sein.
Das ILL
Das Institut Laue-Langevin (ILL)w1ist ein internationales Forschungszenter in Grenoble, Frankreich. Seit Beginn der Versuche in 1972 hat dieses Institut 40 Jahre lang die Wissenschaft und Technologie der Neutronenbeugung angeführt. Das ILL verfügt über eine der stärksten Neutronenquelle der Welt, die Strahlen von Neutronen einer Serie von 40 Hochleistungsinstrumenten zuführt, und die kontinuierlich verbessert werden. Jährlich kommen 1200 Wissenschaftler aus über 40 Ländern an das ILL um ihre Experimente aus dem Bereichen kondensierte Materie, Chemie, Biologie, Nuklearphysik und Materialwissenschaften durchzuführen.
ILL gehört dem EIROforumw2 an, dem Herausgeber von Science in School. Hier finden Sie eine Liste von allen die ILL betreffenden Artikeln in Science in School.
References
- Cornuejols (2009) Biological crystals: at the interface between physics, chemistry and biology. Science in School 11: 70–76.
Web References
- w1 – Weiterführende Information zum ILL.
- w2 – EIRO forum ist eine Kollaboration zwischen acht der größten europäischen zwischenstaatlichen Forschungsorganisationen, die ihre Resourcen, Einrichtungen und Fachwissen kombinieren, um der Wissenschaft in Europa zum Ausschöpfen ihres vollen Potentials zu verhelfen. Im Rahmen ihres Bildungsprogrammes publiziert EIROforum Science in School.
Resources
- Wissenschaftler haben die Neutronenstrahlung auch erfolgreich dafür genutzt um die Frage zu beantworten, wie arktischer Fische durch Frostschutzmittel in ihrem Blut ein Leben bei Minusgraden führen können. Nachzulesen unter:
- Blakely M, Hayes E (2011) Neutronen und Frostschutz: Forschung an arktischen Fischen. Science in School 20: 18–22.
Institutions
Review
Dies ist ein interessanter Artikel, der zeigt, wie Fortschritte in verschiedenen Gebieten der Wissenschaft dazu führen können, die Entwicklung neuer Medikamente zum Wohle der Menschheit voranzutreiben, wie hier im Falle der Neutronenstrahlung.
Der Artikel ist als Hintegrundinformation für Lehrer gedacht und kann dazu dienen, den naturwissenschaftlichen Unterricht mit einem praxisnahen Beispiel anzureichern. Er kann auch dazu herangezogen werden, um, besonders bei älteren Schülern, Verständnis abzufragen oder Diskussionen anzuregen. Je nach Lehrinhalt oder Fokus des Lehrers können unterschiedliche Fragen gestellt werden. Zum Beispiel nach dem Vorteil von Neutronenstrahlung gegenüber Röntgenstrahlen.
Paul Xuereb, Malta





