Μοριακή γαστρονομία στο μάθημα της Χημείας Teach article
Μετάφραση από τον Θοδωρή Χαραλάμπη (Theodoros Charalampis)-Χημικός. Τα αλγινικά σφαιρίδια είναι χρήσιμα τόσο στο μάθημα της Χημείας όσο και στη μοριακή γαστρονομία.
Η μοριακή γαστρονομία αποτελεί μία νέα τάση στην υψηλή κουζίνα, με τους σεφ να προσφέρουν στους πελάτες τους νέες και παράξενες γευστικές εμπειρίες χρησιμοποιώντας υγρό άζωτο, γέλες και αφρό. Μία από τις τεχνικές της που αρχίζει να γίνεται ευρέως γνωστή είναι η χρήση αλγινικών σφαιριδίων που περιέχουν διάφορους χυμούς φρούτων καθώς και διαφορετικές γεύσεις. Ακόμα και αν δεν συχνάζετε σε εστιατόρια βραβευμένα με αστέρια Michelin, μπορεί να έχει πέσει στην αντίληψή σας το τσάι με φυσαλίδες.
Το τσάι με σφαιρίδια, που έκανε την εμφάνισή του αρχικά στην Ταϊβάν τη δεκαετία του 1980, πέρασε από την Ανατολική Ασία στην Δύση πριν από μερικά χρόνια. Αποτελείται από ένα ποτό που έχει σαν βάση του το τσάι και περιέχει ζελεδάκια φρούτων, ταπιόκα ή αλγινικά σφαιρίδια, γεμάτα με χυμό φρούτων ή σιρόπι.
Η παρασκευή και η εξέταση της συμπεριφοράς των αλγινικών σφαιριδίων μπορεί να είναι εντυπωσιακή και να αξιοποιηθεί στην επαγωγική μάθηση κατά τη διδασκαλία των φυσικών επιστημών.
Σε αυτό το άρθρο, προτείνονται τρόποι με τους οποίους μπορούν να αξιοποιηθούν τα αλγινικά σφαιρίδια στη διδασκαλία διαφόρων επιστημονικών εννοιών, και να παρουσιαστούν επιστημονικά φαινόμενα με έναν καλαίσθητο τρόπο. Παρουσιάζουμε τον τρόπο παρασκευής αλγινικών σφαιριδίων και προτείνουμε τρία πειράματα ως παραδείγματα, καθένα από τα οποία μπορεί να πραγματοποιηθεί στη διάρκεια μίας διδακτικής ώρας : μία αντίδραση οξέος – βάσης, χημειοφωταύγεια μέσω οξειδοαναγωγής και συναγωγή θερμότητας αξιοποιώντας ένα θερμοχρωμικό φαινόμενο.
Δημιουργία αλγινικών σφαιριδίων
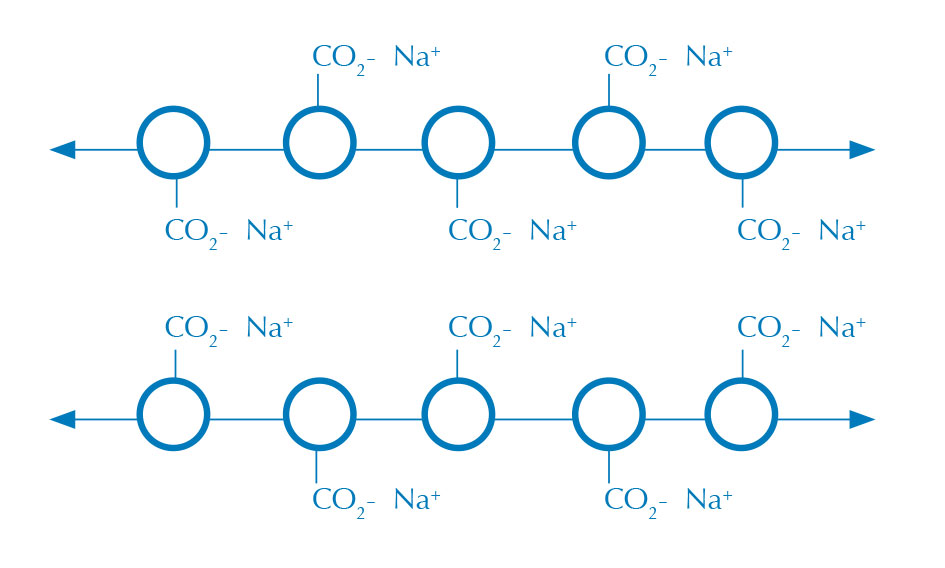
πολυμερές σε διάλυμα
NaCl (χωρίς
διασταυρούμενους δεσμούς)
Η εικόνα είναι ευγενική
προσφορά της Nicola Graf
Τα αλγινικά σφαιρίδια παράγονται κατά την επαφή υδατικού διαλύματος αλγινικού άλατος (σχήμα 1) με διάλυμα ιόντων ασβεστίου οπότε και δημιουργείται μία μεμβράνη αλγινικού ασβεστίου στη διεπιφάνεια των δύο διαλυμάτων (σχήμα 2). Το αλγινικό οξύ είναι ένας μακρύς πολυσακχαρίτης που σχηματίζει σταυροδεσμούς παρουσία δισθενών κατιόντων, όπως τα ιόντα ασβεστίου, οδηγώντας στην παραγωγή ενός αδιάλυτου στο νερό πηκτώματος.
Υλικά
- 2 g αλγινικό νάτριο (Na(C6H8O6))
- 100 mL απιονισμένο νερό
- 10 mL διαλύματος χλωριούχου ασβεστίου (CaCl2) 0,5 % ή διαλύματος γαλακτικού ασβεστίου (Ca(C3H5Ο3)2) 1 %
- Δύο ποτήρια ζέσης των 250 mL
- Πιπέτες ή κουτάλι
- Γυάλινη ράβδος ή άλλο μέσο ανάδευσης
- Σίτα ή κουτάλι
Διαδικασία
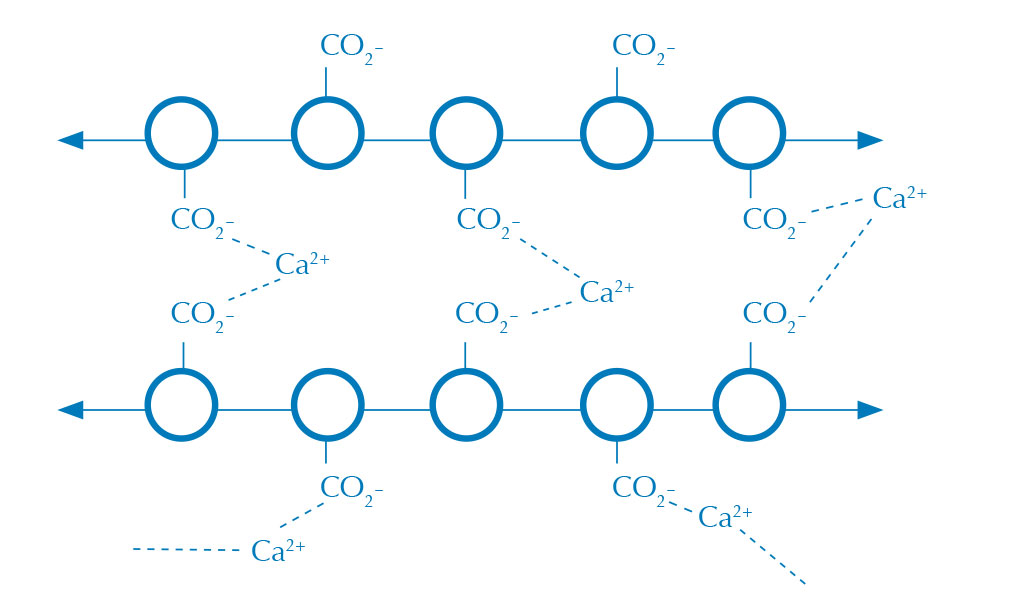
πολυμερές σε διάλυμα CaCl2
(με διασταυρούμενους
δεσμούς)
Η εικόνα είναι ευγενική
προσφορά της Nicola Graf
- Αναμίξτε το αλγινικό νάτριο με το νερό στο ένα ποτήρι ζέσης
- Περιμένετε τουλάχιστον 15 λεπτά έως ότου έχει διαλυθεί όλο το αλγινικό νάτριο
- Μεταφέρετε το διάλυμα των ιόντων ασβεστίου στο άλλο ποτήρι ζέσης
- Προσθέστε σταγόνες του διαλύματος του αλγινικού νατρίου στο διάλυμα των ιόντων ασβεστίου με μία πιπέτα ή με ένα κουτάλι. Ανακατέψτε το διάλυμα των ιόντων ασβεστίου για να μην κολλήσουν τα αλγινικά σφαιρίδια μεταξύ τους.
- Τα σφαιρίδια είναι σταθερά και μπορούν να απομακρυνθούν από το διάλυμα των ιόντων ασβεστίου με ένα κουτάλι ή με μία σίτα.
Κατά την επαφή των δύο υγρών σχηματίζεται ζελατινοειδές αλγινικό ασβέστιο υπό τη μορφή σφαιριδίων εγκλωβίζοντας στο εσωτερικό τους το αλγινικό διάλυμα. Αν στο αλγινικό διάλυμα έχουν προστεθεί άλλες ουσίες, όπως αρωματικές ουσίες, χρωστικές ουσίες ή δείκτες, τότε και αυτές θα εγκλωβιστούν στα σφαιρίδια.
Όξινα – Βασικά σφαιρίδια
Υλικά
- 2 g αλγινικό νάτριο (Na(C6H8O6))
- 500 mL απιονισμένο νερό
- 10 mL διαλύματος χλωριούχου ασβεστίου (CaCl2) 0,5 % ή διαλύματος γαλακτικού ασβεστίου (Ca(C3H5Ο3)2) 1 %
- Τρία ποτήρια ζέσης των 250 mL
- Πιπέτες ή κουτάλι
- Γυάλινη ράβδος ή άλλο μέσο ανάδευσης
- Σίτα (προαιρετικά)
- Δείκτη
- Διάφορα οξέα και βάσεις
Διαδικασία
- Ακολουθήστε την προαναφερόμενη διαδικασία παραγωγής αλγινικών σφαιριδίων, προσθέτοντας όμως έναν δείκτη στο αλγινικό διάλυμα πριν την προσθήκη του στο διάλυμα του ασβεστίου.
- Απομακρύνετε τα σφαιρίδια και μεταφέρετέ τα σε ένα ποτήρι ζέσης που περιέχει το υπόλοιπο απιονισμένο νερό.
- Παρατηρείστε το χρώμα των σφαιριδίων.
- Προσθέστε διαδοχικά διάφορα οξέα και βάσεις στο νερό και παρατηρείστε πως αλλάζει το χρώμα των σφαιριδίων.
Παρ’ όλο που ο δείκτης βρίσκεται στο εσωτερικό των σφαιριδίων, η αλγινική μεμβράνη επιτρέπει την ανταλλαγή κατιόντων υδρογόνου ή υδροξωνίων (ενυδατομένα ιόντα υδρογόνου) μεταξύ του εσωτερικού των σφαιριδίων και του εξωτερικού υγρού. Αλλαγή στην τιμή του pH του εξωτερικού υγρού με την προσθήκη ενός οξέος ή μίας βάσης θα επιφέρει αλλαγή στο pH στο εσωτερικό των σφαιριδίων και συνακόλουθα αλλαγή του χρώματος του δείκτη (σχήμα 3).
Ενώ τεχνητοί δείκτες μπορούν να χρησιμοποιηθούν στην τάξη, στο σπίτι μπορούν να χρησιμοποιηθούν εκχυλίσματα ευαίσθητα στις μεταβολές του pH όπως αυτό του κοκκινολάχανου ή από φλούδες από ραπανάκια.
Φωτοβόλα σφαιρίδια
Αλγινικά σφαιρίδια μπορούν να χρησιμοποιηθούν στην παρουσίαση του φαινομένου της χημειοφωταύγειας απλά με την προσθήκη μίας φωτοβόλου ένωσης στο αλγινικό διάλυμα πριν τον σχηματισμό των σφαιριδίων. Ένας εύκολος τρόπος είναι να χρησιμοποιηθεί ριβοφλαβίνη (βιταμίνη Β2) που φωσφορίζει κατά την έκθεσή της στην υπεριώδη ακτινοβολία. Ενώ μπορεί να χρησιμοποιηθεί καθαρή ριβοφλαβίνη, μπορεί να απομονωθεί και από τροφές όπως είναι οι κρέμες στιγμής σε σκόνη που την περιέχουν.
Υλικά
Εξαγωγή της ριβοφλαβίνης (προαιρετικά):
- Ένα πακέτο κρέμα στιγμής σε σκόνη που περιέχει ριβοφλαβίνη (γνωστή ως Ε101)
- 200 mL απεσταγμένο νερό
- Ποτήρι ζέσης
- Αναδευτήρα
- Χωνί με διηθητικό χαρτί
Για την δημιουργία των φωτοβόλων σφαιριδίων:
- Σκόνη ριβοφλαβίνης (2 φορές στην άκρη της σπάτουλας)
- 2 g αλγινικό νάτριο (Na(C6H8O6))
- 100 mL απιονισμένο νερό
- 10 mL διαλύματος χλωριούχου ασβεστίου 0,5 % ή διαλύματος γαλακτικού ασβεστίου 1 %
- Δύο ποτήρια ζέσης των 250 mL
- Πιπέτες ή κουτάλι
- Γυάλινη ράβδος ή άλλο μέσο ανάδευσης
- Σίτα (προαιρετικά)
- Πηγή υπεριώδους ακτινοβολίας
- 15 – 20 mL πυκνό διάλυμα διθειονικού νατρίου (Na2S2O4)
- 15 – 20 mL υπεροξείδιο του υδρογόνου
Διαδικασία
- Για την εξαγωγή της ριβοφλαβίνης από την κρέμα στιγμής σε σκόνη, βάλτε περίπου 8 g σκόνης σε ένα ποτήρι ζέσης μαζί με 200 mL απιονισμένο νερό. Αναδεύστε καλά για 10 περίπου λεπτά και διηθήστε.
- Ακολουθήστε την προαναφερόμενη διαδικασία παραγωγής αλγινικών σφαιριδίων, προσθέτοντας όμως την ριβοφλαβίνη στο αλγινικό διάλυμα πριν την προσθήκη του στο διάλυμα του ασβεστίου.
- Φωτίστε με την πηγή υπεριώδους ακτινοβολίας τα σφαιρίδια καθώς σχηματίζονται. Θα φωτοβολούν εκπέμποντας ένα κιτρινοπράσινο φώς (σχήμα 4).
- Σβήστε την πηγή υπεριώδους ακτινοβολίας και τα σφαιρίδια θα πάψουν να φωτοβολούν.
- Ανάψτε πάλι την πηγή.
- Προσθέστε το διθειονικό νάτριο στο ποτήρι με αλγινικά σφαιρίδια. Θα διαπιστώσετε ότι τα σφαιρίδια θα πάψουν να φωτοβολούν καθώς το διθειονικό νάτριο διαπερνά τη μεμβράνη που περιβάλλει τα αλγινικά σφαιρίδια και ανάγει την ριβοφλαβίνη στο εσωτερικό τους.
- Προσθέστε το υπεροξείδιο του υδρογόνου για να οξειδωθεί η ριβοφλαβίνη και τα σφαιρίδια θα φωτοβολούν πάλι.
Θερμοχρωμικά σφαιρίδια
Με την προσθήκη ενός θερμοχρωμικού μελανιού στο αλγινικό διάλυμα μπορεί κάποιος να παρουσιάσει το φαινόμενο της συναγωγής της θερμότητας. Στην Ιαπωνία, πουλιέται ένα ειδικό θερμοχρωμικό μελάνι που βασίζεται σε μία λακτόνη του κρυσταλλικού ιώδους (και να μη γίνει σύγχυση με θερμικά μελάνια που χρησιμοποιούνται στους θερμικούς εκτυπωτές) και χρησιμοποιείται για την παρουσίαση φαινομένων της φυσικής που σχετίζονται με τη θερμότητα.
Υλικά
- 2 g αλγινικό νάτριο
- 100 mL απιονισμένο νερό
- 10 mL διαλύματος χλωριούχου ασβεστίου 0,5 % ή διαλύματος γαλακτικού ασβεστίου 1 %
- Δύο ποτήρια ζέσης των 250 mL
- Πιπέτες ή κουτάλι
- Γυάλινη ράβδος ή άλλο μέσο ανάδευσης
- Σίτα
- 3 – 5 mL ενός θερμοχρωμικού μελανιού
- Θερμοάντοχο ποτήρι ζέσης γεμάτο με νερό
- Εστία θερμότητας
Διαδικασία
- Ακολουθήστε την προαναφερόμενη διαδικασία παραγωγής αλγινικών σφαιριδίων, προσθέτοντας όμως το θερμοχρωμικό μελάνι στο αλγινικό διάλυμα πριν την προσθήκη του στο διάλυμα του ασβεστίου.
- Μεταφέρετε τα σχηματιζόμενα σφαιρίδια στο θερμοάντοχο ποτήρι με το νερό.
- Θερμάνετε το ποτήρι μέχρι τα σφαιρίδια να αρχίζουν να ανεβαίνουν προς τα πάνω.
Με την κίνηση των αλγινικών σφαιριδίων γίνεται εμφανής η διάδοση της θερμότητας : με την θέρμανσή τους, τα σφαιρίδια γίνονται λιγότερο πυκνά και ανεβαίνουν, ακολούθως ψύχονται και βυθίζονται καθώς γίνονται περισσότερο πυκνά. Ταυτόχρονα τα αλγινικά σφαιρίδια θα αλλάζουν χρώμα, αποδεικνύοντας ότι η συναγωγή της θερμότητας συνδέεται με αλλαγές στη θερμοκρασία.
Ευχαριστίες
Μέρος της παρούσης εργασίας χρηματοδοτήθηκε από το έργο Teaching Enquiry with Mysteries Incorporated (TEMI) (Peleg et al., 2015), υποστηρίχθηκε από την Ευρωπαϊκή Ένωση στο πλαίσιο του 7ου Προγράμματος-Πλαισίου για τη χρηματοδότηση της έρευνας «Επιστήμη και Κοινωνία» στο πλαίσιο της υπ.αρίθ. 321403 σύμβασης επιδότησης.
References
- Peleg R et al. (2015) The magic sand mystery. Science in School 32: 37-40.
Resources
- Για να μάθετε περισσότερα για την μοριακή γαστρονομία, δείτε:
- Davies E (2014) From methional to fried chicken. Science in School 30: 44–48.
- Για να μάθετε περισσότερα για την σφαιροποίηση στην μοριακή γαστρονομία, δείτε: www.molecularrecipes.com/spherification-class/basic-spherification
- Βίντεο που παρουσιάζει τον τρόπο για να παρασκευάσει κάποιος ένα βρώσιμο «μπουκάλι» νερού μπορείτε να βρείτε στον σύνδεσμο: www.youtube.com/watch?v=YLjzsfgk198
- Βίντεο όλων των πειραμάτων που περιγράφονται στο παρόν άρθρο μπορείτε να βρείτε στο κανάλι του ΤΕΜΙ στο Youtube. Δείτε: www.youtube.com/channel/UC62-j3UpwF-Z5yh84umnxIQ
- Για ένα podcast για το αλγινικό νάτριο, επισκεφτείτε την ιστοσελίδα του Chemistry World website.
- Περιγραφή στα γερμανικά της χρήσης σφαιριδίων με βάση τις αρχές της διερευνητικής μάθησης, ακολουθώντας τη φιλοσοφία του ΤΕΜΙ, μπορείτε να κατεβάσετε από την ιστοσελίδα της ομάδας του ΤΕΜΙ στο πανεπιστήμιο της Βρέμης, στη Γερμανία. Δείτε: www.chemiedidaktik.uni-bremen.de/temi/index.html. Μία μετάφραση στα αγγλικά θα δημοσιευθεί σύντομα στο Βιβλίο των επιστημονικών μυστηρίων στην ιστοσελίδα του ΤΕΜΙ: www.teachingmysteries.eu
- Η σφαιροποίηση μπορεί να αξιοποιηθεί και σε μία σειρά άλλων πειραμάτων. Για μία δράση στην οποία «αλγόμπαλες» αξιοποιούνται στην εξερεύνηση του φαινομένου της φωτοσύνθεσης, για παράδειγμα, δείτε το www.saps.org.uk ή συνδεθείτε απευθείας στον σύνδεσμο: http://tinyurl.com/qxwcafa
- Τα περισσότερα από τα αντιδραστήρια και τα σκεύη που θα χρειαστείτε για αυτές τις έρευνες μπορείτε να τα προμηθευτείτε εύκολα από τους προμηθευτές επιστημονικού εξοπλισμού για σχολεία. Αν δεν μπορείτε να βρείτε κάποιον προμηθευτή για το ιαπωνικό θερμοχρωμικό μελάνι, θα μπορείτε να αγοράσετε θερμοχρωμικούς πολτούς για χρήση τους στο νερό από εξειδικευμένους παρασκευαστές χρωστικών όπως την SpecialFX & Coatings στη Μεγάλη Βρετανία. Επισκεφτείτε το: www.sfxc.co.uk
Review
Την περιέργειά μας πάντα έλκυαν αλλαγές του χρώματος, της θέσης, του σχήματος και του φωτός. Αξιοποιώντας τέτοιες αλλαγές στη διδασκαλία μας βοηθάμε τους μαθητές μας να απολαύσουν ακόμα περισσότερο τις επιστήμες. Η πρώτη και η δεύτερη δραστηριότητα είναι κατάλληλες για μαθητές ηλικίας 15 – 16, ενώ η τρίτη δραστηριότητα, που εμπλέκει την συναγωγή και τη χημειοφωταύγεια, είναι καταλληλότερη για μικρότερους μαθητές, ηλικίας 11 – 14.
Μετά από τις δραστηριότητες, ο εκπαιδευτικός μπορεί να ρωτήσει γιατί χρησιμοποιήθηκαν τα σφαιρίδια, οδηγώντας σε μία συζήτηση για τις φυσικές και χημικές ιδιότητες της ύλης.
Enrico Capaccio, Istituto Superiore S Bellarmino, Montepulciano (Σιένα), Ιταλία





