Φυσικά πειράματα: χημεία με μανιτάρια Teach article
Πόσα ‘χημικά’ υπάρχουν σε ένα φρέσκο μανιτάρι; Αυτά τα απλά πειράματα αποκαλύπτουν την κρυμμένη χημεία μέσα στις φυσικές τροφές.
Τα πάντα γύρω μας και μέσα στο σώμα μας αποτελούνται από χημικές ενώσεις, οι οποίες αντιδρούν μεταξύ τους για να μας κρατούν ζωντανούς. Όμως, πολύ μαθητές δεν βλέπουν την χημεία ως μέρος της καθημερινής τους ζωής: στην πραγματικότητα η χημεία θεωρείται αντίθετη της ‘φύσης’ – ακόμα και κάτι επικίνδυνο που πρέπει να αποφεύγεται. Για παράδειγμα, πολλά φαγητά διαφημίζεται ότι ‘δεν έχουν χημικά’, λες και οι ουσίες που περιέχουν δεν αποτελούνται από μόρια και ενώσεις, αλλά από κάτι εντελώς διαφορετικό.
Αυτή φυσικά είναι μια σημαντική παρανόηση, που πολύ πιθανόν να οδηγήσει σε λάθη και αντιεπιστημονικές αποφάσεις. Στα άρθρα με τα ‘φυσικά πειράματα’ (δείτε επίσης Höfer, 2017), χρησιμοποιούμε χημικές μεθόδους για να αναλύσουμε φυσικές, ωμές τροφές. Ανεξαρτήτως αποτελέσματος, η πραγματοποίηση αυτών των πειραμάτων φέρνει τους μαθητές αντιμέτωπους με το αδιαμφισβήτητο γεγονός ότι οι υγιεινές, φυσικές τροφές είναι ουσίες επίσης μέσα στη σφαίρα της χημείας.

Skeeze/pixabay.com
Η χημεία των μανιταριών
Το φαγητό είναι μεγάλο μέρος της καθημερινής μας ζωής, οπότε είναι λογικό να χρησιμοποιήσουμε τις τροφές ως έναν τρόπο να συνδέσουμε τη χημεία με την καθημερινή μας ζωή. Τα μανιτάρια είναι ένα ενδιαφέρον παράδειγμα, διότι περιέχουν μια ποικιλία ουσιών που μπορούν να αναγνωριστούν πολύ εύκολα. Αυτό μπορεί να εκπλήξει τους μαθητές, που πιθανότατα θα ξεκινήσουν τα πειράματα με πολύ λίγες προσδοκίες σχετικά με την σύσταση των μανιταριών. Αυτές οι ουσίες περιλαμβάνουν υδατάνθρακες, λίπη και πρωτεΐνες, όπως επίσης βιταμίνες και ανόργανες ουσίες ως μικρότερης σημασίας συστατικά, όπως μπορούν και οι ίδιοι οι μαθητές να διαπιστώσουν μόνοι τους.
Σε αυτά τα πειράματα, εφαρμόζουμε βασικά εργαστηριακά τεστ σε βρώσιμα μανιτάρια. Τα πειράματα είναι κατάλληλα για μαθήματα χημεία σε σχολεία της δευτεροβάθμιας εκπαίδευσης. Μπορούν να εκτελεστούν από τους ίδιους τους μαθητές σε 1 ώρα περίπου, μαζί με τη συζήτηση. Για τους καθηγητές απαιτείται κάποιος επιπλέον χρόνος για την προετοιμασία των υλικών που χρειάζονται για τα πειράματα 2 και 3.

σώμα ενός καλλιεργημένου
μανιταριού
U.S. Department of
Agriculture/Flickr
Τι είναι τα μανιτάρια;
Τα μανιτάρια είναι μύκητες, οι οποίοι δεν είναι φυτά ή ζώα, αλλά σχηματίζουν το δικό τους ταξινομικό βασίλειο. Είναι ευκαρυωτικοί οργανισμοί, γεγονός που τα ξεχωρίζει από τα βακτήρια. Όπως και τα φυτά, τα μανιτάρια απορροφούν οργανικές θρεπτικές ουσίες από περιβάλλοντα υποστρώματα με ώσμωση, αλλά η δομή και ο τρόπος αναπαραγωγής τους είναι πολύ διαφορετικά από τα φυτά. Και όπως τα ζώα, τα μανιτάρια είναι ετερότροφοι οργανισμοί: χρειάζεται να προσλάβουν τροφή και δεν μπορούν να τη φτιάξουν μόνοι τους. Τα μυκητώδη κύτταρα δημιουργούν ένα δίκτυο ινών που ονομάζεται μυκήλιο, κρυμμένο μέσα στο έδαφος. Αυτό διακλαδίζεται σαν ένα σύστημα ριζών και είναι υπεύθυνο για την πρόσληψη θρεπτικών ουσιών. Οι μύκητες έχουν επίσης ένα καρποφόρο σώμα, το οποίο αναπτύσσεται πάνω από το έδαφος και είναι το (βρώσιμο μερικές φορές) κομμάτι, το οποίο αποκαλούμε μανιτάρι (δες εικόνα 1).
Θρεπτικά, τα μανιτάρια είναι πολύτιμο τμήμα της διατροφής μας. Μέσα σε άλλες θρεπτικές ουσίες, περιέχουν ιόντα νατρίου, χλωρίου και καλίου, τα οποία είναι απαραίτητα για τη διατήρηση της ισορροπίας του νερού. Επιπλέον φωσφορικά ιόντα για την σταθερότητα των οστών και των δοντιών και τον σχηματισμό των ερυθροκυττάρων. Βιταμίνη C, η οποία δρα ως προστατευτικός παράγοντας για τα κύτταρα και βοηθά το σώμα να ενσωματώσει το σίδηρο.
Στα ακόλουθα πειράματα, χρησιμοποιήσαμε μανιτάρια από μύκητες Agaricus bisporus, ανεπτυγμένους για εμπορικούς σκοπούς, ως δείγματα του υλικού, φρέσκα ή αποξηραμένα. Με γαστρονομικούς όρους, είναι γνωστά ως σαμπινιόν, λευκά μανιτάρια ή (όταν ωριμάσουν και γίνουν καφέ) μανιτάρια πορτομπέλο.
Συμβουλή ασφαλείας
Για όλα τα πειράματα, οι μαθητές θα πρέπει να φορούν προστατευτικά γυαλιά και να ακολουθούν τους συνηθισμένους κανόνες ασφαλείας για τα μαθήματα χημείας, αφού κάποια από τα αντιδραστήρια είναι επιβλαβή ή διαβρωτικά. Παρακαλώ δείτε επίσης τους γενικούς κανόνες ασφαλείας.
Πείραμα 1: Έλεγχος για παρουσία πρωτεΐνης
Δώστε περίπου 5 λεπτά για το τεστ με τη διουρία και 10 λεπτά για το τεστ με τη νινυδρίνη (δείτε το τμήμα με τη διαδικασία παρακάτω).
Υλικά
- Διάλυμα υδροξειδίου του νατρίου (1 mol/l)
- Διάλυμα θειικού χαλκού(ΙΙ) (1 mol/l)
- Διάλυμα νινυδρίνης (2% w/w)
- Φρέσκα βρώσιμα μανιτάρια (π.χ. λευκά μανιτάρια) – αρκετά για να πάρει ο κάθε μαθητής ή ομάδα από ένα
- Λίχνος Bunsen
- Ύαλος ωρολογίου
- Μαχαίρι (όχι πολύ κοφτερό)
- Μικρές εργαστηριακές πιπέττες
- Λαβίδες
Διαδικασία
Πρωτεΐνες μπορούν να ανιχνευθούν χρησιμοποιώντας και το τεστ της διουρίας και το τεστ της νινυδρίνης. Οι διαδικασίες αυτές περιγράφονται εδώ ξεχωριστά.
Αντίδραση διουρίας
- Κόψτε ένα μανιτάρι στη μέση (δείτε εικόνα 2, αριστερά).
- Χρησιμοποιώντας την πιπέτα, καλύψτε την κομμένη επιφάνεια του μανιταριού με μια λεπτή στρώση διαλύματος υδροξειδίου του νατρίου.
- Τοποθετήστε μια σταγόνα διαλύματος θειικού χαλκού(ΙΙ) στην επιφάνεια του μανιταριού.
Παρουσία πρωτεΐνες, το χρώμα θα αλλάξει από ανοιχτό γαλάζιο (το χρώμα του διαλύματος θειικού χαλκού(ΙΙ) ) σε σκούρο μπλε ή μωβ (δες εικόνα 2, μέση). Η αλλαγή αυτή του χρώματος οφείλεται στο σχηματισμό συμπλόκων χαλκού-πρωτεΐνης.
Αντίδραση νινυδρίνης
- Τοποθετήστε μια φέτα φρέσκου μανιταριού πάνω σε έναν ύαλο ωρολογίου.
- Ρίξτε μια σταγόνα διαλύματος νινυδρίνης πάνω σε ένα μανιτάρι.
- Χρησιμοποιώντας λαβίδες, κρατήστε τη φέτα του μανιταριού στο μη φωτεινό τμήμα της φλόγας ενός λίχνου Bunsen (η οποία δεν θα πρέπει να είναι δυνατή).
- Απομακρύνεται την φέτα του μανιταριού από τη φλόγα και κοιτάξτε το χρώμα.
Παρουσία πρωτεΐνης, θα δημιουργηθεί μια βαθιά μωβ ένωση (δείτε εικόνα 2, δεξιά). Η βαθιά μωβ ένωση ονομάζεται μωβ του Ruhemann. Παράγεται όταν η νινυδρίνη αντιδρά με τα αμινοξέα των πρωτεϊνών.
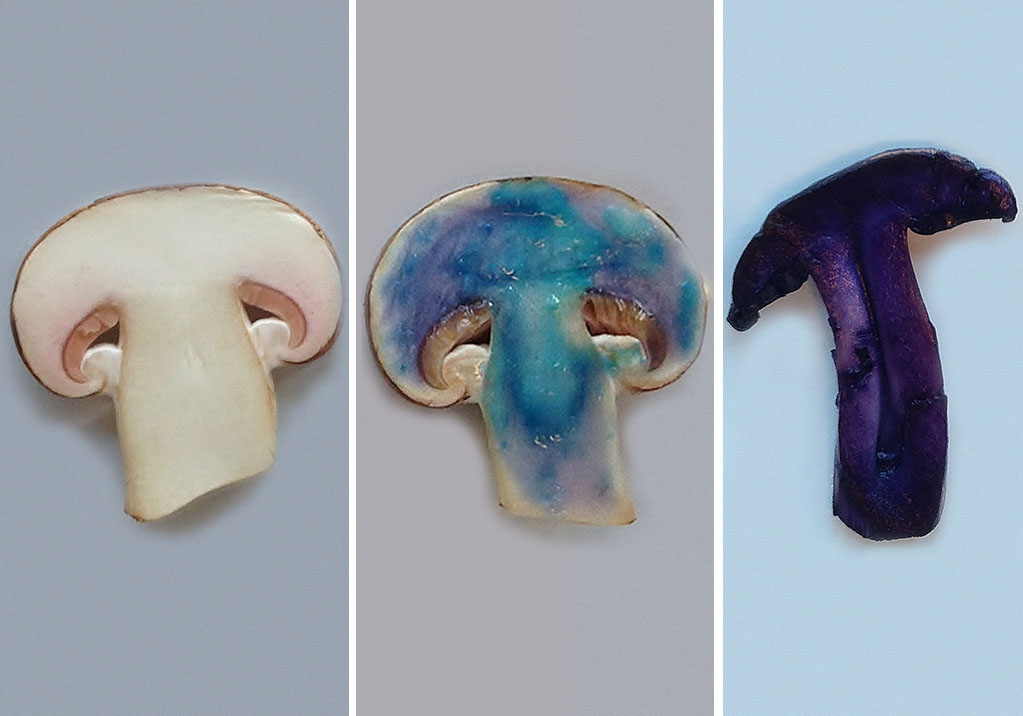
Farina Bunjes
Πείραμα 2: Έλεγχος για παρουσία βιταμίνης C
Διάρκεια: περίπου 15 λεπτά. Οι καθηγητές θα πρέπει να αφιερώσουν 45 λεπτά νωρίτερα για να προετοιμάσουν το διηθητικό χαρτί χλωριούχου σιδήρου (ΙΙΙ). Για να γίνει αυτό, μουλιάστε το διηθητικό χαρτί σε διάλυμα 1% w/w χλωριούχου σιδήρου(ΙΙΙ) και μετά αφήστε το μέχρι να στεγνώσει καλά (περίπου 30 λεπτά).
Υλικά
Κάθε μαθητής (ή ομάδα) θα χρειαστεί:
- Διάλυμα σιδηροκυανιούχου καλίου (1% w/w) σε έναν εξατμιστή/ξεκαστήρα
- Ένα διηθητικό χαρτί μουλιασμένο σε διάλυμα χλωριούχου σιδήρου(ΙΙΙ) και στεγνωμένου
- Ένα φρέσκο μανιτάρι
- Μαχαίρι (όχι πολύ κοφτερό)
- Θάλαμος νηματικής ροής
Διαδικασία
- Κόψτε ένα μανιτάρι στη μέση και πιέστε την φρεσκοκομμένη πλευρά του μανιταριού πάνω στο διηθητικό χαρτί (δείτε εικόνα 3, αριστερά).
- Απομακρύνετε το μανιτάρι. Καθώς δουλεύετε σε έναν θάλαμο νηματικής ροής, ψεκάστε το διηθητικό χαρτί με διάλυμα σιδηροκυανιούχου καλίου. Προσέξτε να μην εισπνεύσετε τον ατμό.
Το διάλυμα σιδηροκυανιούχου καλίου κάνει το χαρτί να γίνει ανοιχτό μπλε, λόγω παραγωγής της διαλυτής μορφής του πρωσσικού μπλε (ή μπλε του Turnbull). Παρουσία βιταμίνης C, τα ιόντα σιδήρου(ΙΙΙ) θα αναχθούν σε ιόντα σιδήρου(ΙΙ), σχηματίζοντας μια πιο σκούρα μπλε ένωση (δείτε εικόνα 3, δεξιά).

Farina Bunjes
Πείραμα 3: Έλεγχος για παρουσία καλίου και νατρίου
Διάρκεια: περίπου 10 λεπτά. Προετοιμάστε τα αποξηραμένα μανιτάρια εκ των προτέρων, κόβοντας τα μανιτάρια σε φέτες και αποξηραίνοντας τα κατά τη διάρκεια της νύχτας στους 105 °C σε κλίβανο ξήρανσης.
Το κάλιο και το νάτριο μπορούν να ανιχνευθούν μέσω των χαρακτηριστικών χρωμάτων της φλόγας. Η χρήση γυαλιού κοβαλτίου για να φιλτράρουμε την κίτρινη φλόγα του νατρίου, κάνει ορατή την χλωμή λιλά φλόγα του καλίου.
Υλικά
- Αποξηραμένα μανιτάρια
- Λίχνος Bunsen
- Λαβίδες πυράκτωσης
- Γυαλί κοβαλτίου ή άλλο φίλτρο μπλε φωτός
Διαδικασία
- Κρατείστε μία φέτα αποξηραμένου μανιταριού με λαβίδες πυράκτωσης σε μη φωτεινή φλόγα ενός λίχνου Bunsen.
- Παρατηρείστε το χρώμα της φλόγας. Το κιτρινο-πορτοκαλί χρώμα υποδεικνύει την παρουσία νατρίου, ενώ το λιλά χρώμα υποδεικνύει την παρουσία καλίου.
- Για να δείτε πιο εύκολα τη λιλά φλόγα, κοιτάξτε τη φλόγα μέσα από το μπλε φίλτρο, το οποίο απομακρύνει το κίτρινο χρώμα της φλόγας του νατρίου.

Farina Bunjes
Πείραμα 4: Δομική για παρουσία φωσφορικών ιόντων
Διάρκεια: περίπου 45 λεπτά (15 λεπτά για το πείραμα, συν 30 λεπτά για την προετοιμασία της στάχτης). Οι καθηγητές θα χρειαστούν επίσης 15 λεπτά για να προετοιμάσουν το διάλυμα επταμολυβδαινικού αμμωνίου.
Υλικά
Για το διάλυμα επταμολυβδαινικού αμμωνίου ((NH4)6Mo7O24):
- 10 g τετραϋδρομολυβδαινικού αμμωνίου
- 20 g νιτρικού αμμωνίου
- 7 ml συμπυκνωμένου διαλύματος αμμωνίας (30% w/w)
- Απεσταγμένο νερό
- Ογκομετρική φιάλη (100 ml)
- Πιπέτα
Για το πείραμα, κάθε ομάδα (ή μαθητής) θα χρειαστεί:
- Απεσταγμένο νερό
- Αποξηραμένα μανιτάρια (μερικές φέτες)
- Αραιωμένο νιτρικό οξύ (2 mol/l)
- Πιάτο πορσελάνης
- Γουδοχέρι (για άλεσμα)
- Λίχνος Bunsen
- Χωνί διήθησης και διηθητικό χαρτί
- Δοκιμαστικοί σωλήνες και βάση δοκιμαστικών σωλήνων
- Πιπέτα
- Πεχαμετρικό χαρτί
Διαδικασία

παράχθηκε από την καύση
αποξηραμένων μανιταριών
Farina Bunjes
Πριν το μάθημα, οι καθηγητές θα πρέπει να προετοιμάσουν ένα διάλυμα επταμολυβδαινικού αμμωνίου, διάλυμα ((NH4)6Mo7O24): τοποθετείστε 10 g τετραϋδρομολυβδαινικού αμμωνίου και 20 g νιτρικού αμμωνίου σε έναν ογκομετρικό σωλήνα. Προσθέστε 7 ml συμπυκνωμένου διαλύματος αμμωνίας (χρησιμοποιώντας πιπέτα) και γεμίστε την φιάλη μέχρι τα 100 ml με απεσταγμένο νερό, γίνεται έτσι πλήρης διάλυση.
Το υπόλοιπο μέρος της διαδικασίας είναι κατάλληλο για μαθητές.
- Προετοιμάστε τη στάχτη των μανιταριών. Πρώτα, τοποθετείστε τα μανιτάρια σε ένα πιάτο πορσελάνης, αλέστε τα και στη συνέχεια κάψτε τα αποξηραμένα μανιτάρια με μη φωτεινή φλόγα λίχνου Bunsen μέχρι να γίνουν στάχτη.
- Διαλύστε τη στάχτη των μανιταριών σε απεσταγμένο νερό (όχι παραπάνω από 10 ml) και μετά φιλτράρετε το διάλυμα για να ξεφορτωθείτε τα αδιάλυτα κομμάτια, συλλέγοντας το διήθημα.
- Οξεοποιήστε το διήθημα με αραιωμένο νιτρικό οξύ, έτσι ώστε το pH να είναι κάτω από 6. Σημείωση: θα χρειαστείτε το επακόλουθο οξεωποιημένο διάλυμα της στάχτης για το επόμενο πείραμα, όπως και για αυτό το πείραμα.
- Χρησιμοποιήστε μια πιπέτα για να βάλετε 5 ml από το οξεοποιημένο διαλύμα της στάχτης των μανιταριών σε δοκιμαστικό σωλήνα και μετά προσθέστε περίπου 10 σταγόνες από το διάλυμα επταμολυβδαινικού αμμωνίου χρησιμοποιώντας μια άλλη πιπέτα.
- Θερμάνετε το διάλυμα για δύο λεπτά με έναν λίχνο Bunsen και μετά τοποθετείστε τον σωλήνα στη βάση για να κρυώσει.
Παρουσία φωσφορικών ιόντων, θα σχηματιστεί λεμονί ίζημα φωσφομολυβδαινικού αμμωνίου ((NH4)3PMo12O40) (δείτε εικόνα 5).

Farina Bunjes
Πείραμα 5: Δοκιμή για την παρουσία χλωριούχων ιόντων
Διάρκεια: περίπου 5 λεπτά
Υλικά
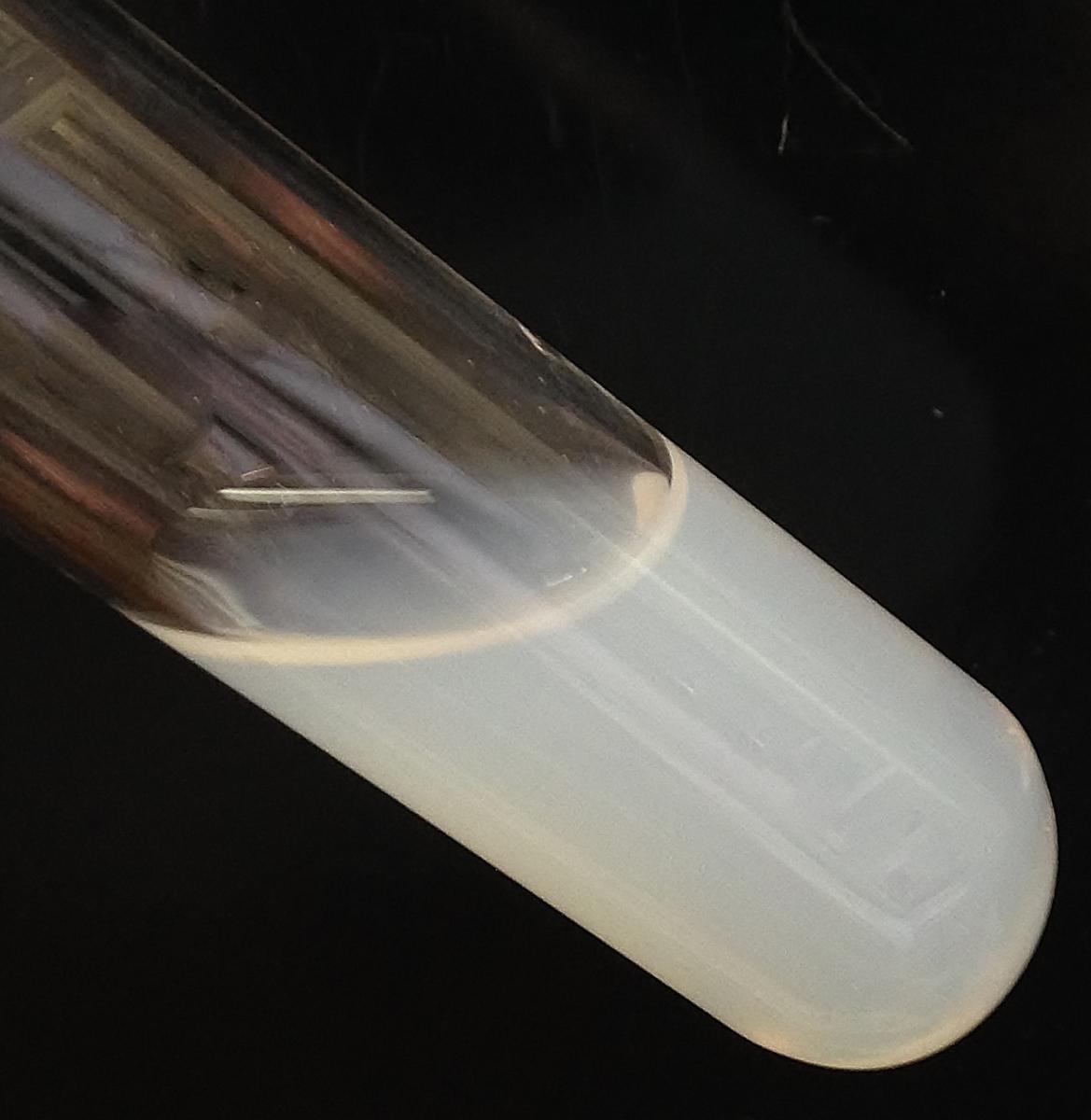
του χλωριούχου αργύρου σε
διάλυμα στάχτης
μανιταριού, υποδεικνύοντας
την παρουσία χλωριούχων
ιόντων
Farina Bunjes
- Οξεοποιημένο διάλυμα στάχτης μανιταριού (δείτε Πείραμα 4)
- Διάλυμα νιτρικού αργύρου (5% w/w)
- Δοκιμαστικός σωλήνας
- Πιπέτα
Διαδικασία
- Τοποθετείστε 3–5 ml οξεοποιημένου διαλύματος στάχτης μανιταριού σε ένα δοκιμαστικό σωλήνα.
- Προσθέστε μερικές σταγόνες νιτρικού αργύρου στον δοκιμαστικού σωλήνα χρησιμοποιώντας μια πιπέτα.
Το λευκό ίζημα υποδεικνύει την παρουσία χλωριούχων ιόντων (δείτε εικόνα 6). Το ίζημα χλωριούχου αργύρου (AgCl) διασκορπίζεται σε μικρά κομμάτια, με αποτέλεσμα το υγρό να έχει μια θολή άσπρη εμφάνιση.
Συζήτηση
Χρησιμοποιώντας αυτά τα πειράματα, οι μαθητές οι ίδιοι μπορούν να αναγνωρίσουν μερικές σημαντικές ενώσεις στα μανιτάρια – που είναι επίσης θρεπτικές ουσίες. Αυτό μπορεί να αποτελέσει τη βάση για συζήτηση πτυχών της χημείας που έχουν αντίκτυπο στην καθημερινή μας ζωή. Για παράδειγμα:
- Πώς θα αντιδρούσατε αν κάποιος έλεγε, ‘Προτιμώ τροφές χωρίς χημικά;’
- Πώς τα μανιτάρια υποστηρίζουν μια ισορροπημένη διατροφή;
- Μπορείτε να σκεφτείτε ένα πείραμα που θα μας βοηθήσει στη διάκριση φυτών και μανιταριών; (Θυμηθείτε ότι τα μανιτάρια δεν μπορούν να κάνουν φωτοσύνθεση, αλλά τα φυτά μπορούν.)
- Σε αυτά τα πειράματα, δεν έχουμε κάνει δοκιμή για την παρουσία αμύλου και γλυκόζης. Ποια νομίζετε ότι θα ήταν τα αποτελέσματα αν εξετάζατε για την παρουσία αυτών των ουσιών;
Η σύσταση των καλλιεργημένων μανιταριών
Οι ακόλουθες πληροφορίες μπορεί να είναι χρήσιμες για τους καθηγητές προς χρήση στη συζήτηση που θα ακολουθήσει μετά από τα πειράματα.
Υδατάνθρακες
Το άμυλο δεν είναι παρόν στα καλλιεργημένα μανιτάρια και η γλυκόζη είναι σχεδόν απούσα. Οι μύκητες περιέχουν κυρίως χιτίνη και κυτταρίνη ως δομικά συστατικά των κυτταρικών τοιχωμάτων. Περιέχουν επίσης τρεαλόζη (ένα σάκχαρο) και μανιτόλη (ένα αλκοολούχο σάκχαρο).
Λιπίδια (λίπος)
Τα λιπίδια εντοπίζονται σε πολύ μικρά σταγονίδια μέσα στο κυτταρόπλασμα των μυκήτων και στο μυκητώδη κυτταρικό τοίχωμα (ως λιπιδικές διπλοστοιβάδες). Τα μανιτάρια περιέχουν 0.3 g λίπους ανά 100 g φρέσκων μανιταριών, που είναι σχετικά μια μικρή αναλογία.
Ανόργανες ουσίες
Τα μανιτάρια είναι πλούσια σε ανόργανες ουσίες – ειδικά σε κάλιο, με ένα εκπληκτικά υψηλό επίπεδο 390 mg ανά 100 g στα φρέσκα μανιτάρια. Φώσφορος είναι επίσης παρόν (περίπου 60 mg ανά 100 g), κυρίως ως φωσφορικό. Η περιεκτικότητα νατρίου των 5 mg ανά 100 g, όμως, είναι χαμηλή, όπως και οι περιεκτικότητες του ασβεστίου και του σιδήρου. Τα φρέσκα μανιτάρια περιέχουν περίπου 93% νερό, όμως η περιεκτικότητα του νερού εξαρτάται από την ηλικία του καρποφόρου σώματος, με τα νεαρά γενικά να περιέχουν λιγότερο νερό.
Βιταμίνες
Τα μανιτάρια περιέχουν σημαντικές ποσότητες βιταμίνης C (περίπου 2.1 mg ανά 100 g φρέσκων μανιταριών), επίσης μερικές βιταμίνες Β (συμπεριλαμβανομένου Β1, Β2, Β6 και αμιδίου νιασίνης, Β3). Τα μανιτάρια είναι επίσης πλούσια σε νικοτινοαμίδιο (5.2 mg ανά 100 g μανιταριών).
References
- Höfer J (2017) Natural experiments: taking the lab outdoors. Science in School 42: 42-48.
Resources
- Διαβάστε ένα ερευνητικό άρθρο για στάση των μαθητών απέναντι στην επιστήμη και τη φύση. Δείτε: Krischer D, Spitzer P & Gröger M (2016) ‘Chemistry is toxic, nature is idyllic’ – investigation of pupils’ attitudes. The Journal of Health, Environment, & Education 8: 7-13. doi: 10.18455/08002
- Για περισσότερες πληροφορίες σχετικά με τη χημεία που εμπλέκεται στα διάφορα πειράματα, δείτε τις ακόλουθες πηγές:
- Biuret test
- Ninhydrin test
- Vitamin C: Teepoo S (2012) A new simple and rapid colorimetric screening test for semi-qualitative analysis of vitamin C in fruit juices based on Prussian blue. Journal of Applied Sciences 12: 568-574. doi: 10.3923/ jas.2012.568.574
- Phosphate test
- Silver chloride
Review
Οι συγγραφείς έχουν αναγνωρίσει μια μεγάλη πρόκληση στις φυσικές επιστήμες: οι μαθητές και ένα μεγάλο μέρος του ευρύτερου κοινού, δεν καταλαβαίνουν ότι τα πάντα γύρω τους – ακόμα και το φαγητό τους – αποτελείται από χημικά.
Τα πειράματα που περιγράφονται σε αυτό το άρθρο, κατάλληλα για τελειόφοιτους μαθητές που δουλεύουν σε εργαστήριο, είναι ένας εξαιρετικός τρόπος για να διαπιστώσουν πως η τροφή είναι εκ φύσεως χημική, χρησιμοποιώντας μανιτάρια ως παράδειγμα. Η άσκηση συνδέει επίσης πλευρές της χημείας με τη βιολογία και μπορεί να ευρύνει την εμπειρία των μαθητών με πρακτική εργασία που δεν καλύπτεται συνήθως στο πρόγραμμα σπουδών των φυσικών επιστημών.
Tim Harrison, School Teacher Fellow, University of Bristol, Ηνωμένο Βασίλειο





