Supporting materials
Mais detalhes sobre a análise SANS (Word)
Mais detalhes sobre a análise SANS (Pdf)
Download
Download this article as a PDF

Traduzido por Duarte Nuno Januário. O aumento da poluição resultante da crescente utilização de detergentes e outros surfatantes é uma preocupação. Uma resposta a este problema: surfatantes que podem ser recolhidos e reutilizados simplesmente ligando e desligando um campo magnético.


Estima-se que cada pessoa na EU utilize cerca de 10 kg de detergentes anualmente. Isto inclui não apenas as barras de sabão, champô, pasta de dentes, detergentes em pó e produtos de limpeza domésticos que nos são familiares, mas também os compostos do mesmo tipo que são encontrados em combustíveis, produtos farmacêuticos e até em comidas ou cerveja. Na indústria são utilizadas grandes quantidades de detergentes, por exemplo, em lavandarias, na preparação de tecidos e couro para a tinturaria, nas lavagens de automóveis e na limpeza e desinfecção hospitalar.
Uma vez cumprida a sua função de limpeza, os resíduos são simplesmente despejados no sistema de esgoto e eventualmente libertados no meio ambiente. Imagine se em vez disso os resíduos pudessem ser recuperados. Este artigo descreve algumas das mais recentes investigações no domínio dos detergentes recicláveis e como podem ser estudados utilizando métodos avançados.
Os surfatantes são compostos que diminuem a tensão superficial dos líquidos, tornando-os adequados para um maior número de aplicações – como agentes emulsionantes, espumantes, molhantes e dispersantes, por exemplo. Os surfatantes que são usados na limpeza são conhecidos como detergentes. O mais simples e mais antigo de todos é o sabão, que já era utilizado na Babilónia há quase 5000 anos atrás; de facto, o fabrico de sabão é uma das mais antigas indústrias químicas.
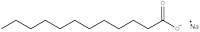
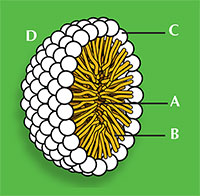
O dodecanoato de sódio (figura 1) demonstra a estrutura geral de todos os surfatantes: uma parte da molécula é hidrofílica, o que significa que será solúvel em água devido à sua “cabeça” carregada, e o resto da molécula é uma “cauda” gordurosa hidrofóbica. A habilidade do detergente para dissolver a água deve-se a um balanço de forças intermoleculares. A cabeça é um ião carboxilato carregado negativamente, capaz de estabelecer ligações de hidrogénio com a água, enquanto a cauda hidrofóbica não se liga ao hidrogénio porque é uma longa cadeia alquílica, que não conta com elementos electronegativos. Isto explica porque os surfatantes formam agregados conhecidos por micelas (figura 2), que são essenciais para a acção de detergentes.

As duas extremidades do detergente também se comportam de forma diferente, por exemplo, com manchas de gordura. As caudas hidrofóbicas interagem com a gordura, enquanto as cabeças hidrofílicas atraem moléculas de água através de ligações de hidrogénio. Após alguma agitação, a gordura liberta-se do material a que se encontrava ligada, ficando confinada às gotas de detergente; as superfícies das gotas consistem em cabeças hidrofílicas solúveis em água. A gordura é assim removida do material e confinada na água pelas micelas (figura 2).
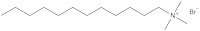
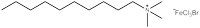
Um grupo de investigadores da Universidade de Bristol, Reino Unido – incluindo dois dos autores deste artigo – encontra-se neste momento a trabalhar num novo tipo de surfatantes: os surfatantes magnéticos, que respondem à acção de campos magnéticos devido à presença de átomos de ferro nas suas cabeças (figuras 3 e 4). Estes surfatantes podem ter aplicações ambientais e médicas.
Como foram desenvolvidos estes surfatantes magnéticos? E como se prova que se produziu realmente um surfatante magnético?
Para começar, os investigadores de Bristol utilizaram um surfatante conhecido e substituíram o grupo bromo por um grupo contendo ferro (figura 3). Depois demonstraram que o composto ainda atuava como um surfatante: era capaz de diminuir a tensão superficial de líquidos, permitia-lhes espumar. Depois, o grupo demonstrou que o ferro na cabeça hidrofílica lhe havia conferido a desejada actividade magnética.
Para entender realmente o que se estava a passar, contudo, os investigadores precisavam de observar com mais atenção o seu composto. Por exemplo, embora a sua capacidade para diminuir a tensão superficial fosse um indicador de que haveria formação de micelas, tal não era uma prova conclusiva. Para testar isto, os investigadores utilizaram uma técnica especial super-sensível designada dispersão de neutrões de pequeno ângulo (SANS – small angle neutron scattering).

A SANS é uma técnica excelente para investigar estruturas entre 0.1 e 100 nm de tamanho. Perfeita, então, para encontrar e caracterizar micelas de surfatante e gotículas de emulsões, que têm tipicamente entre 2 e 10 nm de diâmetro. A SANS é também muito utilizada para investigar materiais macios (ex.: polímeros, colóides e cristais líquidos), moléculas biológicas (ex.: DNA e proteínas em solução) e matéria condensada (ex: agregados de átomos em ligas metálicas e redes de linhas de fluxo em supra-condutores).
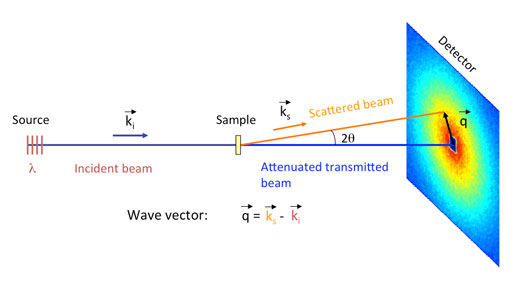
Numa experiência SANS, aponta-se um feixe de neutrões de grande intensidade para a amostra com interesse de estudo (figura 5); este feixe pode ser visto como uma corrente de partículas livres viajando na mesma direção e com a mesma velocidade. Os neutrões livres do feixe interagem com os núcleos dos átomos da amostra, ocorrendo dispersão do feixe. A dispersão dos neutrões do feixe é então registada por um detetor sensível à sua posição. Os dados resultantes – a intensidade dos neutrões dispersados pelas diferentes áreas da amostra – são usados em modelos matemáticos que permitem determinar a forma, o tamanho e a carga dos objetos dispersantes na amostra. Para uma explicação mais detalhada da análise SANS, pode descarregar Material de apoio do site Science in Schoolw1.
Para a sua análise SANS, o grupo de Bristol formou equipa com cientistas do Instituto Laue-Langevin (ILL; ver caixa) em Grenoble, França. Apesar de no novo composto já terem sido observadas propriedades surfatantes, como por exemplo a redução da tensão superficial, os resultados da SANS forneceram as primeiras provas conclusivas de que ocorre também formação de micelas.
Para além disso, os cientistas mostraram que as micelas formadas eram pequenas, esféricas e não carregadas. Isto é importante porque o comportamento de um surfatante, bem como as suas aplicações, são afetados pelas características das micelas e das gotículas na emulsão que forma com diferentes líquidos. Com esta informação, os cientistas conseguem prever – e no futuro investigar – o comportamento do seu surfatante em condições diversas.
Utilizando a SANS, a equipa foi também capaz de testar se em solução as partículas de ferro se dissociam do surfatante, resultando efetivamente numa mistura de surfatantes não magnéticos e partículas magnéticas dissolvidas, ou se os dois componentes permanecem ligados, formando micelas genuinamente magnéticas. Os resultados sugerem que os compostos de ferro se encontravam firmemente integrados nas micelas. Isto abriu a possibilidade de criar emulsões magnéticas com possíveis aplicações médicas (ver em baixo).

Os surfatantes magnéticos podem parecer uma ideia estranha, no entanto têm algumas aplicações muito práticas. Por exemplo, muitos surfatantes não são biodegradáveis. Se fossem usados surfatantes magnéticos, estes poderiam ser recuperados das águas residuais, utilizando campos magnéticos, e reciclados, resultando numa diminuição dos níveis de detergentes no ambiente.

Para além disso, atualmente, quando ocorre um derrame petrolífero no mar, são usados surfatantes para reduzir o petróleo a gotículas em emulsão, para que possam difundir-se no oceano, permanecendo assim o seu potencial enquanto agente poluente. Se fossem usados surfatantes magnéticos, as emulsões resultantes poderiam ser recolhidas, removendo-se o petróleo e os surfatantes da água.
Os surfatantes magnéticos podem até ter aplicações médicas. A administração localizada de fármacos tem como objetivo o seu fornecimento apenas às células específicas onde são necessários, prevenindo o desperdício de compostos farmacêuticos valiosos e minimizando efeitos secundários. A Figura 6 mostra como as gotículas da emulsão (coradas de azul), formadas a partir de surfatantes magnéticos, podem ser manipuladas com um pequeno íman, de forma suficientemente eficiente para contrariar a corrente sanguínea no interior do organismo. Estas emulsões poderiam conter medicação da mesma forma que as que já são utilizadas atualmente, podendo no entanto ser conduzidas diretamente para a localização correta utilizando um íman.

Os surfatantes magnéticos não são o único novo tipo de surfatantes que estão a ser desenvolvidos em Bristol. A equipa de investigação encontra-se também a estudar surfatantes que podem ser ativados ou desativados através de variações de luz, pH, temperatura, pressão ou concentração de dióxido de carbono. O desafio atual é descobrir como sintetizar estes compostos em grande escala, de forma a torná-los baratos e eficientes.

As experiências utilizando SANS requerem feixes intensos de neutrões, que apenas podem ser produzidos em grandes estruturas. Na Europa, são produzidos em laboratórios apoiados e geridos através de colaborações intergovernamentais, como o ISISw2, no Reino Unido, e o Instituto Laue-Langevin (ILL)w3, em França.

O ILL é um centro de pesquisa internacional que opera a fonte estável de neutrões mais intensa do mundo. Todos os anos, são realizadas mais de 800 experiências por cerca de 2000 cientistas provenientes de todo o mundo. A pesquisa foca-se em diversos campos da ciência: física da matéria condensada, química, biologia, física nuclear e ciência dos materiais.
O ILL é um membro do EIROforumw4, que publica a Science in School.
Brown P et al. (2012b) Magnetic control over liquid surface properties with responsive surfactants. Angewandte Chemie 51: 2414-2416. doi: 10.1002/anie.201108010
Kaiser A, Rau M (2010) LeSa21: primary-school science activities. Science in School 16: 45-49.
Mais detalhes sobre a análise SANS (Word)
Mais detalhes sobre a análise SANS (Pdf)
Download this article as a PDF