Co to jest chemiluminescencja? Understand article
Tłumaczenie Jadwiga Schreiber. Świecące meduzy, migotające świetliki czy fluorescencyjne pałeczki na imprezach klubowych; Emma Welsh wprowadzi nas w piękny i tajemniczy świat chemiluminescencji.

Zdjęcie dzięki uprzejmości Erik
Solheim; źródło zdjęcia:
Wikimedia Commons
Świetliki, meduzy i fluorescencyjne pałeczki – te pierwsze latają, drugie żyją w oceanie a te ostatnie urozmaicają imprezę klubową. Co mają wspólnego? Łączą je intrygujące reakcje chemiczne, w wyniku, których produkowane jest światło.
Chemiluiminescencja to zjawisko emisji światła (fal świetlnych), wytworzonego w wyniku specyficznych reakcji chemicznych. Dwie reagujące ze sobą substancje chemiczne tworzą wzbudzony (wysokoenergetyczny) produkt przejściowy, który powracając do podstawowego stanu energetycznego rozpada się na produkty oraz uwalnia energię w formie fotonów świetlnych (zobacz Rysunek 1; pogrubione wyrazy wyjaśnione są w słowniczku)
A + B -> AB* -> Produkty + Światło
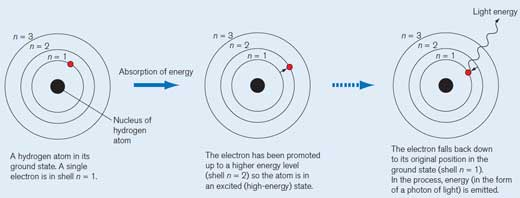
Atom wodoru w stanie podstawowym. Elektron znajduje się w pierwszej powłoce, n=1. Każda powłoka posiada swój stan energetyczny.
Jeśli atom wodoru zaabsorbuje kwant (określoną ilość) energii, przechodzi on na wyższy poziom energetyczny (elektronowa powłoka 2, n=2) i wchodzi w stan wzbudzony (wysokoenergetyczny). Cząsteczkę w stanie wzbudzonym oznacza się gwiazdką (*).
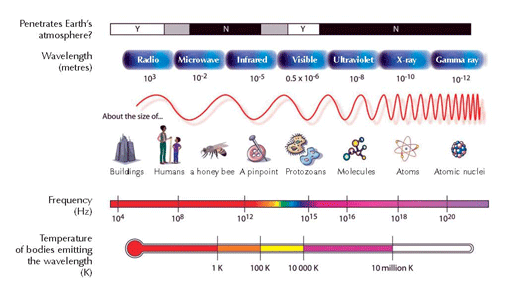
Po krótkim czasie wzbudzony elektron wraca do swojego podstawowego stanu energii (powłoka elektronowa 1, n=1) . W procesie tym uwolniony zostaje kwant energii (foton) w formie promieniowania elektromagnetycznego. Długość fali tego promieniowania zależy od ilości uwolnionej energii. Jeśli długość tej fali znajduje się w zakresie światła widzialnego to energia ta uwolniona zostanie, jako światło o specyficznym kolorze. Długość fali decyduje o barwie światła (spójrz na Rysunek 2)
Zdjęcie dzięki uprzejmości Chemistry Review
Chemiluminescent reactions do not usually release much heat, because energy is released as light instead. Luminol produces a light when it reacts with an oxidising agent; the chemistry of this reaction is shown in ramce 1.
Ramce 1: Luminol, świecący w ciemności związek chemiczny
Uwolnienie fotonu światła z cząsteczki luminolu jest dość złożonym, wieloetapowym procesem. W roztworze alkalicznym luminol występuje w formie anionu, z ujemnym ładunkiem -2) i jest w równowadze jonowej. Anion ten może występować w dwóch formach (tautomerach), gdzie 2 ujemne ładunki mogą zostać zdelokalizowane albo na atom tlenu (forma enolowa) albo na atom azotu (forma ketolowa; zobacz na Rysunek 3).
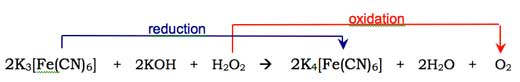
Tlen cząsteczkowy (O2) reaguje z enolową formą anionu luminolu, utleniając go do cyklicznego nadtlenku. Wymagany do tej reakcji tlen powstaje w procesie reakcji redoks (w której jednoczenie występuje redukcja i utlenianie) z udziałem nadtlenku wodoru (H2O2), wodorotlenku potasu i (na przykład) heksacyjanożelazianu (III) potasu (K3[Fe(CN)6], nazywanego również żelazicyjankiem potasu). W reakcji tej jon heksacyjanożelazianu(III) ([Fe(CN)6]3-) redukowany jest do jonu heksacyjanożelazianu(II) ([Fe(CN)6]4-, dając żelazocyjanek potasu, K4[Fe(CN)6]), a dwa atomy tlenu z cząsteczki nadtlenku wodoru zostają utlenione ze stopnia utlenienia -1 do 0:
Powstały w tej reakcji cykliczny nadtlenek rozkłada się na kwas 3-nitroftalowy (kwas 3-amino-1,2-bensodikarboksylowy) w stanie wzbudzonym oraz na cząsteczkę azotu (N2) – zobacz Rysunek 3. Reakcja ta jest faworyzowana, gdyż cząsteczka cyklicznego nadtlenku jest niestabilna i słabe wiązania chemiczne ulegają zerwaniu. Dodatkowo reakcja ta zwiększa entropię (nieuporządkowanie) poprzez uwolnienie cząsteczki gazu. Kiedy „wzbudzony” kwas 3-nitroftalowy spadnie (przejdzie) w podstawowy stan energetyczny, uwolniony zostanie foton światła niebieskiego.
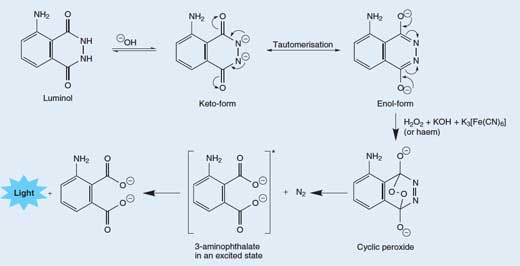
Tautomery to cząsteczki o tym samym wzorze chemicznym, ale odmiennym układzie (połączeniu) atomów czy wiązań chemicznych. Tautomery przechodzą jedne w drugie na skutek spontanicznej reakcji wewnątrzcząsteczkowej; zaokrąglone strzałki przedstawiają ruch elektronów podczas zamiany jednej formy w drugą. Kliknij na obrazek aby powiększyć
Zdjęcie dzięki uprzejmości Chemistry Review
Chemiluminescencja w medycynie sądowej
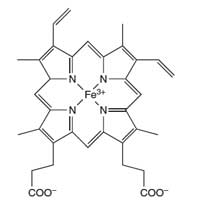
hemoglobinie
Atom żelaza (Fe) znajdujący
się w centrum porfiryny
katalizuje reakcję
przekształcenia luminolu
Zdjęcie dzięki uprzejmości
Chemistry Review
Specjaliści medycyny sądowej używają luminolu do wykrywania krwi w miejscu przestępstwa. Mieszanka luminolu w roztworze nadtlenku wodoru rozpylana jest nad miejscem, gdzie specjaliści podejrzewają znaleźć krew. Żelazo znajdujące się w układzie hemu w hemoglobinie (zobacz Rysunek 4) krwi zachowuje się jak katalizator w reakcji opisanej w ramce 1. Dlatego jeśli w danym pomieszczeniu rzeczywiście znajduje się krew i żelazo z tej krwi wejdzie w rekcję z luminolem, po zgaszeniu światła zauważalne będzie niebieskie światło, świecące około 30 sekund. Śledczy może sfotografować ten sygnał i użyć takie zdjęcie, jako dowód w sądzie (zobacz Wallace-Müller, 2011, w artykule „Praktyczna lekcja medycyny sądowej”).
Ponieważ żelazo działa tu jako katalizator wystarczające są jego śladowe ilości i dlatego nawet bardzo mała ilość krwi wywoła pozytywną reakcję. Oznacza to, że krew może być zidentyfikowana nawet, jeśli nie widać jej gołym okiem.

miejscu przestępstwa
Zdjęcie dzięki uprzejmości How
Stuff Works
Jedną z wad luminolu jest fakt, że reakcja jego przekształcenia może być katalizowana również przez inne substancje możliwie obecne w miejscu przestępstwa np. stopy miedzi, niektóre środki czyszczące (np. wybielacz) czy nawet chrzan. Teoretycznie każdy przestępca mógłby zatrzeć za sobą ślady krwi wybielaczem, ale wybielacz pozostawiłby plamy np. na dywanie, co bardzo szybko zwróciłoby uwagę śledczych. Również mocz zawiera wystarczającą ilości krwi by skatalizować reakcję luminolu. Innym „minusem” jest fakt, że po przeprowadzeniu testu z luminolem na danej powierzchni inne testy mogą już być niewykonalne. Mimo swych wad luminol jest często używany w śledztwach kryminalnych.
W klubie nocnym
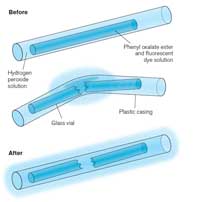
fluorescencyjne pałeczki
produkują światło?. Kliknij na
obrazek aby powiększyć
Zdjęcie dzięki uprzejmości
Chemistry Review
Jeśli zegniesz pałeczkę fluorescencyjną zacznie ona świecić – światło to produkowane jest w procesie chemiluminescencji (zobacz Rysunek 5). Świecące pałeczki zawierają w ich wnętrzu plastikową rurkę wypełnioną mieszanką szczawianu difenolu z barwnikiem (nadającym kolor światłu). Wewnątrz tej plastikowej rurki znajduje się następne rurka wypełniona nadtlenkiem wodoru. Jeśli pałeczka zostanie zgięta, wewnętrzna rurka pęka i uwalnia nadtlenek wodoru do roztworu szczawianu rozpoczynając reakcję chemiczną, w której powstaje światło (zobacz Ramka 2). Kolor powstającego światło zależy od koloru barwnika w mieszaninie (zobacz Ramka 3).
Reakcje chemiluminescencyjne, jak ta we fluorescencyjnych pałeczkach, zależą od temperatury. Reakcja ta przyspiesza, gdy temperatura wzrośnie – gdybyś zgiął taką pałeczkę w ciepłej wodzie wywołałoby to fantastyczny efekt świetlny, trwający jednak dużo krócej niż w temperaturze pokojowej. Odwrotnie jest w niskiej temperaturze, spowolniającej tą reakcję, – jeśli schowałbyś taką pałeczkę do zamrażalki na kilka godzin, po wyjęciu i ociepleniu świeciłaby ona dużo dłużej niż zwykle. W zimnym otoczeniu reakcja ta jest bardzo spowolniona, choć niezahamowana, i efekt świetlny jest prawie niewidoczny.
Ramka 2: Chemia fluorescencyjnych pałeczek
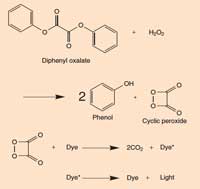
powiększyć
Zdjęcie dzięki uprzejmości
Chemistry Review
Kiedy difenyl szczawianu wejdzie w reakcję z nadtlenkiem wodoru (H2O2),zostaje on utleniony i powstaje fenol oraz cykliczny nadtlenek. Nadtlenek reaguje z cząsteczką barwnika i w ten sposób powstają dwie cząsteczki dwutlenku węgla (CO2) oraz wzbudzona cząsteczka barwnika ze elektronem znajdującym się w wyższym stanie energetycznym. Kiedy cząsteczka ta przechodzi z powrotem do stanu podstawowego, uwalnia ona foton światła. Reakcja ta jest zależna od pH. W silnie zasadowym środowisku produkowane (uwalniane) światło jest dużo jaśniejsze.
Informacje o bezpieczeństwie
Fenol jest toksyczny, gdy fluorescencyjna pałeczka okaże się być nieszczelna, unikaj kontaktu substancji chemicznych z twoim ciałem, jeśli jednak dojdzie do kontaktu ze skórą, od razu zmyj dokładnie to miejsce mydłem; zobacz również ogólne zasady bezpieczeństwa w stronie Science in School .
Ramka 3: Dlaczego pałeczki fluorescencyjne mogą mieć różne kolory?
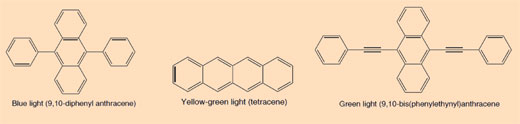
Barwniki znajdujące się w pałeczkach fluorescencyjnych są sprzężonymi związkami aromatycznymi (areny). Stopień sprężenia odzwierciedla się w różnych kolorach emitowanego światła. Foton światła uwalniany jest, kiedy elektron spada z wyższego (wzbudzonego) poziomu energii do stanu podstawowego.
Żyjąca fluorescencja

świętojański
Zdjęcie dzięki uprzejmości
Terry Priest; źródło zdjęcia:
Flickr
Czy zdarzyło Ci się kiedyś spacerować po plaży i zauważyć w wodzie coś świecącego? Albo spędzając lato na wsi zauważyłeś latające robaczki świętojańskie? To żywe przykłady bioluminescencji. Ponad 90% zwierząt żyjących głęboko w oceanie posiada zdolność produkcji światła, która pomaga im w wielu dziedzinach życia. Światło przyciąga potencjalne ofiary (pokarm) czy partnerów seksualnych lub może być formą kamuflażu. Niektóre bakterie komunikują za pomocą sygnałów świetlnych.
Termin „robaczek świętojański” odnosi się do larw niektórych owadów, np. z rodziny świetlikowatych; niektóre gatunki produkują światło by odstraszyć drapieżników, podczas gdy inne przyciągają swoją zdobycz lśniącym światełkiem. Niektóre kałamarnice czy skorupiaki potrafią wydzielić „chmurę” bioluminescencyjnej cieczy by zmylić drapieżnika i uciec. Organizmy żyjące głęboko w oceanach produkują zazwyczaj niebieskie i zielone światło gdyż barwy te są najlepiej widoczne w morskiej wodzie. Światło niebieskie ma krótszą długość fali niż czerwone i dlatego jest w mniejszym stopniu absorbowane przez cząsteczki w wodzie.
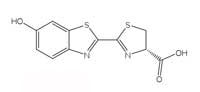
lucyferyny świetlika. Kliknij
na ilustrację, aby ją
powiększyć. Kliknij na
obrazek aby powiększyć
Zdjęcie dzięki uprzejmości
Chemistry Review (structure)
Reakcje bioluminescencyjne używają ATP (adenozynotrifosforan), jako źródło energii. Choć struktura produkujących światło cząsteczek różni się u różnych gatunków, posiadają one wspólną nazwę lucyferyn. Lucyferyna świetlika przedstawiona jest po lewej stronie na rysunku 6. Kiedy świetlik „świeci” lucyferyna ulega utlenieniu i wchodzi w wzbudzony stan energetyczny, w momencie, gdy powraca ona do stanu podstawowego uwolniony zostaje foton światła podobnie jak w chemiluminescencyjnej reakcji luminolu opisanej w ramce 1. W reakcji tej jednak to nie nadtlenek wodoru i heksacyjanożelazianu (III) potasu utleniają lucyferynę a cząsteczkowy tlen i enzym zwany lucyferazą (jest to wspólna nazwa dla różnych gatunków – lucyferazy różnią się między gatunkami).

odkryta została w meduzie
Aequorea victoria
Zdjęcie dzięki uprzejmości
Typoform / the Royal Swedish
Academy of Sciences (RSAS)
Lucyferaza
Lucyferyna + O2 → Utleniona lucyferyna + Światło
Liczne badania naukowe przeprowadzone zostały również nad aequoriną, białkiem znalezionym w meduzie. W obecności wapnia białko to produkuje niebieskie światło fluorescencyjne (zobacz Shaw, 2002, oraz Furtado, 2009) i dzięki temu używane jest w biologii molekularnej do pomiaru poziomu wapnia w żywych komórkach. Naukowcy wciąż mają nowe pomysły przyszłego zastosowania bioluminescencji np. samo zaświecające się oświetlenie choinkowe. Czy Ty też miałbyś jakiś ciekawy pomysł na wykorzystanie tego naturalnego fenomenu?
Słowniczek
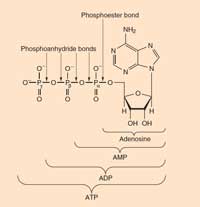
powiększyć
Zdjęcie dzięki uprzejmości
Chemistry Review
Anion: atom (lub cząsteczka) o negatywnym ładunku.
ATP: adenozynotrifosforan występuje we wszystkich znanych formach życia. Jest on głównym źródłem energii komórek. ATP powstaje z ADP (adenozynodifosforan) i fosforanu podczas reakcji egzoergicznych np. podczas utleniania cząsteczki glukozy, i rozkłada się na ADP i fosforan, uwalniając energię i umożliwiając przeprowadzanie reakcji endoergicznych (pochłaniających energię).http://www.scienceinschool.org/node/2378#overlay=node/2378/edit
Bioluminescencja: produkcja światła przez organizmy żywe. Bioluminescencja może powstać poprzez absorbcję światła (fluorescencja lub fosforescencja, np. u wielu ryb głęboko morskich) lub w wyniku reakcji chemicznej (chemiluminescenja, np. świetlik świętojański).
Katalizator: Substancja chemiczna przyspieszająca reakcję, ale nieulegające trwałej przemianie chemicznej w wyniku tej reakcji (np. katalizatora nie ubywa w czasie reakcji). Kataliza przyspiesza reakcje poprzez obniżenie energii potrzebnej do jej przeprowadzania.
Cheminuminescencja: rodzaj luminescencji, w której elektrony wchodzą w stan wzbudzony podczas reakcji chemicznej, np. tak jak w reakcji luminolu opisanej w ramce 1.
System sprzężony: system sprzężony w związku chemicznym oznacza występowanie podwójnych wiązania chemicznych. W systemie sprzężonym atomy połączone są wiązaniami kowalencyjnymi i wiązania te są na przemian pojedyncze i wielokrotne (najczęściej podwójne, ale potrójne są również możliwe). Alkeny są płaskie, związki sprzężone muszą być trójwymiarowe by umożliwić delokalizację elektronów z orbitali atomowych w obrębie tego związku. Przykładami związków sprzężonych są cząsteczki barwników przedstawione w ramce 3.
Wiązania kowalencyjne: wiązania pomiędzy dwoma atomami, które współdzielą parę elektronów.

zdelokalizowane w systemie
sprzężonym.
Ilustracja za uprzejmością
Chemistry Review
Delokalizacja: związki zawierające wiązania sprzężone posiadają wolne elektrony poruszające się swobodnie w układzie sprzężonym tej cząsteczki. Te wolne elektrony nazywane są zdelokalizowanymi np. jak w pierścieniu benzenu jest ich 6 i determinują one taką samą długość wiązań między atomami węgla.
Fluorescencja: rodzaj luminescencji, w której elektrony wzbudzone zostają za pomocą światła, np. jak w maszynach sprawdzających autentyczność banknotów.
Luminescencja: proces produkcji światła, zazwyczaj w niskich temperaturach, w wyniku reakcji chemicznej lub dzięki energii elektrycznej. Żarzenie, natomiast, jest produkją światła w bardzo wysokich temperaturach.
Fosforescencja: proces podobny to fluorescencji, ale produkcja światła trwa dłużej (pomiędzy sekundami a nawet godzinami), przykładem są fluorescencyjne pałeczki.
Podziękowania
Oryginalna wersja tego artykułu opublikowana została w Chemistry Review. Artykuł ten powstał za uprzejmością wydawcy, Philipa Allana. Aby uzyskać abonament Chemistry Review, czasopisma przeznaczonego dla uczniów szczególnie zainteresowanych chemią, zobacz: www.philipallan.co.uk/chemistryreview
References
- Furtado S (2009) Pomaluje Twój świat na zielono: GFP. Science in School 12: 19-23.
- Shaw A (2002) Genetic chess by the light of a jellyfish. Chemistry Review 12(1): 2-5
- Wallace-Müller K (2011) The DNA detective game. Science in School 19: 30-35.
Resources
- Opisy innych doświadczeń z luminolem można znaleźć na stronie internetowej Declana Fleminga; więcej informacji na temat chemiluminescencji i luminolu można znaleźć na stronie www.chm.bris.ac.uk/webprojects2002/fleming/experimental.htm
- Aby dowiedzieć się więcej na temat różnych rodzajów światła stosowanego w chemii zobacz:
-
Douglas P, Garley M (2010) Chemistry and light. Science in School 14: 63-68.
-
Review
Artykuł ten ma na celu zachęcić uczniów do głębszej analizy procesów reakcji chemicznych. Nawet, jeśli nie interesuje ich jak i dlaczego fluorescencyjne pałeczki świecą w ciemności, może zaciekawią ich procesy, dzięki którym świetlik czy meduza produkują światło, lub jak zidentyfikować krew w miejscu przestępstwa. Artykuł ten może być wykorzystany, jako wprowadzenie do tematu reakcji chemicznych lub jako ciekawe przykłady reakcji redoks jak również do ilustracji poziomów energii w powłokach atomu.
Artykuł ten można wykorzystać w różny sposób dla różnych grup wiekowych uczniów. Dla uczniów w wieku 14-15 lat, może on być wykorzystany na lekcji chemii (struktura atomu, ruch elektronów w powłokach atomowych, wprowadzenie do tematu reakcji chemicznych) lub biologii (bioluminescencja). Nauczyciele powinni jednak uprościć niektóre informacje i być może ominąć niektóre detale. Dla uczniów w wieku 16-18 lat artykuł ten będzie pomocny na lekcji chemii (reakcje redoks, kataliza, wpływ temperatury czy pH na szybkość reakcji chemicznej, wiązania kowalencyjne), fizyki (widmo spektroskopowe, fotony) czy genetyki (inżynieria genetyczna). Poniżej znajdują się przykładowe pytaniami sprawdzające zrozumienie tematu.
- Co to jest chemiluminescencja?
- Jak specjaliści medycyny sądowej mogą zastosować chemiluminescencję w śledztwie?
- Wyjaśnij biologiczne funkcje bioluminescencji.
- Dlaczego powinniśmy schować pałeczkę fluorescencyjną do zamrażalki?
- Jak zrobić samo zaświecającą się choinkę bożonarodzeniową?
Ana Gil, Hiszpania