La investigación de la acción de la ureasa Teach article
Traducido por María Jesús Tornero y Gabriel Pinto (Universidad Politécnica de Madrid). Anna Lorenc del proyecto Volvox explica la importancia de la enzima ureasa y presenta un protocolo para demostrar la actividad de la ureasa en clase.
Las enzimas desempeñan un papel esencial en el metabolismo de todos los organismos. Catalizan y controlan la mayoría de las reacciones bioquímicas en nuestro cuerpo- desde la replicación de la información genética (ADN) hasta la digestión. La actividad de la enzima, sin embargo, no siempre es fácil de visualizar. Aquí se presenta una práctica sencilla y económica para ayudar a enseñar el tema de la actividad de la enzima en el aula. Todos los materiales necesarios están disponibles y son seguros.
En esta investigación, la enzima ureasa de la soja (Glycine max) descompone la urea en amoníaco y el dióxido de carbono:
CO(NH2)2 + H2O → 2 NH3 + CO2
La disolución de amoníaco (NH3) tiene un pH alto que puede ser detectado mediante un simple indicador de pH, como el que se obtiene de lombarda. El amoníaco producido por la reacción también puede ser detectado por el olor.
Como la ureasa es producida por una amplia gama de diferentes organismos, esta actividad práctica se puede utilizar en las clases en:
- El ciclo de nitrógeno
- La influencia de los organismos en su medio ambiente
- La adaptación de los animales a diferentes dietas.
Antecedentes
¿Qué es la urea?
Cada organismo descompone los ácidos nucleicos y proteínas, generando residuos nitrogenados porque los ácidos nucleicos y proteínas contienen nitrógeno. Mamíferos, anfibios y algunos invertebrados excretan residuos nitrogenados como la urea, que se produce en el hígado. La urea es un compuesto especialmente bueno para la eliminación de nitrógeno debido a que es soluble en agua y menos tóxico que el amoníaco – los productos de excreción de los peces, por ejemplo. La orina humana contiene 2% de urea.
La urea fue también el primer compuesto orgánico sintetizado. En 1828, Friedrich Wöhler sintetizó urea a partir de compuestos inorgánicos (cianato de plomo y de hidróxido amónico). Fue un logro histórico: hasta entonces sólo los organismos vivos se creía que estaban en condiciones de producir compuestos orgánicos, y estos compuestos se pensaba que eran especiales y requerían una “fuerza vital” para hacerlos. Wöhler superó la brecha entre el mundo vivo y el inerte. No recibió un Premio Nobel por su descubrimiento debido a que dicha distinción no existía en ese momento. Hoy en día, la urea se sintetiza en grandes cantidades: se utiliza para hacer plásticos y como abono nitrogenado.
¿Qué es la ureasa?
La ureasa cataliza la hidrólisis de la urea a dióxido de carbono y amoniaco. Se encuentra principalmente en semillas, microorganismos e invertebrados. En las plantas, la ureasa es un hexámero –consiste en seis cadenas idénticas- y se encuentra en el citoplasma. En bacteria, consiste en dos o tres subunidades diferentes. Para su activación, la ureasa necesita unir dos iones de níquel por subunidad.
¿Cómo se hizo famosa la ureasa?
La ureasa de judías tipo Jack (Canavalia ensiformis) fue la primera enzima purificada y cristalizada, un logro de James B. Sumner en 1926, en un momento en que la mayoría de los científicos creían que era imposible cristalizar enzimas. Esto le valió a Sumner el Premio Nobel de Química en 1946. Hoy en día, la cristalización de proteínas ayuda a los científicos a descubrir su estructura y determinar cómo funcionan. Este conocimiento permite el diseño de las sustancias que interfieren en la acción de la enzima, tales como los medicamentos para la lucha contra el SIDA que inhiben la acción de las enzimas del VIH o de la evolución reciente hacia un posible tratamiento de la rabia (Ainsworth, 2008).
¿Por qué hay ureasa en las semillas de soja?
El papel de la ureasa en semillas de soja no es del todo claro, aunque es posible especular sobre ello. Las hojas de soja también contienen ureasa, pero en este caso, la enzima es mil veces menos activa que en las semillas. Se sabe que la enzima de la hoja ayuda a reciclar el nitrógeno de las proteínas (las proteínas se descomponen para dar urea). En las semillas, la ureasa hace lo mismo cuando los granos germinan. El amoníaco resultante de la reacción también puede proteger las células de la planta de patógenos – parece ser que la enzima de la planta es en sí misma es un insecticida.
¿Dónde más se puede encontrar la ureasa?

Imagen cortesía de iStockphoto
Muchas especies de bacterias producen ureasa, incluyendo a la Helicobacter pylori, la bacteria responsable de la úlcera de estómago. De esta manera, el H. pylori aumenta el pH del jugo gástrico de alrededor de pH 3 a un pH 7, el óptimo para su crecimiento. Una prueba disponible comercialmente para controlar el H. pylori detecta la presencia de ureasa en el aliento, y se utiliza como una herramienta para el diagnóstico de úlcera de estómago.
Los rumiantes (como vacas y ovejas) tienen las bacterias para digerir la celulosa en su rumen – el primer compartimiento de sus estómagos – para ayudarles a digerir su dieta vegetal. Los rumiantes excretan urea en esta parte del estómago, siendo la urea una excelente fuente de nitrógeno para el crecimiento bacteriano. Para asumir el nitrógeno, las bacterias secretan ureasa para descomponer la urea. Finalmente, los animales digieren la masa bacteriana.
¿Es la ureasa de la soja perjudicial para los humanos?
La ureasa no es perjudicial. Sin embargo, los granos de soja en crudo contienen otros compuestos que son poco saludables. Por ejemplo, hay un inhibidor de proteína de soja en crudo que impide que la enzima digestiva tripsina trabaje y hace los granos de soja en crudo no comestibles. La presencia del inhibidor no es fácil de detectar, pero afortunadamente, tiene un nivel similar de intolerancia al calor que la ureasa – ambos son inactivadas por el calor. Por lo tanto, para asegurarse de que el inhibidor está inactivo, los preparados comerciales de semillas de soja (harina de soja o de los alimentos que contienen soja, tales como témpura y tofu) son probados para ver la actividad de la ureasa- de forma muy parecida a la prueba descrita aquí. Si no hay ninguna actividad de la ureasa detectada, el inhibidor presumiblemente también ha sido inactivado.
La ureasa en el ciclo de nitrógeno
El nitrógeno es un elemento crucial para el crecimiento de las plantas, pero la mayoría de las plantas sólo lo pueden utilizar en forma de amonio o nitrato. Sólo las leguminosas (gracias a las bacterias que viven en simbiosis con ellas) y las cianobacterias pueden utilizar nitrógeno elemental desde el aire.
Muchos animales excretan urea en la orina. Los microorganismos del suelo se alimentan de la orina del animal, produciendo ureasa para transformar la urea en amoníaco, que es entonces fácilmente accesible a las plantas. Esto es parte del ciclo del nitrógeno, el proceso por el cual el nitrógeno de las proteínas y otros compuestos se recicla constantemente.
Guión
Este guión permite a los estudiantes detectar la actividad de una planta enzima en las semillas. Cuando el substrato (urea) está presente, la ureasa lo descompone en dióxido de carbono y amoníaco. Disuelto en agua, el amoníaco aumenta el pH, un efecto visto con el indicador de pH de lombarda. En el experimento, los estudiantes observan que para obtener el producto (amoníaco), un sustrato (urea) y una enzima (ureasa) son necesarios. Observan que la actividad de la enzima aumenta el pH.
Extracto de lombarda – un buen indicador de pH
En este guión, usamos extracto de lombarda como un indicador de pH. Contiene antocianinas. La estructura y el color (en disolución) de estos compuestos son sensibles al pH. A pH 7, la disolución es violeta/azul, y en medio ácido se colorea de rojo. Cuando el pH se eleva por encima de 7 (la disolución es más alcalina), el extracto se pone verde. Estos cambios de color son reversibles – solo basta comprobar lo que sucede cuando se añade ácido cítrico y bicarbonato sódico, uno tras otro.
Materiales y equipos
Para cada alumno o grupo de estudiantes:
- 20 ml de disolución al 10% de abono de urea (un fertilizante sólido de pura urea)
- 5 ml de disolución al 10% de ácido cítrico (o de otra disolución de bajo pH)
- 5 ml de disolución al 10% de bicarbonato de sodio (NaHCO3) (u otra disolución de alto pH)
- 40 ml de indicador de lombarda, preparado como se describe a continuación
- 10 ml de extracto de soja, preparado como se describe a continuación (a partir de 1 g de granos de soja secos)
- 10 ml de agua destilada
- Pipetas Pasteur o una pajita de plástico, para la transferencia de las disoluciones
- 6 tubos de ensayo y una gradilla.
Para preparar el extracto de soja y el indicador de lombarda, son necesarios una licuadora y agua hirviendo, así como papel de filtro de café y un embudo.
Tiempo
El experimento se puede realizar en 30 minutos.
La suspensión de soja y extracto de lombarda puede hacerse por adelantado, o su preparación puede ser demostrada durante la práctica. Esto lleva sólo diez minutos, pero hay que notar que los granos de soja deben ser empapados en agua, por lo menos una hora antes de la práctica.
La reacción entre la ureasa de la soja y la urea también tarda aproximadamente diez minutos.
Preparación
Indicador de lombarda
- Cortar dos grandes hojas de lombarda en tiras y colocarlas en un recipiente resistente al calor, como un vaso de precipitados. Vierta en él 200 ml de agua recién hervida, y remoje las hojas completamente.
- Después de 5 min, decantar el líquido y dejar que se enfríe.
- Tirar las hojas.
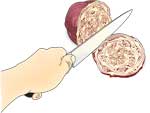
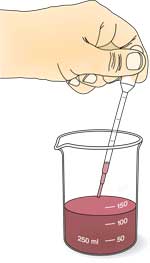

Extracto de soja que contiene ureasa
- Remoje las semillas de soja en agua, por lo menos 1 hora (preferiblemente durante la noche).
- Mezclar la mezcla de semillas de soja en una licuadora de alimentos con 10 ml de agua por gramo de materia seca de soja (el agua para el remojo de los granos de soja puede ser utilizada) hasta que la mezcla esté suave (unos 5 min).
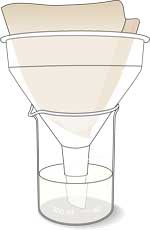
- Filtrar el puré de soja a través de papel de filtro en un embudo.
- Reunir y conservar el filtrado, que contiene ureasa.


Investigación
Los volúmenes que se indican a continuación son (~ 10 ml) para tubos de ensayo de vidrio estándar.
En primer lugar, pedir a los estudiantes que comprueben cómo el pH influye en el color del extracto de lombarda.
- Verter 3 ml de indicador de col roja en cada uno de los tres tubos.
- Agregar 2 gotas de solución de ácido cítrico en el primer tubo de ensayo. Mezclar y observar el cambio de color. Enjuague la pipeta con agua después de la adición de cada componente.
- Agregar 2 gotas de solución de bicarbonato de sodio en el segundo tubo de ensayo. Mezclar y observar el cambio de color.
- Agregar 2 gotas de agua destilada en el tercer tubo de ensayo. Mezclar y observar el cambio de color.
- Comparar y tomar nota de los colores de las soluciones en los tres tubos de ensayo. Coloque los tubos de lado para que actúe como referencia.
A continuación, investigue el efecto de la ureasa de soja en la urea.
- Añadir 2 ml del indicador de col roja a cada uno de los tres tubos.
- Mezcle 2 ml de solución de urea en dos de cada uno de estos tubos. Tenga en cuenta el color.
- Añadir 2 ml de la suspensión de soja a cada tubo y el resto a uno de los tubos con solución de urea.
- Comparar los colores y los olores de las mezclas en todos los tubos. Repita esta observación a los 3 min.
Interpretación
El indicador de col roja se pone verde con el aumento de pH. Este cambio de color, junto con el olor a amoníaco, puede ser detectado en un tubo que contiene la enzima y su sustrato. En tubos que contienen solo la enzima o sólo sustrato, el pH se mantiene estable, por lo que el indicador de col roja permanece violeta.
Seguridad
Aproximadamente el 1% de los niños puede ser alérgico al extracto de soja (véase McGee, 2004). A los profesores se les aconseja comprobar que ninguno de sus alumnos puede verse afectado antes de intentar este protocolo.
Nuevas investigaciones
Una prueba de seguimiento podría llevarse a cabo para investigar los factores que influyen en la actividad enzimática (como la temperatura, el pH y las concentraciones de enzima, sustrato y producto).
Agradecimientos
Este práctico protocolo fue desarrollado por Anna Lorenc para el proyecto Volvox, que está financiado por el Sexto Programa Marco de la Comisión Europea.
El proyecto Volvox
El equipo del proyecto Volvox es un grupo de profesores de biología y especialistas de diez países de la Unión Europea, con vistas a proporcionar profesores de biología a la enseñanza secundaria y otros con protocolos de laboratorio, simulaciones, actividades de clase y muchos otros recursos educativos. Ver www.eurovolvox.org.
References
- Ainsworth C (2008) Locking the cradle. Science in School 8: 25-28. www.scienceinschool.org/2008/issue8/rabies
- McGee H (2004) On food and cooking. London, UK: Hodder & Stoughton. ISBN: 0340831499
Review
La actividad de la enzima es investigada con frecuencia utilizando la acción de la amilasa sobre el almidón, que vincula a la alimentación y la nutrición. El método simple presentado aquí es un buen cambio, que enlaza con el ciclo del nitrógeno, que puede ser un concepto difícil de entender para los estudiantes. La idea de utilizar un indicador natural que los estudiantes pueden utilizar hace que la lección sea más divertida. Además, los estudiantes pueden oler el producto de la reacción debido a la liberación de amoniaco. Factores que afectan la actividad enzimática pueden ser investigados en el grupo de trabajo y esto puede ser discutido en una sesión plenaria.
El artículo puede ser utilizada como prueba de comprensión haciendo preguntas tales como:
- ¿Por qué las hojas de col se ponen en agua hirviendo?
- ¿De qué color será el indicador si el amoníaco está presente en la solución?
- Describa lo que usted puede ver si utiliza el extracto de soja hervida y explicar por qué esto ocurre.
- Comentar cual de los tubos de reacción es el ‘control’ del experimento. Explique lo que esto significa y lo que usted esperaba observar en este tubo.
Shelley Goodman, Reino Unido





