Click ist der Trick: Den Chemie-Nobelpreis 2022 verstehen Inspire article
Dieses Jahr wurde der Chemie-Nobelpreis für die Click-Chemie verliehen. Erfahre mehr über den atemberaubenden methodischen Fortschritt hinter diesem einfach klingenden Namen.
Der diesjährige Chemie-Nobelpreis wurde für die Entwicklung der Click-Chemie und der bioorthogonalen Chemie an Carolyn R. Bertozzi, Morten Meldal und K. Barry Sharpless verliehen.[1] Das war für Chemiker und Biologen keine Überraschung; tatsächlich wurde dieser Nobelpreis seit einiger Zeit erwartet. Oft werden Nobelpreise für sehr spezialisierte Forschungsarbeit vergeben, die sehr wichtig, aber außerhalb ihres speziellen Forschungsthemas relativ unbekannt ist. Click-Chemie dagegen hat die chemische und biologische Forschung derart revolutioniert, dass die meisten Wissenschaftler dieser Forschungsgebiete sie kennen und viele von ihnen sie bereits in ihrer eigenen Forschung angewandt haben. Ich habe diese Chemie selbst im Labor genutzt und habe viele inspirierende wissenschaftliche Arbeiten gelesen, die auf sie als fundamentale Methode gesetzt haben. Aber was sind Click-Chemie und bioorthogonale Chemie und warum haben diese Methoden sich als so wichtiger Fortschritt herausgestellt?
Was ist Click-Chemie?
Als ich mich kürzlich mit einer nicht-wissenschaftlichen Kollegin über den diesjährigen Nobelpreis unterhalten habe, meinte sie, dass Click-Chemie kindlich einfach klingt, wie „LEGO“. Damit hat sie den fundamentalen Fortschritt dieser Arbeit auf den Punkt gebracht! Click-Chemie ist so aufregend und hat sich als so nützlich herausgestellt, weil sie einfach und modular ist. Barry Sharpless definierte Click-Chemie als Reaktionen, die „modular sind, breit gefächerte Anwendungen haben, hohe Ausbeuten erzielen und nur harmlose Nebenprodukte erzeugen.[2] Aber was heißt das und warum sind diese Eigenschaften wichtig?
Eigenschaften von Click-Reaktionen
Modularität – Kleine, einfache reaktive Gruppen können leicht zu größeren Molekülen hinzugefügt werden um verschiedene Arten von Molekülen zu verbinden.
Weiter Anwendungsbereich – Kompatibilität mit einem großen Spektrum funktioneller Gruppen, das heißt, andere Teile des Moleküls stören die Reaktion nicht und werden durch sie nicht beschädigt.
Einfache, milde Reaktionsbedingungen – Idealerweise Raumtemperatur und Atmosphärendruck, und ohne die Notwendigkeit mehrerer Schritte oder Aufreinigungsprozesse
Hohe Ausbeuten – Die Reaktionen sollten idealerweise schnell vollständig ablaufen. Oft wird eine große thermodynamische treibende Kraft genutzt, um das zu erreichen.
Spezifität – Reaktionen sollten nur an den vorgesehenen funktionellen Gruppen stattfinden und vorhersagbare Produkte ergeben.
Keine scharfen Lösungsmittel – Idealerweise sollten die Reaktionen in wässrigen Lösungen (Wasser) ablaufen anstatt in organischen Lösungsmitteln, oder zumindest mit Wasser und Sauerstoff kompatibel sein.
Harmlose Produkte – Es sollten entweder keine Nebenprodukte entstehen, oder diese sollten ungiftig oder einfach abzutrennen sein.
Stabile Produkte – Sie sollten nicht weiter reagieren oder unter physiologischen Bedingungen zersetzt werden und sie sollten einfach zu isolieren sein.
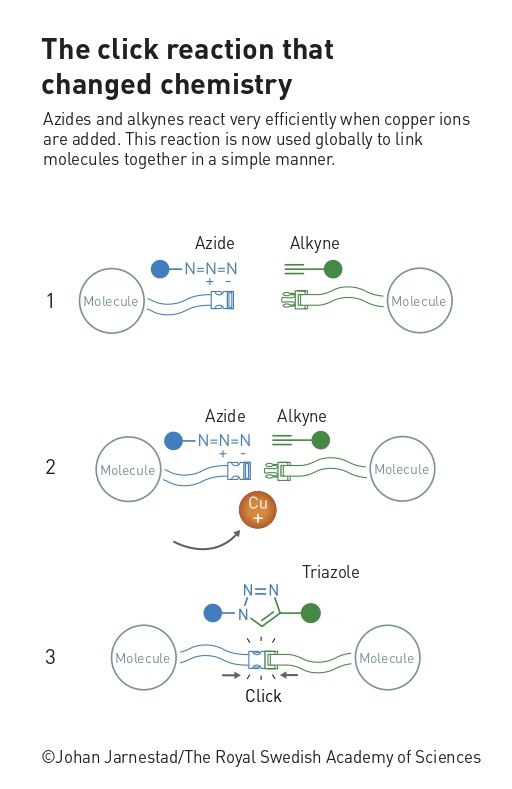
Die bekannteste Click-Reaktion ist die Kupfer(I)-katalysierte Azid-Alkin-Cycloaddition (CuAAC), die in den Gruppen von Barry Sharpless[3] und Morten Meldal.[4] unabhängig voneinander entdeckt wurde. Diese Reaktion macht genau was der Name sagt: Ein Azid und ein Alkin reagieren in Anwesenheit von Kupfer direkt zu einem stabilen zyklischen Triazol-Produkt.
Warum ist Click-Chemie so nützlich?
In gewisser Weise sind die interessantesten Teile dieser Reaktionen die Moleküle, an die die Click-reaktiven Gruppen oder ‚Griffe‘ angehängt werden. Diese können fast alles sein, von Proteinen über Wirkstofffragmente zu Nanopartikeln. Viele chemische Reaktionen um Moleküle zu verbinden benötigen scharfe (und nicht umweltfreundliche) Reaktionsbedingungen, zum Beispiel hohen Druck oder hohe Temperatur, schädliche organische Lösungsmittel, die anschließend sorgfältig entsorgt werden müssen, oder mehrere Schritte mit Aufreinigungen dazwischen. Außerdem sind sie oft nicht selektiv (sie ergeben eine Mischung aus Produkten), inkompatibel mit gewissen funktionellen Gruppen anderswo in den Molekülen, funktionieren nicht in Anwesenheit von Wasser oder Sauerstoff, ergeben niedrige Ausbeuten oder produzieren toxische und reaktive Nebenprodukte, die schwierig abzutrennen sind. Die Nachteile dieser Eigenschaften sind offensichtlich und Click-Reaktionen haben Wissenschaftlern vieler Forschungsgebiete ermöglicht, Substanzen einfacher zu synthetisieren oder zu modifizieren. Zum Beispiel können sie genutzt werden, um Substanzbibliotheken für die Wirkstoffentwicklung herzustellen[5,6] oder um funktionalisierte Polymere und Nanomaterialen zu konstruieren.[7] Wichtig ist auch, dass die einfache, modulare Natur von Click-Reaktionen auch Leuten, die keine Experten in organischer Chemie sind, ermöglicht, die Bausteine zu bestellen und deren Reaktionen in ihrer Forschung zu verwenden.
Die milden, wässrigen Reaktionsbedingungen, Spezifität und breite Anwendbarkeit der Click-Chemie haben sich als unglaublich nützlich für die Biokonjugation erwiesen, das heißt für Reaktionen mit Biomolekülen wie Proteinen, Kohlenhydraten, Lipiden und Nukleinsäuren. Diese komplexen Moleküle haben viele funktionelle Gruppen, sind schwer spezifisch zu modifizieren und werden oft von organischen Lösungsmitteln oder scharfen Reaktionsbedingungen zerstört. Warum wollen wir Biomoleküle überhaupt chemisch modifizieren? Es gibt viele Gründe, ein besonders wichtiger ist ‚Labeling‘.[8,9] Unser Artikel über Fluoreszenzmikroskopie gibt ein Beispiel dafür. Es ist wichtig, bestimmte Biomoleküle in Zellen lokalisieren zu können, um ihre Funktionen in Gesundheit und Krankheit zu verstehen. Biokonjugationsreaktionen ermöglichen das Anhängen von Fluorophoren, welche mit Fluoreszenzmikroskopie verfolgt werden können. Auch viele andere Label können angehängt werden, zum Beispiel zur Aufreinigung oder medizinischen Bildgebung. Eine andere Anwendung der Biokonjugation ist das ‚Targeting‘, wobei ein Wirkstoff an eine Targeting-Gruppe angehängt wird um sicherzugehen, dass er das richtige Protein oder Gewebe (zum Beispiel einen Tumor) erreicht. Solche Targeting-Ansätze können schädliche Nebenwirkungen reduzieren, da die benötigte Menge an Wirkstoff reduziert und sichergestellt wird, dass dieser nicht am falschen Ort wirkt.
Und was ist bioorthogonale Chemie?
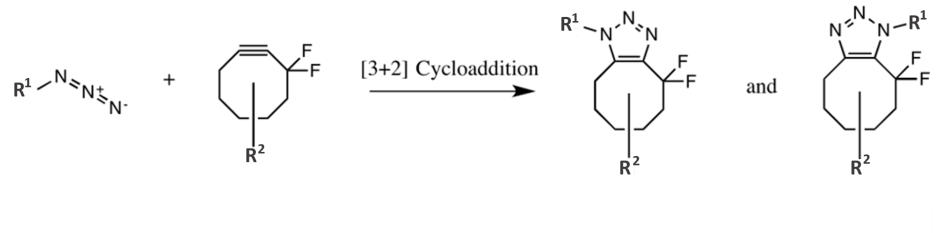
Obwohl die CuAAC mit Biomolekülen kompatibel ist, kann sie nicht in lebenden Systemen benutzt werden, weil Kupfer giftig ist. Hier kommt der zweite Teil des Nobelpreises ins Spiel. Carolyn Bertozzi prägte den Begriff „bioorthogonal“ für Reaktionen, die in biologischen Systemen ausgeführt werden können, ohne von den umgebenden biologischen Prozessen beeinflusst zu werden und ohne diese zu stören. Sie erhielt den Preis für die Entwicklung von Reaktionen, die keine toxischen Metalle als Katalysatoren benötigen und in lebenden Zellen angewandt werden können, insbesondere der spannungsunterstützten Azid-Alkin-Cycloaddition (SPAAC).[10] In diesem Fall destabilisiert die Ringspannung im Difluoroctin-Ausgangsmaterial dieses so sehr, dass die Reaktion ohne Katalysator effizient abläuft.
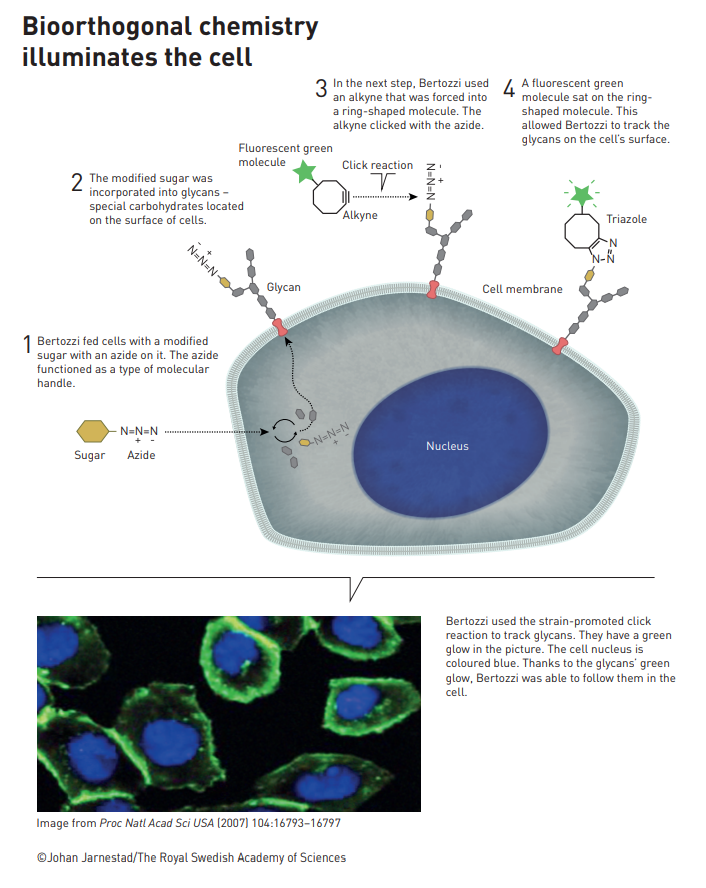
Das hat neue Wege eröffnet, Click-Chemie zur Untersuchung von Zellbiologie zu nutzen. Methoden wie Gencode-Erweiterung oder „Metabolic Engineering“ können genutzt werden, um Zellen dazu zu bringen, Biomoleküle mit einem angehängten Click-‚Griff‘ herzustellen.[11] Diese Biomoleküle können dann in lebenden Zellen modifiziert werden, indem man einen Click-modifizierten Reaktionspartner hinzugibt. Das ermöglicht es Wissenschaftlern, biologische Prozesse in Echtzeit zu beeinflussen und zu verfolgen. Die Bertozzi-Gruppe hat diese Reaktionen genutzt um Glykosylierung (das Anhängen von Zuckern oder Kohlenhydraten an Biomoleküle in der Zelle) zu untersuchen, einem sehr wichtigen zellulären Prozess mit vielen Auswirkungen auf Gesundheit und Krankheit.[12]
Zusammenfassung
Es ist schwierig, den Einfluss der Click-Chemie und bioorthogonalen Chemie auf die Wissenschaft zu übertreiben, insbesondere auf die physiologische, biochemische, biomedizinische und Materialforschung. Einige zusätzliche Click- und bioorthogonale Reaktionen sind seit dieser bahnbrechenden Arbeit entwickelt worden und diese chemischen Werkzeuge haben unzählige wichtige Entdeckungen und Fortschritte ermöglicht. Das hebt klart die multidisziplinäre Natur moderner Forschung hervor. Die ursprüngliche Arbeit wurde von organischen Chemikern gemacht und wird nun in vielen verschiedenen Forschungsfeldern breit genutzt, von der Zellbiologie bis zur Wirkstoffentwicklung oder Polymerforschung. Es gibt ein hohes Maß an öffentlichem Missverständnis darüber, welche Art der Forschung wichtig ist. Die Leute denken oft, dass Forschung, die sich nicht direkt mit einem gesellschaftlichen Bedürfnis wie der Entwicklung von Medizin oder Technologie befasst, Geldverschwendung wäre. Hingegen sind Methodenentwicklung und Grundlagenforschung an fundamentalen Fragen wesentliche Bausteine für die lebensverändernden Anwendungen der Zukunft.
References
[1] Carolyn R. Bertozzi, Morten Meldal, and K. Barry Sharpless are awarded the Nobel Prize in Chemistry, 2022: https://www.nobelprize.org/uploads/2022/10/advanced-chemistryprize2022-2.pdf
[2] Kolb HC et al. (2001) Click Chemistry: Diverse chemical function from a few good reactions. Angewandte Chemie 40: 2004–2021. doi: 10.1002/1521-3773(20010601)40:11<2004::AID-ANIE2004>3.0.CO;2-5
[3] Rostovtsev VV et al. (2002) A Stepwise Huisgen Cycloaddition Process: Copper(I)-Catalyzed Regioselective “Ligation” of Azides and Terminal Alkynes. Angewandte Chemie 41: 2569–2599. doi: 10.1002/1521-3773(20020715)41:14<2596::AID-ANIE2596>3.0.CO;2-4
[4] Tornøe CW, Christensen C, Meldal M (2002) Peptidotriazoles on Solid Phase: [1,2,3]-Triazoles by Regiospecific Copper(I)-Catalyzed 1,3-Dipolar Cycloadditions of Terminal Alkynes to Azides. The Journal of Organic Chemistry 67: 3057–3064. doi: 10.1021/jo011148j
[5] Hein CD, Xiu X, Wang D (2008) Click Chemistry, a Powerful Tool for Pharmaceutical Sciences. Pharmaceutical Research 25: 2216–2230. doi: 10.1007/s11095-008-9616-1
[6] Sharpless KB, Manetsch R (2006) In situ click chemistry: a powerful means for lead discovery. Expert Opinion on Drug Discovery 1: 525–538. doi: 10.1517/17460441.1.6.525
[7] Geng Y et al. (2021) Click chemistry strategies for the accelerated synthesis of functional macromolecules. Journal of Polymer Science 59: 963–1042. doi: 10.1002/pol.20210126
[8] Kaur J, Saxena M, Rishi N (2021) An Overview of Recent Advances in Biomedical Applications of Click Chemistry. Bioconjugate Chemistry 32: 1455–1471. doi: 10.1021/acs.bioconjchem.1c00247
[9] Zuin Fantoni N, El-Sagheer AH, Brown T (2021) A Hitchhiker’s Guide to Click-Chemistry with Nucleic Acids. Chemical Reviews 121: 7122–7154. doi: 10.1021/acs.chemrev.0c00928
[10] Agard NJ et al. (2006) A Comparative Study of Bioorthogonal Reactions with Azides. ACS Chemical Biology 1: 644–648. doi: 10.1021/cb6003228
[11] Nikić I, Lemke EA (2015) Genetic code expansion enabled site-specific dual-color protein labeling: superresolution microscopy and beyond. Current Opinion in Chemical Biology 28: 164–173. doi: 10.1016/j.cbpa.2015.07.021
[12] Agard NJ, Bertozzi CR (2009) Chemical Approaches To Perturb, Profile, and Perceive Glycans. Accounts of Chemical Research 42: 788–797. doi: 10.1021/ar800267j
Resources
- Lies die Erklärung der Nobelpreis-Organisation zur Bedeutung der Click-Chemie und bioorthogonalen Chemie.
- Lies einen Artikel in The Guardian über den Chemie-Nobelpreis 2022.
- Versuche dieses Rollenspiel um zu verstehen, wie Forschungsprojekte finanziert werden und wie wichtig Grundlagenforschung ist McHugh M et al. (2021) What is it good for? Basic versus applied research. Science in School 55.
- Tritt die Mystery Box-Herausforderung an, um etwas über die Natur der Wissenschaft zu lernen: Horvat AK et al. (2022) The mystery box challenge: explore the nature of science. Science in School 59.
- Lerne wie Fluoreszenzmikroskopie unser Darmmikrobiom beleuchten kann: Ponnudurai RP (2022) Shedding light on the gut microbiome. Science in School 60.
- Lies ein Interview mit dem diesjährigen Gewinner des Medizin-Nobelpreises, Svante Pääbo : Hayes E (2011) An archaeologist of the genome: Svante Pääbo. Science in School 20: 6–12.
- Lies ein Interview mit dem Gewinner des Medizin-Nobelpreises 2001, Tim Hunt: Gebhardt P (2007) Eyes on the horizon, feet on the ground: interview with Tim Hunt. Science in School 18: 9–13.