Ausflippen wegen Biochemie und Bananen Teach article
Verstehe eine Reihe biochemischer Prozesse mithilfe dieser schnellen und einfachen Experimente mit einer der beliebtesten Obstsorten der Welt.
Bananen sind eine der beliebtesten Obstsorten weltweit – mehr als 100 Milliarden von ihnen werden jedes Jahr verzehrt. Sie sind nicht nur ein Grundnahrungsmittel für Millionen von Menschen sondern auch eine wichtige Quelle für Einkommen und Arbeit, insbesondere in Lateinamerika.
Zusammen mit Kochbananen sind die Bananen ein Teil der Gattung Musa, die circa 70 Arten umfasst. Heutzutage kommen jedoch fast alle süßen Bananen von einer einzelnen Variante mit dem Namen Cavendish. Diese Bananen werden unter Verwendung asexueller Reproduktion kultiviert, sodass sie genetisch identisch sind. Dieser Verlust an Biodiversität macht sie jedoch äußerst verwundbar durch parasitäre Attacken – wie momentan geschehen durch eine globale Infektion mit dem Pilz Fusariumw1.
Was vielleicht einige überrascht ist die Eignung der Banane als gute Möglichkeit, biochemische Prozesse zu verstehen. In dieser Reihe schneller Klassenraumaktivitäten rund um die Banane erfahren die Schülerinnen einiges zum Zuckerstoffwechsel, Stärkespeicherung, Melaninproduktion und die Moleküle, die für den Bananengeschmack verantwortlich sind. Die Aktivitäten sind für Schülerinnen der Sekundarstufen geeignet und bauen auf Chemie auf verschiedenen Schwierigkeitsniveaus auf.

Hanna_photo/Shutterstock.com
Aktivität 1: Messung des Zuckergehalts mit einem Refraktometer
Vor Beginn der eigentlichen Aktivität zeigen Sie ihren Schülerinnen sechs Bananen unterschiedlichem Reifegrades (vergleiche Bananen 1-6 in Tabelle 1, welche aufsteigend nach ihrem Reifegrad sortiert sind). Welche Banane ist nach Meinung der Lernenden die süßeste? Die meisten Schülerinnen werden auf die schwarze Banane tippen, aber liegen sie damit richtig? Die Lernenden können einen Geschmackstest mit verbundenen Augen durchführen. Können ihre Geschmacksknospen die richtige Antwort erschmecken? Um das herauszufinden messen die Lernenden den Zuckergehalt der verschiedenen Bananen mit einem Refraktometer. Die Aktivität dauert ca. 20 Minuten.
Materialien
- Bananen mit verschiedenem Reifegrad (je drei Bananen für jeden der sechs Grade, z.B. insgesamt 18 Bananen)
- Multiskalen-Refraktometer
- Gabel
- Schüssel
- weiches, feuchtes Tuch
Durchführung
- Schäle die unreifste Banane (Banane 1 in Tabelle 1) und brich ein Stück von ca. 3 cm Länge ab.
- Zerdrück das Bananenstück mit der Gabel in der Schüssel, bis du einen halbflüssigen Brei erhälst.
- Trage etwas Brei auf das Messprisma des Refraktometers auf. Schließ die Öffnung, sodass sich der Brei auf der gesamten Oberfläche des Prismas verteilt ohne Luftblasen oder trockene Stellen zu bilden.
- Halte den Refraktor in eine natürliche Lichtquelle und schau in das Okular. Du wirst ein rundes Feld mit einer Skala sehen, die einen Wert in % Brix anzeigt – die Anzahl an Gramm Saccharose pro 100 Gramm Probe (z.B. 1 g Saccharose in 100 g Probe = 1 % Brix). Du musst möglicherweise das Okular fokussieren, um die Skala deutlich zu erkennen.
- Notiere den Zuckergehalt in % Brix.
- Säubere das Instrument (sowohl die Klappe als auch das Prisma) mit dem feuchten Tuch.
- Wiederhole die Schritte 1-6 für mindestens drei weitere Bananen des gleichen Reifegrads und errechne dann den mittleren Zuckergehalt (vgl. Tabelle 1 und Abbildung 1).
- Wiederhole die Aktivität bis du den mittleren Zuckergehalt der Bananen 1-6 ermittelt hast.
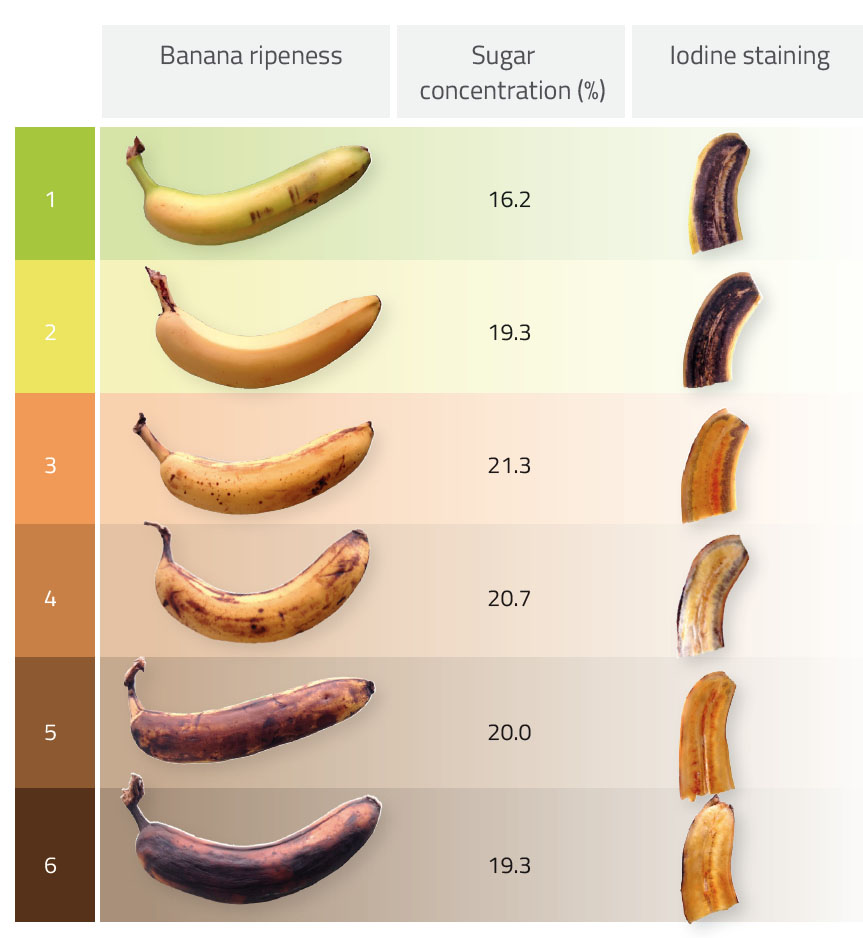
Jill Skarvan
Banana ripeness: Reifegrad der Banane, Sugar concentration (%): Zuckerkonzentration (%), Iodine staining: Iodfärbung

Jill Skarvan
Sugar content (% Brix): Zuckergehalt (% Brix), Degree of ripeness: Reifegrad
Aktivität 2: Analyse des Stärkegehalts mit Iod
Hierbei benutzen die SchülerInnen Lugol’sche Iodlösung um die Anwesenheit von Stärke in Bananen nachzuweisen, wobei gezeigt wird, dass die Stärkemenge während des Reifeprozesses abnimmt. Diese Aktivität dauert ca. zehn Minuten.
Materialien
- Bananen mit unterschiedlichem Reifegrad (je drei Bananen für jeden der sechs Reifegrade, z.B. 18 Bananen insgesamt)
- Lugol’sche Lösung: 2% Kaliumiodid mit 1% Iod in Wasser (I3K)
- Küchenmesser
- Bürste
Durchführung
- Schneide jede Banane längs durch.
- Bestreiche die Oberfläche der Banane mit einer Bürste mit Lugol’scher Iodlösung.
- Warte eine Minute und vergleiche die unterschiedlichen Ergebnisse (s. Tabelle 1).
Diskussion
Während des Reifeprozesses katalysiert das Enzym Amylase den Abbauprozess von Stärke (einem Polysaccharid) zu einfachem Zucker – zuerst zu Maltose (ein Disaccharid) und dann zu Glucose (ein Monosaccharid). In der Aktivität ist die Banane 3 in Tabelle 1 diejenige mit dem höchsten Zuckergehalt (in Form von Mono- und Disacchariden). Nach dieser Stufe der Reifung beginnt der Zuckergehalt zu sinken, weil die Mehrheit der Stärke zu einfachen Zuckern abgebaut wurde und die Banane fortlaufend Glucose für die Zellatmung verbraucht.
Dieses Phänomen wird auch bei der Reaktion mit der Lugol’schen Lösung verdeutlicht: unreife Bananen haben einen höheren Stärkeanteil als reife Bananen, was durch eine dunklere Färbung mit Lugol’scher Lösung gezeigt wird. Mit weiterer Reifung ist die Färbung wegen dem geringeren Stärkegehalt deutlich reduziert.
In einem Blindtest könnten die SchülerInnen nicht diejenige Banane mit dem höchsten Zuckergehalt als die süßeste auswählen. Andere Faktoren die den Geschmack beeinflussen können beinhalten die Weichheit der Banane und ihr Wassergehalt. Darüber hinaus werden Nahrungsmittel, die viel Stärke aber wenig Zucker enthalten, beim Kauen süßer, weil die Amylase, die auch im Speichel präsent ist, einige Stärkemoleküle zu Zucker abbaut.
Diskutieren Sie einige der folgenden Fragen mit ihren SchülerInnen:
- Welche Banane ist die süßeste?
- Warum steigt der Zuckergehalt zu Beginn des Reifeprozesses an, aber sinkt zum Ende hin?
- Wie ändert sich der Stärkegehalt während des Reifeprozesses?
- Ist am Anfang oder am Ende des Reifeprozesses der Stärkegehalt der Banane höher oder niedriger? Kannst du begründen?
- Ist Süße nur vom Zuckerhalt abhängig oder beeinflussen auch andere Faktoren die Süße?
Aktivität 3: Den Speicherort der Stärke ausfindig machen
In dieser Aktivität stellen die SchülerInnen miskroskopische Präparate von Bananenbrei der reifsten und unreifsten Banane her. Unter dem Mikroskop können die Lernenden die Organellen der Stärkespeicherung (Amyloplasten) sehen und verstehen, warum diese Organellen während des Reifeprozesses verschwinden. Diese Aktivität dauert ca. 15 Minuten.
Materialien

Bananenbrei für die
Betrachtung unter dem
Mikroskop
Samuel Ginsburg
- Bananenbrei aus Aktivität 1 (Banane 1 und 6 aus Tabelle 1)
- Lugol’sche Iodlösung
- Mikroskop
- Objektträger
- Deckgläser
Durchführung
- Schmiere eine kleine Menge Bananenbrei auf einen Objektträger und füge einen Tropfen Lugol’sche Lösung hinzu (Abbildung 2).
- Platziere ein Deckgläschen auf die Probe. Versuche bei 100- und 400facher Vergrößerung die Organellen zu finden, die die Stärke in Bananen speichern.
- Wiederhole die Schritte 1 und 2 mit der anderen Bananenbreiprobe.
Diskussion
Amyloplasten sind für die Synthese und die Speicherung von Stärkekörnern durch Polymerisierung von Glucose zuständig. In unreifen Bananen führt die Zugabe von Lugol’scher Lösung zu einer tiefvioletten Färbung der Stärke und der Amyloplasten (Abbildung 3). In reiferen Bananen kommt es zu keiner Reaktion mit der Lösung, weil der Stärkegehalt stark reduziert ist und die Amyloplasten in den Proben nicht mehr vorliegen. (Abbildung 4).
Diskutieren Sie einige der folgenden Fragen mit ihren SchülerInnen:
- Warum wird Iod zur Bananenprobe hinzugefügt?
- Wie ist der Name der Organelle, die Stärke in Pflanzen speichert?
- Welche Unterschiede kannst du bei diesen Organellen in den verschiedenen Bananenproben erkennen und warum?

Samuel Ginsburg

Samuel Ginsburg
Aktivität 4: Bananen werden schwarz

Eintauchen der halben
Banane in kochendes Wasser
wird die Schale aufgrund der
Melaninproduktion schwarz.
Sacha Glardon
SchülerInnen lernen mit dieser einfachen Aktivität etwas über den Effekt der Melaninproduktion und Zellschäden in Bananen. Dazu werden sie einfach in heißes Wasser getaucht, was dazu führt, dass ihre Schale schwarz wird. Die Aktivität dauert ungefähr fünf Minuten.
Materialien
- Gelbe Banane (z.B. Banane 2 aus Tabelle 1)
- 1 Ein-Liter-Becherglas mit kochendem Wasser
Durchführung
- Tauche die halbe Banane in das heiße Wasser.
- Nach einer Minute wird die untergetauchte Hälfte schwarz (s. Abbildung 5).
Diskussion
Wenn die Banane in heißes Wasser getaucht wird, sind ihre Zellen Hitze ausgesetzt, die Zellschäden verursacht. Als Antwort darauf wird das dunkle Pigment Melanin gebildet, was zur Schwarzfärbung der Bananenschale führt. Das Pigment schützt Außenzellen (sowohl in pflanzlichen als auch tierischen Lebewesen) vor Schäden durch ultraviolette Strahlung und wirkt durch seine antioxidative Eigenschaft freien Radikalen entgegen. Melanin entsteht durch die Oxidation der Aminosäure Tyrosin, was durch ein kupferhaltiges Enzym names Tyrosinase katalysiert wird. Wenn Bananenzellen beschädigt sind, wird Tyrosinase freigesetzt. Die Melaninproduktion beeinflusst nicht den Reifeprozess, aber da reife Bananen älter sind und dadurch mehr Zellschäden erlitten haben, sind sie brauner.
Diskutieren Sie die folgenden Fragen mit ihren Lernenden:
- Warum wird die Banane schwarz?
- Was verursacht diesen Farbwechsel?
- Beschleunigt das Eintauchen in heißes Wasser den Reifungsprozess?
- Was ist der Unterschied zwischen einer Banane in heißem Wasser und einer natürlich schwarzen Banane?
Aktivität 5: Herstellung von künstlichem Bananenaroma
Diese Aktivität richtet sich an SchülerInnen zwischen 16 und 19 Jahren und beinhaltet die Synthese künstlicher Geschmacksstoffe. Unter Verwendung von 2-Methyl-1-Butanol können die Lernenden den organischen Stoff Isoamylacetat (3-Methylbutylethanoat) produzieren, der einen ähnlichen Geruch wie Bananen und Birnen aufweist. Alternativ kann 1-Pentanol verwendet werden. Hierbei stellen die Lernenden Amylacetat (Pentylethanoat), her, was einen Geruch ähnlich der Banane oder des Apfels hat. Diese Aktivität dauert 15 Minuten. Möglicherweise sollten Sie die Klasse aufteilen, sodass die eine Hälfte Isoamylacetat und die andere Hälfte Amylacetat herstellt. Die Gruppen können im Anschluss die Gerüche vergleichen.
Materialien
- Essigsäure (CH3COOH)
- 2-Methyl-1-Butanol (C5H12O) oder 1-Pentanol (C5H12O)
- Schwefelsäure (H2SO4)
- Siedesteine
- Bunsenbrenner
- Reagenzglas
- 500-ml-Becherglas
Sicherheitshinweis
Dieses Experiment verwendet Schwefelsäure. Die SchülerInnen sollten Schutzbrillen und Handschuhe tragen und den üblichen Sicherheitsstandards des Chemieunterrichts Folge leisten. Wie bei allen chemischen Experimenten dürfen die Lernenden die Stoffe nicht probieren. Beachten Sie auch die allgemeinen Sicherheitshinweise.
Durchführung
- Pipettiere 2 ml Essigsäure in das Reagenzglas.
- Füge 2 ml 2-Methyl-1-Butanol oder 1-Pentanol hinzu.
- Vermische die Edukte und gib einen Tropfen Schwefelsäure hinzu.
- Erhitze die Mischung für etwa zwei Minuten, über dem Bunsenbrenner, ohne sie zu kochen. Die Zugabe von Siedesteinen verhindert ein Überhitzen. Achte darauf, die Öffnung des Reagenzglases nicht auf Mitschüler zu richten.
- Schütte den Inhalt des Reagenzglases in einen 500-ml-Becherglas, um den Geruch zu intensivieren.
Diskussion
Isoamylacetat und Amylacetat sind die Hauptbestandteile von künstlichem Bananenaroma, auch wenn die Aromaproduzenten ihre genauen Rezepturen geheim halten. Isoamylacetat entsteht bei der Kondensation von 2-Metyhl-1-Butanol mit Essigsäure, während Amylacetat bei der Kondensation von 1-Pentanol mit Essigsäure entsteht. Beide Veresterungsreaktionen werden durch Schwefelsäure katalysiert (Abbildung 6). Wie bei allen Früchten ist der natürliche Geschmack bei Bananen eine Mischung aus vielen verschiedenen Komponentenw2, es ist also für künstliche Aromen sehr kompliziert, den Geschmack und Geruch exakt zu imitieren.
Diskutieren Sie einige der folgenden Fragen mit ihren SchülerInnen:
- Wie riechen die Produkte der Reaktion?
- Welches Molekül ist für den typischen Bananengeschmack verantwortlich?
- Was ist der Unterschied zwischen natürlichen und künstlichen Aromen und warum riechen sie unterschiedlich?

Sacha Glardon
Acetic acid: Essigsäure, 2-methyl-1-butanol: 2-Methyl-1-Butanol, Isoamyl acetate: Isoamylacetat, 1-pentanol: 1-Pentanon, Amyl acetate: Amylacetat
Vertiefende Aktivitäten: Mehr über Bananen erfahren
Es gibt eine große Zahl zusätzlicher Aktivitäten, die Sie durchführen können und die Ihnen weitere Einblicke in die Biologie und Chemie der Banane und Verbindungen zu anderen interdisziplinären Themen gewähren. Sie könnten z.B.:
- Bananen-DNA isolieren um zu verstehen, dass alle lebenden Organismen (Bananen eingeschlossen) DNA beinhalten, welche die genetischen Informationen speichert, die von der Elterngeneration auf die Nachkommen übergeben wird.
- Verdeutlichen Sie die Zellatmungsaktivität, indem Sie eine Banane in einem luftdichten Behälter verwahren und mit CO2– und O2-Sensoren die sich ändernden Konzentrationen messen.
- Verstehen die den Stärkeabbau und seinen Effekt auf den Blutzuckerspiegel und die Speicherung von Glykogen in der Leber besser, indem sie den Blutzuckerspiegel alle 15 Minuten nach dem Verzehr einer Banane messen (falls in ihrem Land zulässig).
- Untersuchen Sie die Bedeutung von Biodiversität im Zusammenhang mit Krankheitsausbrüchen.
- Vollziehen Sie die historischen, wirtschaftlichen und ethischen Faktoren des Bananenhandels nach.
Web References
- w1 – Eine der verheerendsten Krankheiten die momentan die Banane bedroht geht vom Pils Fusarium aus. Erfahren Sie mehr dazu auf der Website der Ernährungs- und Landwirtschaftsorganisation der Vereinten Nationen.
- w2 – James Kennedy, ein Chemielehrer aus Australien hat eine tolle Grafik entworfen, die eine Liste aller Inhaltsstoffe in ‘allen natürlichen Bananen’ zeigt.
Resources
- Lesen Sie mehr über die Produktion von und den Handel mit Bananen auf der Banana Link Website.
- Für die Geschichte der Banane schauen sie dieses Video von National Geographic.
Institutions
Science on StageReview
Dieser Artikel beschreibt eine Sammlung einfacher aber bedeutsamer Experimente unter Verwendung einer alltäglichen Obstsorte (Bananen) mit dem Ziel, grundlegende Stoffwechselprozesse zu verstehen. Der Reifeprozess (und die damit verbundenen Farbänderungen) werden beispielsweise verwendet, um die Umwandlung von Stärke in Maltose und Glucose zu verdeutlichen. Für einen Erfolg sollten die SchülerInnen den Unterschied zwischen einfachen und komplexen Kohlenhydraten kennen. Lehrer können mit den vorbereiteten Diskussionsfragen einen Einstieg finden oder den Lernzuwachs festigen und erhöhen.
Monica Menesini, Sekundarschullehrerin für Naturwissenschaften (pensioniert), Italien





