Chimica e luce Understand article
Tradotto da Teresa Celestino. Peter Douglas e Mike Garley indagano su come chimica e luce interagiscono in molti aspetti della nostra vita quotidiana.

concessione di BlackJack3D /
iStockphoto
Da sempre utilizziamo i raggi solari per scaldarci durante il giorno e lo scintillio della fiamma per illuminare la notte. Oggi siamo in grado di controllare la conversione di energia per ottenere luce dall’elettricità, dal calore e da reazioni chimiche; nella vita quotidiana usiamo la chimica e la luce per le comunicazioni, nell’elettronica, in medicina e nelle attività ludiche; i fotochimici stanno lavorando per un futuro più pulito e brillante ideando nuovi metodi per convertire la luce solare in energia utile e per la rimozione fotochimica degli inquinanti.
Le sorgenti luminose: la lampadina, il laser, il LED e la luce liquida
Nel processo di produzione della luce il passaggio fondamentale è rappresentato dalla conversione di energia. Vari tipi di lampade e dispositivi di illuminazione convertono l’energia con modalità differenti e con diverso rendimento.
Nella lampadina a tungsteno, l’energia elettrica scalda un filamento finché non diventa bianco incandescente; in questo modo l’energia termica è convertita in energia luminosa. L’emissione di luce da parte di un filamento solido produce uno spettro continuo nel campo del visibile, come nell’arcobaleno. Purtroppo il rendimento con il quale l’energia elettrica è convertita in energia luminosa è solo del 5-10% circa.

Immagine per gentile
concessione di mipokcik /
iStockphoto
Nella lampada fluorescente l’energia elettrica è convertita in energia di eccitazione degli atomi di mercurio presenti all’interno di un tubo sotto forma di vapore. In questo caso la conversione di energia avviene con un rendimento intorno al 20%, circa il doppio rispetto a quello di una lampadina a tungsteno. Tuttavia lo spettro di luce emessa da queste lampadine (quello che si ottiene quando gli elettroni ritornano allo stato fondamentale) non è continuo: la luce è emessa a specifiche lunghezze d’onda e colori corrispondenti ai livelli di energia degli atomi di mercurio. Pertanto le lampade fluorescenti per uso domestico sono rivestite internamente di fosforo bianco per aumentare la continuità dello spettro di emissione. Se al posto del vapore di mercurio ci sono altri gas come il neon (che dà una luce arancione) o altri gas inerti, si ottengono lampade fluorescenti variamente colorate, usate per schermi e insegne luminose (vedere la foto). Inoltre diversi tipi di rivestimenti di fosforo cambiano il colore della luce emessa dalla lampada.

Immagine per gentile
concessione di Petrovich9 /
iStockphoto
L’energia elettrica può essere convertita ancora più efficacemente in luce tramite diodi ad emissione luminosa (LED); l’elettricità eccita gli elettroni in appositi semiconduttori (vedere il glossario per i termini in corsivo) a struttura stratificata fino a produrre luce visibile, con un rendimento al di sopra del 35%. I pannelli elettroluminescenti sfruttano lo stesso principio. Anche molti laser utilizzano l’energia elettrica per generare luce laser ad alta intensità, che può essere concentrata in un raggio molto sottile e intenso. I laser ad alta potenza possono tagliare il metallo o persino essere usati come bisturi luminosi in chirurgia.

mentre emette
chemiluminescenza
Immagine di pubblico dominio;
fonte: Wikimedia Commons
Il laser sono anche usati nelle comunicazioni e nella tecnologia digitale dei lettori di codici a barre e a disco ottico.
La “luce liquida” è basata su un altro genere di conversione energetica – la chemiluminescenza – con la quale si ottiene luce fredda tramite reazioni chimiche piuttosto che energia termica. E’ così che funzionano gli stick luminosi chemiluminescenti. In natura le lucciole e le creature che vivono nell’oscurità delle grotte o negli abissi marini usano la chemiluminescenza per comunicazioni inter o intra-specie.
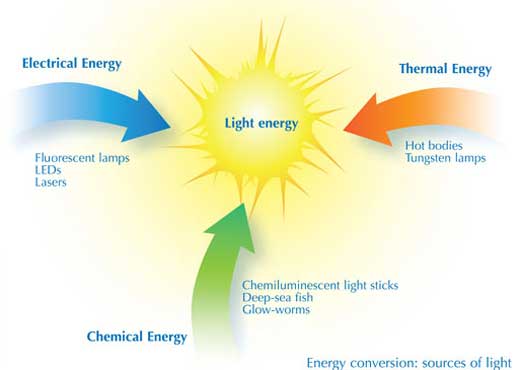
sorgenti di luce
Immagine per gentile
concessione di Nicola Graf
Fotochimica: fluorescenza, materie plastiche, fotografia e medicina
Un tipo di luce emessa – la fluorescenza – è usata negli azzurranti ottici dei detersivi in polvere. Questi assorbono una piccola quantità di radiazione UV della luce solare e la riemettono sotto forma di luce blu, rendendo i capi “più bianchi del bianco”. La fluorescenza è inoltre usata nei sistemi anti-contraffazione delle banconote, mentre la fosforescenza (simile alla fluorescenza ma di più lunga durata) è utilizzata nella segnaletica di sicurezza. Fluorescenza, fosforescenza e chemiluminescenza sono anche utilizzate in articoli di moda come il fondo tinta luminoso, il gel per capelli, il rossetto e i gioielli.
La luce può essere usata per ottenere materie plastiche. Queste sono sintetizzate tramite la polimerizzazione, che consiste nell’unire tante piccole molecole (monomeri) per darne una sola (polimero). Questo processo spesso richiede una certa quantità di energia per essere avviato, ma una volta partito l’energia che si sprigiona dall’unione dei monomeri solitamente basta per assicurarne la continuazione. Quando la luce è assorbita da una molecola, questa diventa più energetica a causa dell’assorbimento dell’energia del fotone; si dice che la molecola è stata eccitata. Queste molecole allo stato eccitato sono eccellenti iniziatori di polimerizzazione a causa del loro surplus di energia – si può così sfruttare la luce per convertire monomeri liquidi in materia plastica solida. Grazie a questo processo chiamato fotopolimerizzazione abbiamo il cemento dentale che indurisce sotto la luce UV, oppure i pigmenti fotoindurenti usati per fissare immagini su un’ampia varietà di substrati – i barattoli delle bibite analcoliche per esempio. A differenza dei pigmenti comuni, i fotoindurenti sono fissati dalla luce piuttosto che tramite il calore e/o l’ossidazione all’aria.

bambino di vetro ‘Bili Rubin’ ,
mentre mostra come la luce è
usata nel trattamento
dell’itterizia
Immagine per gentile
concessione di Peter Douglas
usata in odontoiatria
Immagine per gentile
concessione di dem10 /
iStockphoto
La pellicola fotografica si basa sulle proprietà fotochimiche degli alogenuri d’argento. Quando un granello di alogenuro di argento su una pellicola assorbe un fotone di luce, si produce un atomo di argento. La pellicola è quindi chimicamente trattata, e i granelli di argento metallico costituiscono la parte nera di un negativo bianco e nero.
L’applicazione più nota della fotochimica in medicina è il trattamento dell’itterizia, dovuta all’accumulo nel corpo di una sostanza gialla liposolubile e neurotossica chiamata bilirubina.
La bilirubina è continuamente generata come prodotto dell’emolisi (il processo di distruzione dei globuli rossi del sangue), ma è normalmente metabolizzata nel fegato in una forma solubile in acqua poi espulsa. Tuttavia, se il fegato è danneggiato o non ancora pienamente sviluppato, l’accumulo incontrollato di bilirubina può essere fatale. L’esposizione alla luce blu cura l’itterizia attraverso una trasformazione fotochimica che converte la bilirubina in una forma solubile in acqua, permettendone l’escrezione. Negli ospedali i reparti per i bambini nati prematuri – particolarmente esposti all’itterizia – sono dotati di culle con una speciale illuminazione per il trattamento di questa disfunzione.
Un’altra applicazione medica della fotochimica consiste nella terapia fotodinamica per lottare contro il cancro. Un composto intensamente colorato con una particolare fotochimica è iniettato direttamente nel tumore. Questo composto assorbe in via preferenziale le cellule cancerose rispetto alle cellule normali e, quando irradiato tramite un laser o altra sorgente luminosa, forma molecole allo stato eccitato che reagiscono con l’ossigeno, generando sostanze chimiche letali per le cellule cancerose.

Immagine per gentile concessione di Nicola Graf
Energia pulita, pianeta pulito

Immagine per gentile
concessione di narvikk /
iStockphoto
Il bisogno energetico mondiale aumenta mentre le fonti di energia non rinnovabili sono limitate. Un modo di affrontare il problema consiste nell’utilizzo di minori quantità di energia (ad esempio usando lampade a basso consumo). Un altro modo è quello di sfruttare le fonti di energia rinnovabili come le celle solari di silicio, che convertono l’energia luminosa in elettricità. Le prime celle monocristalline, messe a punto negli anni ’50 per il funzionamento dei satelliti, erano molto costose. Attualmente celle di silicio amorfo o policristallino molto economiche sono comunemente usate nel funzionamento di dispositivi come calcolatrici, caricatori di batterie, così come per usi domestici su larga scala, impianti di produzione dell’energia a livello industriale e persino nazionale.
In classe, la conversione della luce solare in elettricità può essere osservata con una cella di Grätzel, che sfrutta la fotosintesi artificiale utilizzando coloranti naturali che si trovano, ad esempio, nelle ciliegie (vedi Shallcross et al., 2009).
In futuro, un altro vero problema sarà rappresentato dalla necessità di avere un combustibile trasportabile pulito. L’idrogeno può essere generato indirettamente dall’energia solare attraverso l’elettrolisi dell’acqua, ma questa reazione è energeticamente dispendiosa. Di conseguenza numerose ricerche si stanno attualmente concentrando sulla possibilità di scindere l’acqua in idrogeno e ossigeno usando la luce solare in via diretta.
In quale altro modo chimica e luce contribuiscono a rendere il nostro pianeta pulito? Il diossido di titanio (TiO2) è un semiconduttore con interessanti proprietà fotochimiche. Esso è usato come pigmento bianco poiché diffonde efficacemente la luce solare. Inoltre assorbe i raggi UV. Quando è usato come pigmento o negli schermi solari per la sua capacità di assorbire gli UV, ciascuna particella è ricoperta di silice per impedire alla superficie libera di TiO2 di venire a contatto con l’ambiente circostante. Questo è necessario in quanto sotto la luce UV le particelle di TiO2 generano specie chimiche molto reattive che possono distruggere tutte le molecole complesse presenti nelle vicinanze. Questo apparente inconveniente del TiO2 non ricoperto è ora molto utile nella distruzione degli inquinanti, dato che quando la superficie libera di diossido di titanio è irradiata con luce UV in soluzione, essa distrugge completamente ogni composto organico nelle sue vicinanze. Come risultato, ogni inquinante organico presente è completamente mineralizzato in diossido di carbonio, acqua e ioni ammonio e cloruro.
Questi esempi mostrano che la chimica e la luce ci circondano – esse sono una parte importante del nostro mondo tecnologico e hanno un importante ruolo per un futuro più pulito e brillante!
Glossario
Chemiluminescenza: La generazione di luce direttamente da una reazione chimica, come accade nelle lucciole e nei lightstick chemiluminescenti.
Elettroluminescenza: La generazione diretta di luce dall’elettricità, ad esempio negli schermi dei telefoni cellulari.
Fluorescenza: L’emissione di luce associata ad una transizione elettronica da uno stato eccitato a uno stato di minore energia, durante la quale l’elettrone non cambia il suo spin. A causa di ciò l’emissione luminosa avviene molto velocemente dopo l’eccitazione, solitamente nel giro di pochi nanosecondi. Dunque, se la sorgente di eccitazione è rimossa, la fluorescenza cessa in pochi nanosecondi.
Luminescenza: Termine generale per indicare l’emissione di luce.
Fosforescenza: L’emissione di luce associata alla transizione da uno stato eccitato a uno stato di minore energia durante la quale l’elettrone cambia il suo spin. Questo permette all’emissione di luce di avvenire più lentamente, talvolta su una scala di secondi nelle molecole e in tempi spesso più lunghi nei vari tipi di fosforo allo stato solido. Quindi, se la sorgente di eccitazione è rimossa, la fosforescenza può ancora essere vista, come negli adesivi “brillanti nel buio” o nella luminosità rimanente del fosforo in un tubo fluorescente immediatamente dopo che la luce è stata spenta (quindi una volta che la fluorescenza è cessata).
Terapia fotodinamica: Una cura medica nella quale la luce è usata per distruggere cellule tumorali nel trattamento del cancro.
Fotopolimerizzazione: Il processo tramite il quale la luce è utilizzata per sintetizzare un polimero a partire da monomeri. La fotopolimerizzazione è usata per fissare pitture, inchiostri e sigillanti sensibili alla luce. I sigillanti fotoindurenti sono comunemente usati in odontoiatria.
Semiconduttore: Per gli scopi di questo articolo, la caratteristica importante di un semiconduttore consiste nella disposizione dei livelli energetici degli elettroni in due “bande”: una “banda di valenza” completa a bassa energia e una “banda di conduzione” vuota ad alta energia. L’eccitazione consente all’elettrone il passaggio dalla banda di valenza a quella di conduzione lasciandosi dietro un “buco”. Sia il buco che l’elettrone sono mobili e hanno la possibilità di migrare verso la superficie del semiconduttore, dove possono agire rispettivamente come ossidante e riducente nella distruzione degli inquinanti.
Il London International Youth Science Forum
Il presente articolo si basa su una lezione dimostrativa tenuta dal Dott. Peter Douglas e dal Dott. Mike Garley sulle applicazioni di chimica e luce nella vita quotidiana. La lezione si è svolta durante il London International Youth Science Forum del 2009 ed è stata seguita da 250 studenti provenienti da 40 nazioni.
Nel London International Youth Science Forum del 2010, il Dott. Douglas esplorerà i futuri sviluppi della scienza con eminenti scienziati, dignitari e innovatori industriali. Un elemento chiave del programma è l’opportunità di visitare siti industriali, centri di ricerca, istituzioni e organizzazioni scientifiche, comprese alcune istituzioni e laboratori di livello mondiale. Per ulteriori dettagli sulle modalità di partecipazione degli studenti, visitare il sito: www.liysf.org.uk
References
- Shallcross D et al. (2009) Looking to the heavens: climate change experiments. Science in School 12: 34-39. www.scienceinschool.org/2009/issue12/climate
Resources
- Per un confronto degli spettri di differenti sorgenti luminose – e per le istruzioni su come costruire un proprio spettometro, vedere:Westra MT (2007) A fresh look at light: build your own spectrometer. Science in School 4: 30-34. www.scienceinschool.org/2007/issue4/spectrometer
Review
La luce va ben al di là di ciò che possiamo vedere. La luce è usata in ogni aspetto della scienza, dall’illuminazione nel buio alla degradazione della plastica. Questo articolo dà una visione d’insieme dell’utilità pratica della luce e costituisce una lettura di base interessante per gli studenti che vogliono approfondire il concetto di luce come forma di energia.
Andrew Galea, Malta





