Van Gogh sötétedő öröksége Understand article
Fordította: Adorjánné Farkas Magdolna. Van Gogh festményein a ragyogó sárga szín csúnya barnára változik. Andrew Brown elmagyarázza, hogy a franciaországi Grenoble-ben működő European Synchrotron Radiation Facility (Európai Szinkrotron-sugárzási Létesítmény) által…
Vincent van Gogh’s (1853-1890) széles ecsetvonásokkal vitte fel a vászonra vibráló és gyakran valószerűtlen színeit, hogy ezáltal fejezze ki a hangulatát és az érzéseit. Ez lényeges eleme volt az ő egyedi stílusának és nagy hatást gyakorolt a modern festészet fejlődésére. A 19. században előállított újgenerációs színezékek lehetővé tették van Gogh számára, hogy kikeverje azokat a gyönyörű sárga színeket, amelyeket például a híres Napraforgók (Sunflowers) festményén is használt. Ezeknek a – sok alkotásán előforduló – megragadó színárnyalatoknak az előállításához használta az új pigmentet, amit krómsárgának neveznek. Sajnos, több mint 100 évvel azután, hogy Gogh letette az ecsetet, néhány festményen látható módon a krómsárga egyáltalán nem megragadó barnára sötétedett. Ez a jelenség felkeltette egy csoport tudós figyelmét.

A képet the Van Gogh Museum, Amsterdam szíves hozzájárulásával közöljük

A képet the Van Gogh Museum, Amsterdam szíves hozzájárulásával közöljük

A képet Acacia217 szíves hozzájárulásával közöljük; A kép forrása: Wikimedia Commons

A képet the Van Gogh Museum, Amsterdam szíves hozzájárulásával közöljük
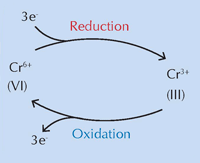
Egy nemzetközi kutatócsoport, amelyet Koen Janssens , a University of Antwerp, Belgium munkatársa vezet, arra a következtetésre jutott, hogy a krómsárga (PbCrO4 · xPbO), kémiai változása az ultraibolya (UV) fény hatására következik be. (Monico et al., 2011). Bevezetése óta tudják, hogy ez a pigment fény hatására sötétedik. Az 1950-es években elvégzett vizsgálatok kimutatták, hogy enek az az oka, hogy a Cr(VI) Cr(III)-má redukálódik (ld.: 1. ábra). Azonban mostanáig nem ismerték a pontos mechanizmust, és nem azonosították a keletkezett terméket.
A képet Nicola Graf szíves hozzájárulásával közöljük
Történelmi festék-tubusok
A rejtély megfejtését Janssens csoportja azzal kezdte, hogy festék-tubusokat gyűjtöttek be van Gogh kortársától, Rik Wouters (1882-1913) flamand festőtől. Néhány tubus tiszta krómsárga pigmentet, míg más tubusok fehér összetevővel kevert világosabb árnyalatú sárga festéket tartalmaztak. A kutatók a mintákat UV sugárzással mesterségesen öregítették, és azt várták, hogy a színek néhány hónap után változnak meg. Ehelyett – legnagyobb meglepetésükre – már kevesebb mint három hét múlva a világosabb árnyalatú sárga festék felszínén egy csokoládébarna réteg alakult ki. Ehhez képest a nem kevert festék csak egy kicsit vagy egyáltalán nem változott meg. “Nagyon meglepődtünk” – mondta Janssens.

Annak érdekében, hogy kiderítsék, hogy milyen végzetes kémiai reakció megy végbe, a csoport a festékmintát röntgensugár alkalmazásával alaposan megvizsgálta. A munka nagy része a franciaországi Grenoble-ben működő European Synchrotron Radiation Facility (ESRw1, Európai Szinkrotron-sugárzási Létesítményben) zajlott, ahol kétféle technikát, az XRF-t és a XANES-t használták arra, hogy különleges érzékenységgel detektálják a festékmintában a kiválasztott elemek térbeli eloszlását és oxidációs állapotát. (ld. a keretes írást).
Az elemzések kimutatták, hogy a pigment vékony felszíni rétegének sötétedése kapcsolatban lehet azzal, hogy a krómsárga festékben a Cr(VI) Cr(III)-á redukálódott. Ez összhangban van azzal, amit az ólom-kromát alapú ipari festékeknél figyeltek meg. Ráadásul, először sikerült kimutatni azt, hogy a Cr2O3 · 2H2O formában van jelen a tönkrement festékben. Ezt a vegyületet krómoxizöld festékként ismerik. De hogyan okozhatja egy zöld színű festék a megfigyelt barnulást? A tudósok azt gyanítják, hogy a krómoxizöldben jelenlévő redukált króm a festék olajtartalmának oxidációja során képződik. Az oxidálódott olaj, a zöld színű festék és a maradék sárga festék keveréke okozhatja a barna színt. , that may be the root of the brown colouration.
A röntgensugár technika alkalmazásával a kutatók ki tudták muattni, hogy a világosabb színű festékkeverék kénvegyületeket is tartalmaz. Arra a következtetésre jutottak, hogy ezeknek a vegyületeknek szerepük lehet a króm redukálásában. Ez magyarázza, hogy miért sötétedik kevésbé a nem kevert sárga festék.
A röntgensugár ráragyog van Gogh-ra

nagyobb méretű változatért
kattintson a képre
A képet the Van Gogh Museum,
Amsterdam szíves
hozzájárulásával közöljük
A tudósok elkülönített festékmintákban vizsgálják a lejátszódó kémiai reakciókat, ugyanis arra szeretnének választ kapni, hogy a két festményből – View of Arles with Irises (Arles látképe íriszekkel) (1888) és Bank of the Seine (Szajnapart) (1887) – nyert minták felszíni sárga rétege vajon ugyanolyan okok miatt sötétedett-e meg.
Az XRF spektroszkópiát használták arra, hogy feltérképezzék anak a területnek a kémiai tulajdonságait, ami összeköti a sötét felszíni réteget a változalan sárga festékréteggel. A XANES spektrumot ezeken a régiókon belüli pontokban vették fel. Az eredmények megerősítették a régebbi kísérletek eredményét: a sötétebb felszíni rétegben kimutatták a króm redukált formáját, a Cr(III)-at, ebből arra lehet következtetni, hogy ennek a jelenléte a felelős a barna színért. Továbbá azt találták, hogy a Cr(III) egyenlőtlenül oszlott el, azokon a helyeken volt jelen, ahol a festék szulfát- és báriumvegyületeket tartalmazott.
A kémiai vizsgálatok megerősítették az előző kísérletből levont következtetést, miszerint a kénvegyületeknek szerepük van a króm redukciójában (ld. az alábbi egyenletet). Van Gogh a kénvegyületeket tartalmazó port fehér színe miatt keverte a krómsárgához, hogy világosabb árnyalatot kapjon. Életének egy szakaszában ezzel a keverékkel a fényesen megvilágított helyeket festette meg.
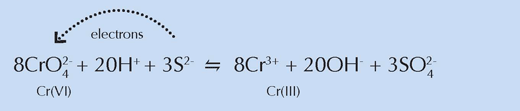
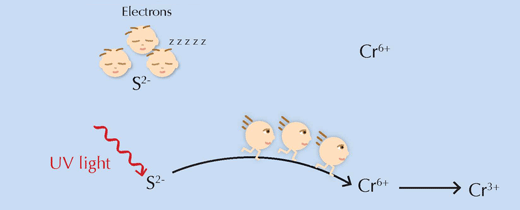
Már csupán egyetlen fontos kérdés maradt: hogyan segíti elő az UV sugárzás a reakciót? A válasz meglehetősen egyszerű: energiát biztosít, amely fedezi a reakcióban az aktiválási energiát, ezzel lehetővé teszi, hogy végbemenjen a reakció (ld. alább a 6. ábrát).
A képet Nicola Graf szíves hozzájárulásával közöljük
Mit lehet tenni?
Janssens csoportja kiderítette a van Gogh festményein használt festék sötétedésének kémiai hátterét. A kérdés azonban az, hogy fel tudjuk-e használni ezt a tudást a művész munkáinak megmentésére? Ella Hendriks, az amszterdami Van Gogh Museumw3 munkatársa kételkedik ebben: “A modern múzeumokban már kiszűrik az ultraibolya fényt. A festményeket kontrollált körülmények között tartjuk, így biztosítjuk a számukra a legjobb feltételeket.” Ezek közé tartozik az alacsony hőmérséklet is. Általános szabályként fogadják el, hogyha a hőmérséklet 10 ºC-kal emelkedik, akkor a kémiai reakciók sebessége 2-4-szeresére nő, és ez alól a króm redukciója sem kivétel.
Ha már az UV sugárzás mértékét és a hőmérsékletet is megfelelően szabályoztuk, akkor még mi mást tehetnénk van Gogh festményeiért? Létezik egy radikálisabb lehetőség: ahelyett, hogy csupán lassítjuk a festék sötétedésének folyamatát, törekedjünk arra, hogy teljesen megfordítsuk azt. “A következő kísérletünk már folyamatban van” – mondja Janssens – “valójában azt szeretnénk megtudni, hogy milyen körülmények a felelősek a króm redukciójáé rt, és van-e remény arra, hogy a festékben visszaalakítsuk az eredeti oxidációs állapotot.”w4
Bár az nagyszerű megoldás lenne, ha ilyen módon vissza tudnánk fordítani az idő kerekét, Janssens azonban elismerte, hogy jelenleg meglehetősen elképzelhetetlen, hogy visszanyerjük a megváltozott festék eredeti színét. Ennek ellenére a tudósok munkája megerősíti azt a reményünket, hogy többet tehetünk van Gogh festményeinek megőrzése érdekében, hogy a következő generációk is gyönyörködhessenek e nagy művész alkotásaiban.
Művészeti alkotások tanulmányozása szinkrotronnal
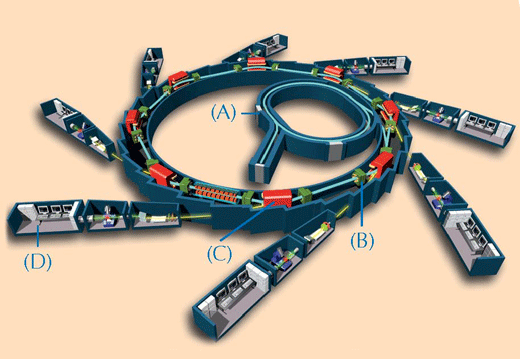
A mesterművek kémiai vizsgálata komoly probléma. Az analízishez csupán nagyon kis mennyiségű mintát lehet venni, és ezek gyakran sokféle vegyület keverékét tartalmazzák heterogén anyagi rendszerben. A nehézségek megoldására a tudósok a röntgensugárzáson alapuló tecnikákat használják. Minél erősebb és pontosabb a röntgensugár, annál jobb minőségű elemzést lehet végezni. Erre a célra a leginkább alkalmas röntgensugárzást a szinkrotron sugárforrásokw2 (ld. alább a 2. ábrát) biztosítják. Ebben a kísérletben kétféle spektroszkópiai módszert alkalmaztak a festék vizsgálatára az ESRF-ben, ezek: az XRF és a XANES.
A képet EPSIM 3D / JF Santarelli, Synchrotron Soleil szíves hozzájárulásával közöljük; a kép forrása: Wikimedia Commons
XANES
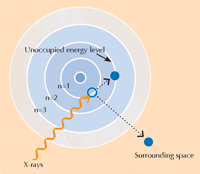
A XANES spektroszkópia a röntgensugár elnyelés fizikáján alapul. Egy adott elem atomjai az elemre jellemző módon nyelik el a röntgensugárzást. Ezért az elnyelési spektrum alapján azonosítani lehet a mintát felépítő elemeket. A vízszintes tengelyen a sugárzás energiáját ábrázolják, a függőleges tengelyen az abszorpció mértékét. A nagyfelbontású röntgensugár abszorpciós spektrumot általában egy olyan energia-tartományban veszik fel, amely közel van a kérdéses elem egyik abszorpciós éléhez (ld. alább a 3. és a 4. ábrát). Az ilyen részletgazdag spektrum azt is meg tudja mutatni, hogy a vizsgált elem milyen oxidációs állapotban van. Ez az információ a kutatók körében nagy érdeklődésre tarthat számot.
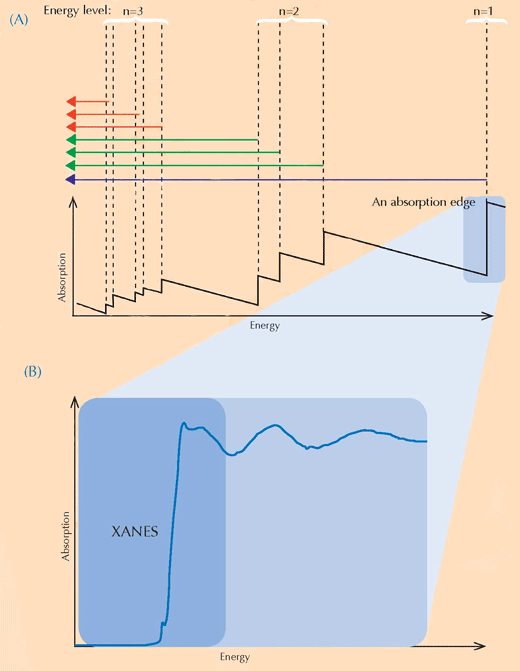
A képet Atenderhold szíves hozzájárulásával közöljük; a kép forrása: Wikimedia Commons (B) Egy abszorpciós él részletesen. Ha egy simának látszó abszorpciós élt kinagyítva megnézünk, akkor feltűnnek kisebb kiemelkedések, amelyek kisebb mértékű abszorpciónak felelnek meg. Azt a régiót, amely az abszorpciós él vezető élének közelében van, röntgenabszorpciós spektrumélközeli szerkezetként (XANES, kék téglalapba foglalva) emlegetik, és megfelel egy elektronátmenetnek egy közeli energiaszintre. A kutatók a XANES régiót használják van Gogh festményeinek elemzésére, mivel ez információt ad a mintában lévő atomok oxidációs állapotáról: azok az atomok,amelyek különböző oxidációs állapotban lehetnek, eltérő számú elektront tartalmazhatnak (ld. feljebb az 1. ábrát). Ez módosítja az energiaszinteket és azért a XANES spektrumot.
A képet M Blank szíves hozzájárulásával közöljük: a kép forrása; Wikimedia Commons
A képet Nicola Graf szíves hozzájárulásával közöljük
XRF
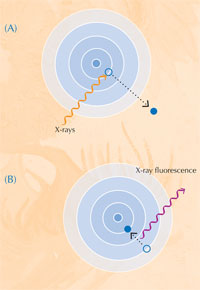
Amikor egy atom röntgensugárzást nyel el, akkor kevésbé stabil gerjesztett állapotba kerül. Amikor visszajut a stabilabb állapotba, másodlagos röntgensugárzást bocsát ki, ezt a jelenséget röntgen-fluoreszcenciának (XRF) nevezik (ld. az 5. ábrát). Egy vizsgált minta által kibocsátott XFR spektrumot arra lehet felhasználni, hogy feltérképezzék vele egy kiválasztott területen az elemek eloszlását. Ezzel szemben a XANES csak a minta egy pontjáról ad információt. Az XRF és a XANES módszerekkel szerzett információk segítségével a szerzők részletes képet kaptak a festékminta kémiai állapotáról.
A képet Nicola Graf szíves hozzájárulásával közöljük
Tudomány a képzőművészetben
Mit gondol Ön és tanítványai? A tudomány segítségével meg tudjuk-e állítani a fontos képzőművészeti alkotások pusztulását, vagy vissza tudjuk-e állítani eredeti állapotukat? Vagy el kell fogadnunk, sőt történeti bizonyítékként kell értékelnünk a romlást?
References
-
Monico L et al. (2011) Degradation process of lead chromate in paintings by Vincent van Gogh studied by means of synchrotron X-ray spectromicroscopy and related methods. 2. Original paint layer samples. Analytical Chemistry 83: 1224-1231. doi: 10.1021/ac1025122
Web References
- w1 – A European Synchrotron Radiation Facility (ESRF, Európai Szinkrotronsugárzási Létesítmény), egy nemzetközi kutatóintézet, amely élen jár a fotonokkal kapcsolatos kutatásokban. Az ESRF az EIROforum tagja, amely a Science in School folyóiratot kiadja. Többet megtudhat róla: www.esrf.eu
- w2 – További részleteket megtudhat arról, hogy hogyan használják a szinkrotronsugárzást a kutatásban, ld.:
- Capellas M, Cornuéjols D (2006) Shipwreck: science to the rescue! Science in School 1: 26-29.
- Capellas M (2007) Pompeji freskóinak restaurálása. Science in School 6.
- w3 – Ha többet meg akar tudni Vincent van Gogh-ról és művészetéről, látogasson el a Van Gogh Museum nagyszerű weboldalára: www.vangoghmuseum.nl
- A múzeum weboldalának egyik szekciója általános- és középiskolai oktatási anyagokat is tartalmaz: www.vangoghmuseum.nl/vgm/index.jsp?page=110&lang=en
- w4 – Meghallgathatja a Koen Janssens-nel készült beszélgetést van Gogh festészetéről a BBC Radio 4 adón: www.bbc.co.uk/programmes/b00yjs49
- w5 – CLEAPSS egy UK-ban létrehozott tanácsadó szervezet, amely támogatja a természettudományos és műszaki oktatást a következő témakörökben: egészség és biztonság; kockázat-becslés; a vegyszerek, élő szervezetek és eszközök felhasználása. További információért ld.: www.cleapss.org.uk
- Az ólom, a króm és vegyületeik biztonságos használatához olvassa el a tanulói biztonsági adatlapokat, amelyeket ingyen letölthet innen: http://www.cleapss.org.uk/free-publications/general-publications
Resources
- Képek és a kiemelkedő művekből vett festékminták elemzéséről készült animációk találhatók: www.vangogh.ua.ac.be
- Többet megtudhat a képzőművészeti alkotások megőrzésének tudományáról:
- Leigh V (2009) The science of preserving art. Science in School 12: 70-75.
Institutions
Review
Ez a cikk nagyszerűen összekapcsolja a tudományt a művészettel és a konzerválási eljárásokkal. A fejlett technika segítségével kutatják azokat a kémiai folyamatokat, amelyek a van Gogh által évtizedekkel ezelőtt használt pigmentekben lejátszódik.
A cikk jó példát ad arra, hogy megmutassa, hogy mindig van természettudományos magyarázat az idők során a művekben bekövetkező változásokra. A cikket főként a kémiaórákon lehet felhasználni a 16-18 éves korosztály számára, leginkább az oxidáció-redukció témakörnél.
A tanulók jobban megérthetik a kutatás kémiai tartalmát, ha válaszolnak a következő kérdésekre:
- A cikkben leírt tudományos munka feltárta, hogy a króm redukciójáért valószínűleg a szulfidionok a felelősek. Írják le azoknak a folyamatoknak a kémiai egyenleteit, amelyekben az ólom-kromátot (PbCrO4) a H2S -ben illetve a PbS -ben lévő szulfidion redukálja. Vegyék figyelembe, hogy a Cr(VI)-ot tartalmazó vegyületek az oxidálószerek.
- A tudósok feltételezik, hogy a van Gogh által használt festékben található szulfátokból keletkezhetnek a szulfidionok. Próbálják meg kitalálni, hogy a festék milyen más módon lehet kitéve a szulfidionok hatásának.
- Az ezüstékszerek egy idő után megsötétednek, ha a levegővel érintkeznek. Írják fel annak a reakciónak az egyenletét, amely felelős ezért. Figyeljenek arra, hogy ez nem egy egyszerű helyettesítési reakció!
Az osztályban a következő kísérlettel lehet megmutatni, hogy az ólom-kromát sötétebbé válik, ha szulfidionokkal lép reakcióba:
- Állítsanak elő ólom-kromátot: egy főzőpohárban valamilyen vízben oldódó ólom-sóhoz, például ólom(II)-acetáthoz Pb(CH3COO)2, vagy ólom-nitráthoz, Pb(NO3)2, öntsenek azonos térfogatú kálium-kromát, K2CrO4. oldatot. Hígítsák az oldatokat ~ 0,03 M-osra.
- Azonnal sárga ólom-kromát csapadék keletkezik. Egy tölcsérbe helyezett szűrőpapíron öntsék keresztül a megmaradt folyadékot. Elszívó fülkében óvatosan szárítsák a csapadékot levegő befúvásával, de ne szárítsák meg teljesen.
- Készítsenek hidrogén-szulfid (H2S) oldatot úgy, hogy 50 mg nátrium-szulfidot (Na2S) 90 ml vízben feloldanak, és az oldathoz 10 ml sósavat (HCl, 0,1 M) öntenek, majd összekeverik.
- Fújjanak levegőt egy léggömbbe, és húzzák rá egy kisméretű üveg Drechsel-féle gázmosóra, amelyben néhány mililiter hidrogén-szulfid oldat van (ld. az alábbi ábrát). Engedjék rá a hidrogén-szulfid tartalmú levegő-áramot az ólom-kromát csapadék felszínére.
- A csapadék azonnal megbarnul. Elősegítették és felgyorsították azt a folyamatot, ami a van Gogh által használt festékek sötétedését okozza.

A képet Vladimir Petruševski szíves hozzájárulásával közöljük
Biztonsági megjegyzések: minden vízben oldódó ólom-só és minden kromát mérgező (0,003 M-nál nagyobb koncentrációban), és azt is feltételezik, hogy rákkeltőek. A kálium-kromát irritációt és / vagy fekélyt okozhat, ha a bőrrel érintkezik. Egy kevés bizonyíték amellett is szól, hogy az ólom-kromát rákkeltő. Káros lehet a még meg nem született magzatra, így ne használják, ha a tanár vagy a diákok közül valaki terhes lehet. A kén-hidrogén mérgező, kellemetlen szagú gáz.
A következő kísérletet vegyi fülke alatt végezzék el, és viseljenek védőszemüveget és védőkesztyűt. Minden vegyszert a helyben érvényes rendszabályok szerint kezeljenek. Nézzék meg a Science in School általános biztonsági előírásait is. Hasznos lehet, ha elolvassák a króm és az ólom CLEAPSS tanulói biztonsági adatlapjaitw5.
Vladimir Petruševski, Volt Jugoszláv Köztársaság Macedónia





