Les reaccions redox a les cèl·lules: la química de la vida Understand article
Traduït per Mireia Güell. Apreneu com els biosensors fluorescents poden monitoritzar la química de l’interior de les cèl·lules vives.
Tendim a pensar en les reaccions de reducció i oxidació (redox) com a química pura. No obstant això, en les cèl·lules vives la reducció és només un guany d’electrons i l’oxidació és una pèrdua d’electrons. Les reaccions redox tenen un paper important en una àmplia gamma de processos bioquímics. Els desequilibris en reaccions redox cel·lulars intervenen en diverses malalties, per tant, mantenir l’equilibri en aquestes reaccions és fonamental per la nostra salut.
Considereu les següents semireaccions:
C ⇌ C4+ +4e–
O2+4e– ⇌ 2O2-
En una, el carboni s’oxida, i en l’altra l’oxigen es redueix. Juntes, les dues equacions descriuen una reacció redox que sembla química senzilla. No obstant això, aquesta reacció es produeix en els nostres cossos contínuament.
Green fluorescent protein
(GFP) from the jellyfish
Aequorea victoria.
Image courtesy of Protein Data
Bank (PDB ID: 1GFL)
Una reacció redox típica
En les reaccions redox, els electrons es transfereixen entre dues espècies químiques. Per exemple, en la reacció explosiva de la termita, que de vegades s’utilitza per soldar vies fèrries, els electrons es transfereixen de l’alumini metàl·lic a l’òxid fèrric:
Fe2O3(s) + 2Al(s) → Al2O3(s) + 2Fe(l)
Aquest canvi es veu millor si eliminem els àtoms d’oxigen de l’equació:
2Fe3+ + 2Al → 2Al3+ + 2Fe
Podem veure que els àtoms d’alumini perden electrons (s’oxiden) i que els electrons es transfereixen als ions de ferro de l’òxid fèrric reduint-los. En principi, totes les reaccions redox consisteixen en dues semireaccions: la semireacció d’oxidació (en aquest cas el parell Al/Al3+) i la semireacció de reducció (aquí el parell Fe3+/Fe).
Les redox biològiques
Metabolisme
La reacció de la termita mostra que les reaccions redox espontànies poden alliberar energia, que pot ser útil en el cos. Les dues semireaccions del començament de l’article són en realitat només una manera diferent de descriure el metabolisme cel·lular. Quan mengem, el menjar es descompon en sucres com la glucosa. Dins de la cèl·lula, aquests sucres s’oxiden, transferint electrons a O2. Una manera alternativa d’escriure l’equació és:
C6H12O6(s) + 6O2(g) → 6CO2(g) + 6H2O(l) + energia
En aquesta equació, 48 electrons es transfereixen des dels àtoms de carboni del sucre als àtoms d’oxigen, alliberant energia per impulsar més reaccions redox en el procés. Mantenir l’equilibri en aquestes reaccions és fonamental per la funció cel·lular normal; si l’equilibri es desplaça massa en un o altre sentit de la reacció, hi pot haver conseqüències no desitjades, com per exemple una malaltia.
Imatge cortesia de Prince S. Amponsah (DKFZ Heidelberg)
La comunicació cel·lular
Durant molt de temps les molècules químicament reactives que contenien oxigen, conegudes com a espècies reactives d’oxigen (ROS), que poden alterar l’estat redox d’una cèl·lula, s’havien considerat com a subproductes no desitjables i nocius del metabolisme cel·lular. Normalment, el citoplasma de les cèl·lules es troba en un estat reduït; un canvi cap a un estat més oxidat ha estat vinculat a diverses malalties, incloent el cancerw1.
No obstant això, algunes ROS també tenen papers beneficiosos com el de molècules de senyalització i són, per tant, essencials per la salut dels organismes. Milers de molècules diferents de ROS s’utilitzen com a senyals missatgers per permetre les cèl·lules comunicar-se. Alguns exemples són el superòxid (O2–), el peròxid d’hidrogen (H2O2) i l’òxid nítric (NO.), que normalment es produeixen de manera controlada i tenen papers en processos com el guariment de ferides, l’envelliment, la inflamació i la mort programada de les cèl·lules (apoptosis).
Les redox i el càncer
En el càncer, les cèl·lules es divideixen de manera incontrolable i les proteïnes es comporten de manera estranya, com per exemple apareixent i desapareixen de manera inesperada. Les reaccions redox han estat implicades en la formació del càncer, per exemple malmetent el nostre ADN, i es creu que les ROS activen l’expressió de proteïnes de gens que promouen el càncer (oncògenes) o bé desactiven els gens supressors dels tumors, les proteïnes de les quals fan el contrari. Les ROS també poden oxidar proteïnes, alterant directament la seva estructura i, per tant, la seva funció. Si aquestes proteïnes són importants per la divisió cel·lular o el moviment de les cèl·lules, llavors el càncer podria aparèixer.
Un cop el tumor s’ha desenvolupat, els mecanismes redox es poden aprofitar en el tractament. Molts medicaments contra el càncer ataquen els tumors incrementant la producció de les ROS dins les cèl·lules malignes, la qual cosa finalment les mata. No obstant això, les cèl·lules cancerígenes generalment incrementen la producció dels seus sistemes de defensa antioxidants, contrarestant aquest efecte.
Els mecanismes redox també poden ser responsables de la resistència a la teràpia, quan els tractaments mèdics disponibles no funcionen. Per atacar els tumor de manera eficient, aquests medicaments utilitzen les proteïnes de transport del cos per arribar la ubicació desitjada (per exemple on es troben les cèl·lules malignes). No obstant això, les reaccions redox poden alterar aquestes proteïnes, convertint-les en no-funcionals i interferint en la teràpia.
Aquestes són només algunes de les raons per les quals entendre les reaccions redox biològiques i com les cèl·lules assoleixen l’equilibri redox pot ajudar en la lluita contra el càncer.
Imatge cortesia de Prince S. Amponsah (DKFZ Heidelberg)
Aportant llum les reaccions redox
Per entendre com funcionen els diferents factors que interactuen en les cèl·lules sanes i les malaltes, podem visualitzar els processos redox en les cèl·lules utilitzant versions d’una proteïna d’una medusa fluorescent coneguda com a proteïna fluorescent verda (GFP). Durant les dècades del 1960 i el 1970, investigadors van descobrir la GFP en la medusa Aequorea victoria i la van modifica perquè produís diferents colors. Més tard, aquest treball va ser premiat amb el Premi Nobel de Químicaw2.
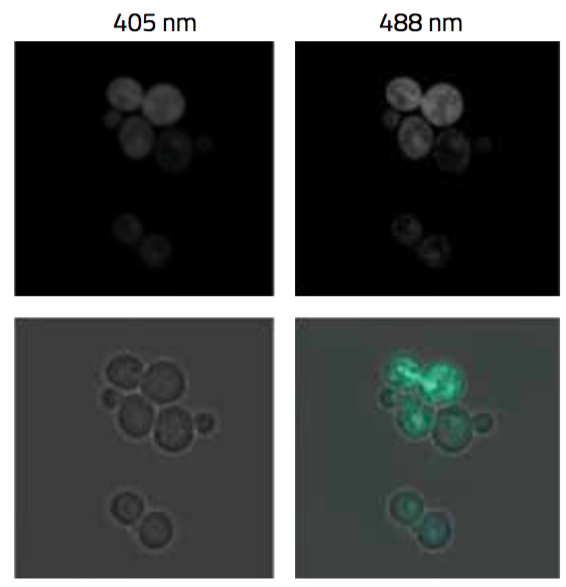
Utilitzant la genètica, podem crear cèl·lules que produeixen biosensors fluorescents basats en la GFP per utilitzar-los en el seguiment dels estats redox de les cèl·lules. Un dels biosensors és una variant de la GFP anomenat roGFP2, que pot ser modificat amb diferents segments de proteïna per assolir objectius específics. Per exemple, pot ser dirigit a localitzacions específiques en la cèl·lula (per exemple el citosol o els mitocondris) mitjançant l’addició de seqüències de trànsit (figura 1). Alternativament, es pot generar un biosensor especialitzat per una molècula redox concreta afegint un segment de proteïna que reaccioni amb espècies redox.
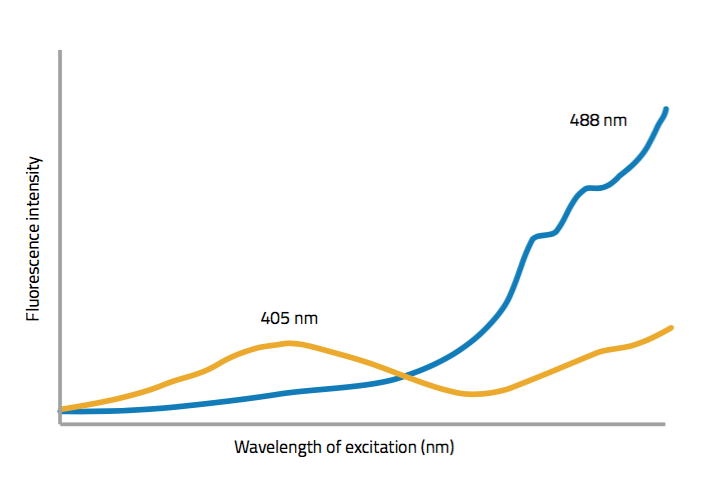
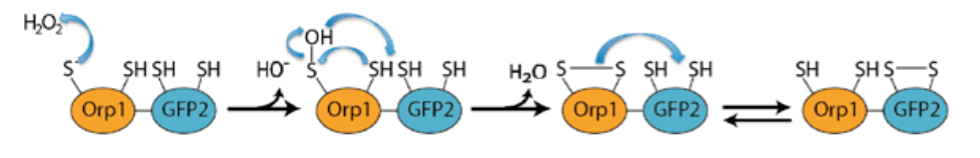
Per mesurar els nivells de H2O2 en les cèl·lules, utilitzem el sensor Orp1-roGFP2 (figura 2). El sulfur de la part Orp 1 del biosensor reacciona amb el peròxid i la proteïna s’oxida, creant ponts disulfúrics que canvien la forma de la proteïna i, així, redueixen la seva fluorescència en el rang de la mesura (figura 3).
Utilitzant aquestes proteïnes GFP modificades, podem veure en temps real per on viatgen les espècies redox i com influencien o mantenen l’estat redox, tant en els individus sans com en els pacients amb càncer. Això pot ajudar-nos a entendre la dinàmica de les nostres cèl·lules quan estem sans i si desenvolupem càncer. Potser un dia podrem utilitzar els nostres descobriments per suggerir nous tractament per la malaltia.
Web References
- w1 – El grup del professor Tobias Dick al German Cancer Research Center (DKFZ) investiga la regulació redox en cèl·lules sanes i cancerígenes. Per llegir més sobre la seva recerca, vegeu: www.dkfz.de/en/redoxregulation/index.php
- w2 – Més informació sobre el Premi Nobel de Química 2008 pel descobriment i el desenvolupament de la GFP està disponible a la web dels Premis Nobel. Vegeu: http://tinyurl.com/7y8df4s
Resources
- Més sobre la GFP es pot trobar at:
- Furtado S (2009) Painting life green: GFP. Science in School 12: 19–23.
- Per saber-ne més sobre les reaccions químiques redox, visiteu: http://tinyurl.com/d65vdx6
- Per una activitat sobre els gens implicats en el càncer, vegeu:
- Communication and Public Engagement team (2010) Can you spot a cancer mutation? Science in School 16: 39-44.
Review
Conèixer les reaccions redox que es produeixen en les cèl·lules vives és important per entendre molts mecanismes cel·lulars com per exemple l’envelliment, la inflamació, l’apoptosi i el càncer.
Aquest article descriu com biosensors, alguns dels quals estan basats en la GFP, poden ser utilitzats per detectar el nivell de les espècies químiques que participen en les reaccions redox i, per tant, per entendre la dinàmica de les nostres cèl·lules.
Aquest article pot ser utilitzat per explicar tècniques de laboratori usades en biologia molecular així com per donar la baser per discutir sobre el paper dels antioxidants i la utilització de la GFP en biologia. Preguntes de comprensió sobre l’article podrien ser:
- En la respiració cel·lular, quin element s’oxida i quin element es redueix?
- Demostreu com 48 electrons s’intercanvien en la respiració cel·lular.
- Què són les espècies reactives d’oxigen?
- Descrigueu els papers del superòxid, el peròxid d’hidrogen i l’òxid nítric en la cèl·lula.
- Descrigueu com les espècies reactives d’oxigen es poden utilitzar en la teràpia contra el càncer.
Monica Menesini, Liceo Scientifico A Vallisneri, Itàlia





