Kromozomların patlaması: kanser nasıl başlar Understand article
Tercüme eden: Canbolat Gürses ve Hikmet Geçkil (İnönü Üniversitesi, Moleküler Biyoloji ve Genetik Bölümü). Beyin tümörleri çocuklarda en çok görülen genel ölüm nedenlerinden biri olup hücre bölünmesi sırasında kromozomlar ayrıldığı zaman başlayabilir.
mutasyonun kanserle
bağlantılı kromozomal
‘patlamalara’ neden olduğu
görülüyor
EMBL / P Riedinger izniyle
Bu birçok evde görülen bir sahnedir. Endişeli bakışlarla gözleri dört açılmış çocuk en sevilen kolyesinin kalan parçalarını tutarken, tüm aile bireyleri elleri ve dizleri üzerinde dağılan renkli boncukları bulmaya çalışır.
Boncukların çoğu toplandıktan sonra bir yetişkin nazikçe onları yeni bir ipe dizer ve böylece kriz sona erer. Çocuk, orijinal kolyenin birebir kopyasından daha azıyla ebetteki tatmin olmayacaktır. Koltuk altına ya da dolap arkasına yuvarlananlar da dahil tüm boncukları bulmak ve onları doğru sırada yeniden dizmek ince bir iştir.

iStockphoto
Almanya’daki Heidelberg Üniversite Hastanesinden, Andreas Kulozik çok daha ciddi bir probleme sahip bir aileyle karşılaştı. Küçük bir kız ve erkek kardeşi oldukça agresif tümörler geliştirmişlerdi. Başlangıçtaki genetik testlerde Andreas, kardeşlerin TP53 geninde aynı mutasyona sahip olduklarını buldu. Ancak, bu mutasyonun tüm hücrelerde bulunması, çocukların onu sonradan edinmediğini ancak ebeveynlerinden kalıtıldığını gösteriyordu.
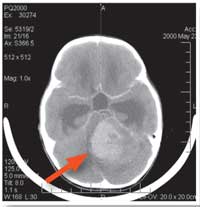
taraması (oka bakınız) altı
yaşındaki bir kızın
beynindeki bir
medulablastomayı gösteriyor
Reytan’ın izniyle; resim
kaynağı: Wikimedia Commons
Avrupa Moleküler Biyoloji Laboratuvarı’ndanw1Jan Korbel, Alman Kanser Araştırma Merkezi’ndenw2 Stefan Pfister ve Peter Lichter’in çocuk beyin tümörlerinin genetiği üzerine olan işbirliklerinde bu aile iyi bir başlama noktası oluşturabilirdi. Uluslararası Kanser Genom Konsorsiyumunun bir parçası olarak Jan, Stefan ve Peter çocuk tümör hücrelerinin tüm genomunu ilk kez diziliyorlardı. Meduloblastoma olarak adlandırılan bu kanser türü, pediyatride en yaygın rastlananı ve en ölümcül olanı olup, gelişmiş ülkelerde araba kazalarından sonra çocuklarda ikinci en yaygın ölüm sebebidir.

resim kaynağı Flickr
Jan’ın araştırma grubunda veri analizlerinden sorumlu Tobias Rausch “DNA dizi bilgisini elde ettiğimizde kız çocuğunun genomunda ilk başta gerçekten açıklayamadığımız bir kaos gördük” diyor. “Ondan sonra başka bir grubun yeni keşfettiği ve kromotripsis, adını verdikleri bir fenomeni ortaya koyan yayınlarını gördük,” diye ekliyor grup arkadaşlarından Adrian Stütz.
Bu bilim adamları da kırılan kolye senaryosunun hücresel dengi olan kromotripsis’i gördüklerini fark ettiler: bir kromozom (bazen iki) bir sebepten sayısız küçük parçalara ayrılıyordu ve daha sonra bazı parçalar kayboluyor diğerleri de yanlış sırayla tekrar bir araya geliyordu. Bilim adamları daha çok örneği analiz ettiklerinde, bu durumun kalıtılan TP53 mutasyonu taşıyan tüm medulablastoma hastalarının kanserli dokularında olduğunu gördüler. Ancak, normal TP53 taşıyan hastaların hiçbirinde veya medulablastomalı hastaların sağlıklı dokularında bu durum görülmüyordu.
“Bu durum, bize üç olayın bağlantılı olabileceği fikrini verdi,” diyor Jan. “Bir TP53 mutasyonunun kromozomların patlamasına yol açabileceğini veya hücrenin uygun bir cevap vermesini engellediğini düşünüyoruz. Bu daha sonra nasıl oluyorsa oldukça agresif kanser formuna yol açmaktadır.”
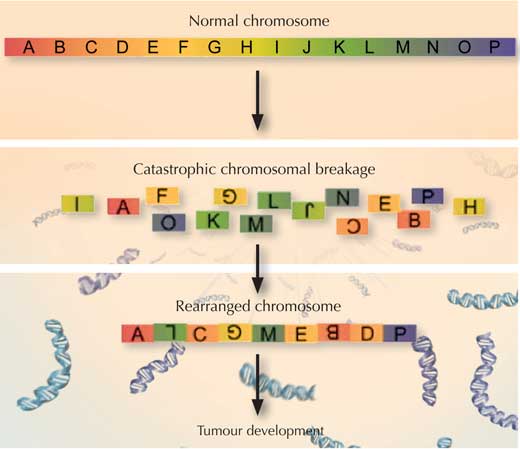
Böylece TP53’teki bir mutasyon nasıl oluyor da kromozomların patlamasına ve sonuçta bu durum kansere yol açıyor? Bilim adamları TP53’ün telomerleri koruyarak kromozomların aşınmasının engellenmesine yardımcı olduğunu biliyorlar. Telomerler kromozomların sonunu birlikte tutan şapkalardır. Eğer TP53 hatalı olursa, Jan ve çalışma arkadaşlarının tahminlerine göre, telomerler bozulabilir ve kromozomlar birbirine yapışabilir.
Böyle bir senaryoda, hücre bölünmeye başladığı zaman birbirine yapışmış kromozomlar problemlerle karşılaşabilir. Kromozomlar zıt yönlerde çekilecektir. Boncuk kolyenin çok sert çekilmesi gibi, belli bir noktada gerilim çok fazla olacak ve kromozomlardan biri ya da her ikisi kırılacak ve DNA parçaları ortamda uçuşmaya başlayacaktır. Hücrenin tamir mekanizması kromozomları tekrar bir araya getirmeye çalışırken, genetik materyalin bazı parçaları dışarıda bırakılabilir ve diğerleri yeniden düzenlenirken yanlış yerlere ve hatta yanlış kromozoma eklenebilir.

kaynağı: Wikimedia Commons
Öte yandan TP53, zarar gören DNA’mız için bir anahtar rol de oynar. Eğer bu genom koruyucusu pek çok hata bulursa, hücreleri programlı hücre ölümüne (apoptoz) veya hücresel yaşlanmaya (senesens) zorlar. Böylece, bu tamir edilemeyecek derecede hasarlı hücrenin bölünmesi ve genetik kusurlarını yeni hücrelere geçirmesi engellenmiş olur.
Ancak, TP53’te mutasyon varsa, kromozomun patlamasına TP53 yol açmış olsun veya olmasın kromotripsis gibi kromozomun yanlış biçimde yeniden düzenlendiği durumlar fark edilmeyebilir. Sonuç olarak, kansere yol açan genler olan onkogenler aktive olup hücryi kontrolsüz bölünmeye sürükleyebilir ve böylece bir tümör oluşabilir. Jan, Stefan ve Peter hasarlı bir TP53’ün etkilerinin bir arada kansere nasıl yol açtığını her basamakta anlamaya çalışmaktadır.
Bu arada, onların bulguları Andreas ve Stefan gibi klinisyenler ve hastaları için yankı da bulmaktadır. “Eğer bir hastanın tümör hücreleri kromotripsis işaretleri gösteriyorsa bir kalıtılmış TP53 mutasyonuna bakmamız gerektiğini biliyoruz” diyor Stefan. Bu önemlidir. Çünkü kalıtılmış bir TP53 mutasyonuna sahip olmak kullanılan çoğu kanser tedavisinin geri tepmesine neden olabilir. Çoğu kemo ve radyoterapi tedavileri kanser hücrelerinin DNA’larına zarar vererek onları öldürür fakat bu tür yaklaşımlar vücuttaki diğer normal hücreleri de etkiler. Çoğu hastada bu durum her ne kadar ağrılı yan etkilere yol açabilse de, uzun vadede fazla bir zarar görülmez. Ancak bu durum TP53 mutasyonlu bir hasta için geçerli değildir. Cünkü bu mutasyon nedeniyle kişinin sağlıklı olanları da dahil olmak üzere tüm hücreleri DNA hasarına karşı koymada sorun yaşayacaktır.
DNA’yı hedefleyen böyle tedaviler aslında sağlıklı hücreleri kansere çevirebilir ve sekonder ve tersiyer tümörler denilen “kalıtılmış TP53 mutasyonlu hastalarda sıklıkla görülen şeylere yol açabilir” diyor Stefan. Böyle hastalarda DNA’ya daha az hasar veren ajanlar kullanarak daha az yoğun tedaviler tercih edilir. Eğer bir hasta kalıtlanmış bir TP53 mutasyonu içeriyorsa, bu acilen o kişinin ailesinin de test edilmesini gösterir. Eğer herhangi bir aile bireyi mutasyonu taşıyorsa, hayatlarının bir noktasında tümör gelişimi olasılığı yüksek olduğundan, düzenli tarama yapılması gerekir. “Kromotripsisle ilişkili görülen agresif ve erken evreli kanser türlerindeki kanserle savaşın en iyi yolu erken teşhis edilmesidir” diyor Jan.
Aslında bilim adamları tüm kanser türlerinin % 2-3’ünün muhtemelen kromotripsisden kaynaklandığını düşünüyorlar böylece Jan’ın grubu şu anda TP53 mutasyonlarının medullablastoma yanında diğer tümörlerdeki benzer kromozom patlamalarında bir rol oynayıp oynamadığını araştırıyorlar. Akut miyeloid lösemide kalıtlanmış TP53 mutasyonları ve kromotripsis arasında aynı bağlantıyı gösteren kanıtlar buldular. Yetişkinlerdeki bu agresif türdeki kan kanserinde, Jan ve çalışma arkadaşları kalıtsal olmayan TP53 mutasyonu (yani TP53 mutasyonunu sadece tümör hücrelerinde içerenler) ve kromotripsisin eğiliminin yaşlılarda daha fazla olduğunu keşfettiler. Bilim adamları, TP53’ün telomer bütünlüğündeki görevi göz önüne alındığında bunun anlamlı olduğuna işaret ediyorlar. Yaşlandıkça kromozomlarımızın uçları doğal olarak kısalır ve eğer TP53’te bir terslik olursa bu durum kromozom uçlarının birbirine yapışmasına neden olabilir. Bu da bilim adamlarının düşündüğü gibi kromotripsise ve sonuçta kansere sebep olur.
Jan’in grubu bu durumu beyin, kan ve diğer kanserlerde araştırmaya ve TP53’ün hatalı türlerinin kırılan kolye gibi kromozomal patlamayla nasıl ilişkili olduğunun yanı sıra kansere katılan hücre içi diğer etkilerin neler olduğunu keşfetmeye devam ediyor.
EMBL hakkında

Avrupa Moleküler Biyoloji Laboratuar’ı (EMBL)w1dünyanın en üst seviyedeki araştırma enstitülerinden biri olup, kendini yaşam bilimlerinde temel araştırmalara adamıştır. EMBL uluslararası, yenilikçi ve disiplinler arasıdır. Enstitünün 60 ülkeden çalışanı biyoloji, fizik, kimya ve bilgisayar bilimi birikimine sahip olup, moleküler biyolojiyi geniş bir yelpazede çalışan araştırma işbirliği gerçekleştiriyorlar.
EMBL, Science in School’un yayımcısı olan EIROforumw3‘un bir üyesidir.
References
- Yayımlanan araştırma sonuçları:
-
Rausch T et al. (2012) Genome sequencing of pediatric medulloblastoma links catastrophic DNA rearrangements with TP53 mutations in cancer. Cell 148(1-2): 59-71.
-
Web References
- w1 – European Molecular Biology Laboratory hakkında daha fazla bilgi.
- w2 – The German Cancer Research Center (Deutsches Krebsforschungszentrum) 1000 bilimadamının kanserin mekanizmalarını araştırdığı, kanser risk faktörlerini tanımladığı ve insanları kanserden koruyan stratejileri bulmaya çalışan Almanya’daki en büyük biyomedikal araştırma enstitüsüdür.
- w3 – Kaynaklarını, tesislerini ve uzmanlarını Avrupa biliminin tam potansiyeline ulaşması için birleştiren EIROforum, Avrupa’nın en büyük sekiz devletlerarası bilimsel araştırma örgütünü bir araya getirmektedir. Eğitim ve sosyal yardım aktiviteleri bağlamında, Science in School dergisi EIROforum tarafından yayımlamaktadır.
Resources
- Genetikçilerin kanserli hücreleri nasıl belirlediği hakkındaki bir eğitim aktivitesi için, bakınız:
-
Communication and Public Engagement Team (2010) Bir kanser mutasyonunu belirleyebilir misiniz? Science in School 16: 39-44.
-
- Kanser kök hücrelerinin kanser tedavisinde nasıl devrim yarattığını öğrenmek için bakınız:
-
Mazza M (2011) Kanser Kök Hücreleri – gelecek için umut mu?Science in School 21: 18-22.
-
- Genetik mutasyonların hastalıklara nasıl neden olduğuyla ilgili daha fazla bilgi için bakınız:
-
Patterson L (2009) Getting a grip on genetic diseases. Science in School 13: 53-58.
-
- Kanser olasılığı da dahil, genlerinizin sizin için ne sakladıklarını bilmekle ilgili bir sınıf aktivitesi için bakınız:
-
Strieth L et al. (2008) Meet the Gene Machine: stimulating bioethical discussions at school. Science in School 9: 34-38.
-
Institutions
Review
Makale, bir senaryo oluşturmak için ilgi çekici olarak açık ve kısa olarak yazılmıştır. Kromozomların patlamasının kırılan kolyeye benzetilmesi çok uygundur. Bu, öğrencilerin patlayan bir kromozomun tekrar eski haline dönmesinin zorluğunu anlamasına yardımcı olabilir. Okulda bunun gösteri şeklinde gerçekleştirilmesi mümkündür çünkü boncuklar bir okulun biyoloji laboratuvarında standart olarak bulunan parçalardır.
Bu makale, genetik mutasyonların öğretilmesinde veya genlerin kanserdeki rolleri hakkında sürdürülen tartışmalarda ilave aktivite olarak kullanılabilir. Ayrıca, TP53 mutasyonlarıyla ilişkili başka araştırmalar için temel olarak veya kanser ve çocukluk medullablastomalarındaki genlerin rolleriyle ilgilenen tıp öğrencileri için de kullanılabilir. Uygun sorularla birlikte kullanıldığında bu makale; mutasyonlar, onkogenler, kanser türleri, kanser tedavileri ve telomerler hakkında web’e dayanan araştırmalar için geniş fırsat sunması bakımından kapsamlı bir alıştırma olarak kullanılabilir.
Uygun kavrama soruları şunları içerir:
- Eğer tüm hücrelerde bir mutasyon bulunursa bu daha çok rastgele midir yoksa ebeveynlerden kalıtılanmış mıdır? Cevabınızı açıklayın.
- Medulablastoma nedir? Onun neden bu kadar kötücül olduğunu açıklayın.
- Kromotripsisin ne olduğunu gösteren bir seri diyagram çizin.
- TP53 geninin iki görevi nedir?
- Bir TP53 mutasyonunun kansere yol açtığı iki olası mekanizma nelerdir?
- Onkogenler nedir?
- TP53 mutasyonu kanser tedavilerini nasıl etkiler?
- Telomerlerin kromozomlardaki görevi nedir?
Öğrenciler ayrıca nadir olan terim ve kavramlardan bir sözlük oluşturmak için makaleyi kullanabilirler.
Shaista Shirazi, Birleşik Krallık





