Wybuchające chromosomy: jak powstaje nowotwór Understand article
Tłumaczenie Katarzyna Badura. Nowotwory mózgu są jednym z najczęstszych powodów śmierci dzieci a ich punktem startowym może być moment, gdy dochodzi do rozerwania chromosomów w momencie podziału komórki.
TP53 zdaje się mieć wpływ
na chromosomalne
“eksplozje” powiązane z
powstawaniem nowotworów”
Zdjęcie dzięki uprzejmości
EMBL / P Riedinger
To scena rodem z wielu gospodarstw domowych: cała rodzina na klęczkach zbiera uciekające koraliki, a zrozpaczone dziecko stoi po środku z szeroko otwartymi oczami, trzymając w rękach resztki ulubionego naszyjnika.
Gdy w końcu większość koralików zostanie zebrana, jeden z dorosłych nawlecze je na nową nić i kryzys zostanie zażegnany. Chyba że dziecko nie będzie zadowolone z tego, że w rękach trzyma jedynie niemalże wierną kopię oryginału naszyjnika: znalezienie wszystkich koralików – włączając te, które wpadły pod kanapę albo za szafę – oraz ułożenie ich w oryginalnej kolejności jest naprawdę trudnym zadaniem.

francisblack / iStockphoto
W szpitalu Uniwersytetu w Heidelbergu w Niemczech, Andreas Kulozik napotkał rodzinę ze znacznie poważniejszym problemem: mała dziewczynka oraz jej brat posiadali w swoich organizmach wysoko rozwinięte, agresywne nowotwory. Andreas odkrył, że rodzeństwo posiada dokładnie taką samą mutację genu TP53. Mutacja ta była obecna we wszystkich komórkach ich organizmów, nie tylko tych nowotworowych, co znaczyło, że raczej musieli to odziedziczyć po rodzicach niż nabyć z komórek, które uformowały nowotwór.
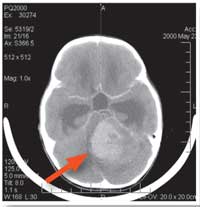
komputerowa) skan
obrazujący rdzeniaka (patrz
strzałka) w mózgu
sześcioletniej dziewczynki
Zdjęcie dzięki uprzejmości
Reytan; źródło obrazu:
Wikimedia Commons
Kiedy Jan Korbel z European Molecular Biology Laboratoryw1 (Europejskiego Laboratorium Biologii Molekularnej) nawiązał współpracę ze Stefanem Pfisterem i Peterem Lichterem z Niemieckiego Centrum Badań nad Rakiemw2 w celu zbadania genetycznej genezy dziecięcego nowotworu mózgu, wspomniane koneksje rodzinne zdały mu się dobrym punktem startowym. Jako członkowie Międzynarodowego Cancer Genome Consortium, Jan, Stefan oraz Peter po raz pierwszy sekwencjonowali genom komórek dziecięcego nowotworu. Nazwany rdzeniakiem, jest jednym z najczęściej występujących nowotworów złośliwych i drugą, po wypadkach samochodowych, przyczyną zgonów dzieci w krajach rozwiniętych.
„Kiedy dotarliśmy ponownie do danych sekwencji DNA, zauważyliśmy w genomie dziewczynki chaos, którego początkowo nie potrafiliśmy wyjaśnić.” powiedział Tobias Rausch, członek grupy badawczej Jana, który prowadził analizę danych. “Wtedy zobaczyłem publikację innej grupy badawczej, opisującą niedawno odkryte zjawisko, które nazwali chromothripsis, i wtedy zaskoczyło”, dodaje drugi członek grupy – Adrian Stütz.

faith goble; źródło obrazu:
Flickr
Naukowcy zdali sobie sprawę z tego, że obserwują właśnie chromothripsis, komórkowy odpowiednik scenariusza o zerwanym naszyjniku: chromosom (a czasami dwa) w jakiś sposób eksplodował na niezliczoną ilość małych fragmentów, które następnie zostały z powrotem złożone, czasem z pominięciem brakujących elementów, a momentami w złej kolejności. Wraz z przeanalizowaniem większej ilości próbek naukowcy zauważyli, że takie zjawisko ma miejsce w tkankach nowotworowych rdzeniaka u wszystkich pacjentów, którzy odziedziczyli mutację genu TP53, natomiast nie pojawia się w przypadkach normalnego genu TP53 lub w tkankach zdrowych osób chorujących na rdzeniaka.
“To pozwala nam przypuszczać, ze wszystkie trzy wydarzenia są ze sobą powiązane” mówi Jan “Przypuszczamy, że mutacja genu TP53 wywołuje eksplozję chromosomów, bądź też zapobiega przed tym, by komórka odpowiednio zareagowała. To w jakiś sposób prowadzi do bardziej agresywnych form raka.”
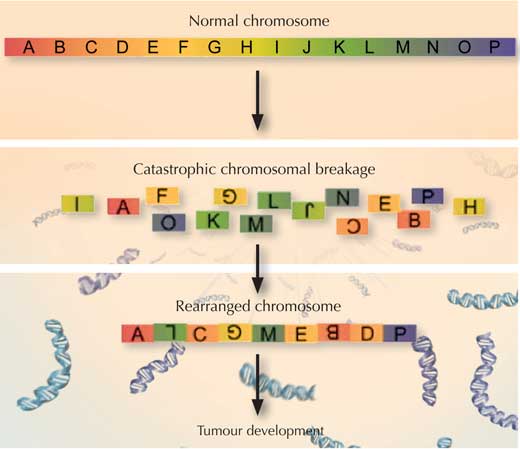
W takim razie w jakiś sposób mutacja genu TP53 wywołuje eksplozję chromosomu i jak może to prowadzić do nowotworu? Naukowcy wiedzą, że gen TP53 zapobiega przetarciu chromosomów na końcach, chroniąc tym samym telomery – zaślepki, które utrzymują końce chromosomów razem. W momencie, gdy gen TP53 jest uszkodzony, telomery mogą być zagrożone, a chromosomy mogą się do siebie przykleić, spekulują Jan i jego koledzy.
W myśl takiego scenariusza, w momencie podziału komórki, chromosomy, które są złączone mogą wygenerować problem. Byłyby one bowiem rozciągane w dwie przeciwne strony. W pewnym momencie naprężenie byłoby tak duże, że podobnie jak zbyt mocno pociągnięty naszyjnik, chromosomy popękałyby rozsyłając w różne strony fragmenty DNA. Jako że w tym momencie do akcji ruszyłaby komórkowa maszyneria mająca na celu poskładanie chromosomu (-ów), niektóre fragmenty materiału genetycznego mogłyby zostać pominięte, bądź też umieszczone w złej kolejności, a nawet w złym chromosomie.

Evan-Amos; źródło obrazu:
Wikimedia Commons
Z drugiej strony, gen TP53 odgrywa równie kluczową wolę w kontroli naszego DNA pod kątem uszkodzeń. Jeśli ten strażnik genomu znajdzie zbyt wiele błędów, może skierować komórkę na drogę programowanego samobójstwa (apoptozy) lub komórkowego odpowiednika domu starców (etap starzenia się), w celu uniknięcia podziału takiej komórki i dalszego przekazywania wad genetycznych.
Jeśli jednak gen TP53 jest zmutowany, rozległe uszkodzenia DNA mogą pozostać niezauważone – uszkodzenia takie jak błędnie poskładany chromosom po chromothripsis, niezależnie od tego, czy gen TP53 był powiązany z eksplozją chromosomu, czy też nie. W rezultacie dochodzi do aktywacji onkogenów – genów odpowiedzialnych za powstawanie nowotworu – a tym samym komórka zaczyna się niekontrolowanie dzielić i dzielić generując nowotwór. Jan, Stefan i Peter spekulują, że konsekwencje wadliwego genu TP53 w kombinacji z innymi czynnikami mogą prowadzić do nowotworu u tych pacjentów, dlatego też chcieliby przeprowadzić bardziej szczegółowe badania, by móc stwierdzić co dokładnie dzieje się na poszczególnych etapach.
W międzyczasie, ich odkrycie wywołało negatywne konsekwencje zarówno dla grupy klinicystów takich jak Andreas i Stefan, jak również dla ich pacjentów. „Teraz już wiemy, że gdy komórki nowotworowe pacjenta wykazują oznaki chromothripsis, musimy poszukać dziedzicznej mutacji w genie TP53” mówi Stefan. Ten fakt jest niezwykle istotny, ponieważ posiadanie odziedziczonej mutacji genu TP53 mogłoby zostać wykorzystane w terapii przeciwnowotworowej działającej na zasadzie rykoszetu. Wiele chemio- i radioterapii polega na zabijaniu komórek nowotworowych poprzez niszczenie ich DNA, jednak nie pozostaje to bez wpływu na inne komórki ciała. U wielu pacjentów, mimo iż może to prowadzić do bolesnych efektów ubocznych, nie generuje to długoterminowej szkody. Inaczej wygląda sytuacja w przypadku osób posiadających mutację genu TP53. Z powodu tej właśnie mutacji, wszystkie komórki takiego pacjenta, włączając również te zdrowe, będą miały problem z uporaniem się z uszkodzeniami DNA.
W ten właśnie sposób terapie, których punktem docelowym jest DNA mogą spowodować, że komórki zdrowe zmienią się w nowotworowe, powodując tym samym powstanie drugo- lub trzeciorzędowych nowotworów – “takie zjawisko często obserwujemy u pacjentów posiadających odziedziczoną mutację genu TP53” mówi Stefan. Dla takich pacjentów wskazane byłoby przepisanie terapii wykorzystującej jednostki generujące mniejsze zniszczenia DNA. Co więcej, jeśli pacjent posiada w swoim organizmie odziedziczoną mutację genu TP53, powinno to skłonić lekarza do przebadania najbliższej rodziny pacjenta. Jeśli którykolwiek ze zdrowych badanych członków rodziny posiada w swoim organizmie tą mutację, powinien być poddawany regularnym badaniom, jako że jest z natury podatny na ewentualny rozwój nowotworu w późniejszym etapie życia. „Największe szanse na zwalczenie nowotworu – szczególnie tego złośliwego, we wczesnej fazie rozwoju, powiązanego z chromothripsis – mamy w momencie, gdy jest on wcześnie zdiagnozowany” podkreśla Jan.
W rzeczywistości naukowcy są przekonani, że 2-3% wszystkich nowotworów najprawdopodobniej powstaje w wyniku chromothripsis, dlatego też grupa Jana w chwili obecnej sprawdza czy mutacja genu TP53 odgrywa jakąś rolę w podobnych eksplozjach chromosomów mających miejsce w przypadkach innych chorób nowotworowych niż rdzeniak. Na chwilę obecną udało im się znaleźć dowody na powiązanie zjawiska chromothripsis i odziedziczonej mutacji genu TP53 w badanej przez nich ostrej białaczce szpikowej. W przypadku tego agresywnego nowotworu krwi atakującego organizmy dorosłych, Jan wraz z kolegami odkrył, że pacjenci nieposiadający odziedziczonej mutacji genu TP53 (np. z mutacją obecną tylko w komórkach nowotworowych) oraz wykazujący objawy chromothripsis mają tendencję do życia dłużej. Naukowcy wskazują, iż ma to sens biorąc pod uwagę jaką funkcję pełni gen TP53 w integralności telomerów. Nasze zatyczki chromosomowe ulegają naturalnemu skróceniu wraz z wiekiem, a to zwiększa prawdopodobieństwo złączenia się chromosomów w momencie, gdy z genem TP53 dzieje się coś niedobrego. To ostatecznie doprowadza do chromothripsis, a w konsekwencji zwiększa prawdopodobieństwo zmian nowotworowych, podejrzewają naukowcy.
Grupa Jana kontynuuje badanie tej kwestii zarówno w mózgu, jak i krwi jak również w innych nowotworach, próbując wyjaśnić w jaki sposób błędna wersja genu TP53 jest połączona z chromosomami pękającymi jak naszyjniki, oraz z innymi aspektami funkcjonowania komórek w przypadku pojawienia się nowotworu.
Więcej o EMBL

Europejskie Laboratorium Biologii Molekularnej (EMBL)w1 jest jednym z największych na świecie instytutów badawczych, dedykowanych badaniom podstawowym w naukach przyrodniczych. EMBL jest jednostką międzynarodową, innowacyjną i interdyscyplinarną. Jej pracownicy, pochodzący z 60 krajów świata, posiadają wiedzę z zakresu biologii, fizyki, chemii oraz informatyki i współpracują prowadząc badania, które obejmują pełne spektrum biologii molekularnej.
EMBL jest członkiem EIROforumw3, wydawcy Science in School.
References
- Wyniki badań zostały opublikowane w:
-
Rausch T et al. (2012) Genome sequencing of pediatric medulloblastoma links catastrophic DNA rearrangements with TP53 mutations in cancer. Cell 148(1-2): 59-71.
-
Web References
- w1 – Dowiedz się więcej o European Molecular Biology Laboratory.
- w2 – Niemieckie Centrum Badań nad Rakiem (Deutsches Krebsforschungszentrum) jest największym biomedycznym instytutem naukowym w Niemczech. Pracuje tam ponad 1000 naukowców, badając mechanizmy nowotworowe, identyfikując nowotworowe czynniki ryzyka i opracowując strategie zapobiegania przypadkom zachorowania na raka.
- w3 – EIROforum jest rodzajem współpracy pomiędzy ośmioma największymi międzyrządowymi badawczymi organizacjami naukowymi, które łączą swoje zasoby, zaplecze i doświadczenie do wspierania europejskiej nauki w celu osiągnięcia pełnego potencjału. W ramach swojej działalności edukacyjnej i promocyjnej, EIROforum publikuje Science in School.
Resources
- Żeby znaleźć zajęcia dla nauczyciela o tym jak genetycy identyfikują komórki nowotworowe wejdź na:
-
Communication and Public Engagement Team (2010) Czy umiałbyś znaleźć mutację powodującą nowotwór? Science in School 16.
-
- Żeby się dowiedzieć w jaki sposób komórki macierzyste raka mogą zrewolucjonizować sposób leczenia raka, zobacz:
-
Mazza M (2011) Komórki macierzyste nowotworu – nadzieja na przyszłą terapię? Science in School 21: 18-22.
-
- Jeśli chcesz zdobyć więcej informacji na temat genetycznych mutacji powodujących choroby przeczytaj:
-
Patterson L (2009) Zmierzmy się z chorobami genetycznymi. Science in School 13.
-
- W celu przygotowania zajęć dla klasy na temat tego jakie informacje przechowują w sobie geny, w tym prawdopodobieństwo zachorowania na raka, sprawdź:
-
Strieth L et al. (2008) Meet the Gene Machine: stimulating bioethical discussions at school. Science in School 9: 34-38.
-
Institutions
Review
Artykuł został napisany w jasny i zwięzły sposób, stanowiąc interesujące podstawy na scenariusz zajęć. Porównanie eksplozji chromosomów do zerwanego naszyjnika jest bardzo trafne, może pomóc studentom zrozumieć jak trudne jest złożenie rozerwanego chromosomu w jedną całość zgodnie z pierwotnym wzorem. Przygotowanie demonstracji na zajęcia jest możliwe, ze względu na fakt, że tak małe elementy jak paciorki czy koraliki bez większego problemu można znaleźć w pracowni biologicznej.
Ten artykuł można wykorzystać jako rozszerzenie tematu genetycznych mutacji bądź też rozwinięcie dyskusji na temat roli genów w nowotworach. Może zostać również użyty jako podstawa do dalszych poszukiwań informacji związanych z mutacjami genu TP53 oraz szeroko pojętą rolą genów w rozwoju nowotworów i dziecięcego rdzeniaka dla studentów chcących w przyszłości związać się z medycyną. W połączeniu z odpowiednimi pytaniami kontrolnymi, artykuł ten może zostać wykorzystany jako ćwiczenie czytania ze zrozumieniem z szeroką gamą możliwości na późniejsze przeszukiwania internetowych baz danych w poszukiwaniu informacji związanych z tematyką mutacji, onkogenów, rodzajów nowotworów, sposobów leczenia nowotworów oraz telomerów.
Przykłady odpowiednich pytań kontrolnych:
- Jeśli mutacja zostanie stwierdzona we wszystkich komórkach to czy jest to wynik przypadkowej mutacji czy mutacji odziedziczonej po rodzicach? Uzasadnij swoją odpowiedź.
- Czym jest rdzeniak? Wyjaśnij dlaczego jest taki złośliwy.
- Narysuj serię diagramów obrazujących czym jest chromothripsis.
- Jakie są zadania genu TP53?
- Jakie są dwa mechanizmy w wyniku których mutacja genu TP53 może doprowadzić do powstania raka?
- Czym są onkogeny?
- W jaki sposób mutacja genu TP53 wpływa na sposób prowadzenia terapii przeciwnowotworowej?
- Jaką funkcję pełnią w chromosomach telomery?
Uczniowie mogą również korzystać artykuł skonstruować słowniczek nietypowych słów i pojęć.
Shaista Shirazi, Wielka Brytania





