Le nouveau système international d’unités SI Understand article
Les progrès de la recherche scientifique sont tels que toutes les unités fondamentales vont pouvoir être définies en fonction de constantes fondamentales de l’Univers.
Malgré l’obstination des USA à s’en tenir aux unités comme le mile, la livre ou le degré Fahrenhait, le reste du monde est en général d’accord pour utiliser des unités qui se divisent par dix. Le système métrique, dit aussi Système International d’Unités (SI) est le moyen le plus complet et le plus précis que l’homme a inventé pour mesurer l’univers. Il comprend les sept unités de base pour la longueur, la masse, le temps, le courant électrique, la luminosité et la quantité de matière.
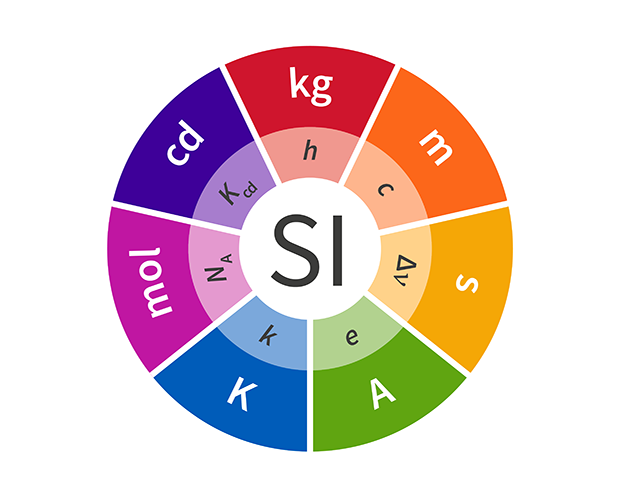
Avec la permission du BIPM
Depuis l’introduction du système métrique vers 1790, les scientifiques se sont acharnés à en définir les unités de manière de plus en plus précise. Quatre d’entre elles vont être revisées : le kilogramme (kg), le kelvin (K), l’ampère (A) et la mole (mol), pour les relier à des constantes universelles. Ces nouvelles définitions seront adoptées de manière internationale le Jour de la métrologie mondiale, le 20 mai 2019. Après cette date, toutes les unités du système métrique seront définies à partir des constantes de l’univers.
Le mètre (distance)
En 1799, on a défini le mètre par deux traits gravés sur une barre de platine. Mais récemment les physiciens ont réalisé que le mètre peut être défini avec plus de précision (une partie par milliard) en utilisant l’interféromètre qui a permis de découvrir les ondes gravitationnelles. Le mètre (m) est aujourd’hui la distance parcourue par la lumière dans le vide pendant 1/299 792 458 ème de seconde. Cette définition ne sera pas modifiée par la nouvelle mise à jour 2019.
Kilogramme (masse)

international est un cylindre
d’un alliage platine-iridium.
Avec la permission du BIPM
Pendant plus d’un siècle, le kilogramme standard a été un cylindre de platine-iridium conservé au Bureau International des Poids et Mesures BIPM près de Paris, France. Mais sa masse précise fluctue à cause de facteurs comme l’accumulation de poussière microscopique. Dorénavant, le kilogramme sera défini par rapport à la constante de Planck, qui vaut 6.626070040 x 10-34 kg m2 s-1. Cette constante, représentée par la lettre h, est la plus petite quantité d’énergie quantifiée. Elle sert à calculer les énergies en physique des particules.
La seconde (temps)
La seconde a tout d’abord été fixée à partir du temps séparant deux pleines lunes. Puis, on l’a définie par rapport à la durée du jour solaire, et enfin par rapport à l’année solaire. Mais aujourd’hui, les secondes sont définies à l’échelle atomique, avec une précision de une partie sur dix milliards. Le temps atomique est basé sur la période d’une radiation produite et absorbée par les atomes, qu’on appelle “fréquence de transition hyperfine” (Δν). Une seconde est (et restera) 9 192 631 770 périodes de la radiation du Césium-133.
Le kelvin (température)
L’échelle de température en kelvin commence à l’état le plus froid possible de la matière. Aujourd’hui, le kelvin est défini par le point triple de l’eau, qui est la température où l’eau coexiste sous forme solide, liquide et gazeuse. Comme ce point triple est à 273.16 K, un Kelvin vaut le 1/273.16 ème du point triple. Mais l’eau n’est jamais pure, et les impuretés influencent sur ce point triple. En 2017, une équipe de physiciens allemands du Physikalisch-Technische Bundesanstalt a mesuré la constante de Boltzmann avec une précision inégalée. Cette constante, symbolisée par la lettre k, est le rapport de l’énergie cinétique moyenne des particules de gaz divisée par la température du gaz. Elle vaut exactement 1.38064852 x 1023 joule par Kelvin. Donc elle sert à redéfinir la température, qui est donc maintenant égale à l’énergie cinétique d’un gaz divisée par k.

Paul Vladuchick/Flickr, CC BY-NC-ND 2.0
L’ampère (courant électrique)
André-Marie Ampère (1775–1836), qui est souvent considéré comme le père de l’électrodynamique, a l’honneur d’avoir donné son nom à l’unité de courant électrique. Jusqu’à aujourd’hui, l’ampère était la quantité de courant qui produit une force de 2 x 10-7 newton par mètre séparant deux conducteurs parallèles de longueur infinie. Mais, comme c’est difficile de se référer à des choses de longueur infinie, on a décidé de redéfinir l’ampère à partir de la charge fondamentale d’une particule, à savoir celle de l’électron, dont la charge e est définie comme égale à 1.6021766208 x 10-19 ampère seconde.
La candela (luminosité)

luminosité
approximativement égale à
une candela.
tristangage/Flickr, CC BY-NC-
ND 2.0
La dernière unité de base SI est la candela, qui mesure la luminosité, qu’on appelle aussi brillance, et qui est l’énergie diffusée dans l’espace entourant une source lumineuse. Les premiers standards de la candela étaient reliés à la radiation du corps noir, c’est-à-dire à la lumière émise par tous les objets en fonction de leur température. Aujourd’hui la candela vaut 1/683 watt d’une lumière jaune de 540 x 1012 Hz émise par stéradian. Et cette définition ne sera pas modifiée. A titre de comparaison, une bougie ordinaire a une intensité lumineuse de presque 1 candela.
La mole (quantité de matière)
A la différence de toutes les autres unités de base, la mole est un nombre sans dimension. Elle relie le nombre d’atomes à la masse, en suivant une approche amorcée par Amadeo Avogadro (1776 – 1856). Jusqu’à aujourd’hui, la mole a été définie comme le nombre d’atomes qu’il y a dans 12 gramme (g) de Carbone-12. Ce nombre, appelé nombre d’Avogadro, vaut environ 6 x 1023. La nouvelle définition de la mole ne dépendra plus de la définition du kilogramme. Ce sera la masse de 6.022140857 x 1023 objets (atomes ou molécules).

Science Photo Library
Acknowledgement
Ceci est la version éditée d’un article publié en ligne dans le magazine Symmetry du 7 novembre 2017w1.
Web References
- w1 – Symmetry magazine est une publication en ligne gratuite, traitant de physique des particules: Elle est publiée par le Fermi National Accelerator Laboratory et par SLAC National Accelerator Laboratory, USA. L’article en ligne se trouve sur Symmetry website.
Resources
- En savoir plus sur le Jour de la métrologie mondiale.
- La mesure précise de la constante de Boltzmann se trouve sur mesurer la constante de Boltzmann avec une précision extrême.
- Et voici un article accessible sur le changement des unités SI prévu en mai 2019.
- La détection des ondes gravitationnelles par la collaboration LIGO se fait via:
- Introduction à LIGO et aux ondes gravitationnelles: un clapotis de l’espace-temps.
- Diana Kwon (2017) Comment enclencher le microphone cosmique. Science in School 39: 8-11.
Review
La science et la technologie ont fait de tels progrès récemment qu’on peut faire aujourd’hui des mesures physiques avec une précision inégalée. Cet article décrit comment ces progrès agissent sur la métrologie.
Dès leurs premières leçons de sciences, les élèves apprennent le système d’unités SI, mais ils ont parfois de la peine avec la physique qui est derrière ces définitions. Cet article sert à introduire les unités de base aux élèves de 11 à 16 ans, et les unités plus complexes aux élèves plus âgés.
L’information sur les définitions d’unités peut aussi être utilisée en sens inverse, c’est-à-dire qu’on peut étudier les définitions une fois que les unités sont comprises. Par exemple, enseigner les ondes gravitationnelles conduit à introduire les mesures par interférométrie, lesquelles sont connectées à la définition du mètre.
Voici quelques questions de compréhension que le maître peut utiliser:
- Qu’appelle-t-on Système International d’Unités?
- Expliquer les différences entre le SI et le système d’unités en usage aux USA.
- Nommer les sept unités de base du SI, ainsi que les grandeurs physiques qui leur correspondent.
- Pourquoi est-ce qu’on change les définitions des unités SI?
- Choisir une grandeur physique du SI et expliquer la définition correspondante de son unité.
Gerd Vogt, maître de physique et coordinateur des sciences, Higher Secondary School for Environment and Economics, Yspertal, Austria





