Masticar sabores Teach article
Traducido por: Liliana Olazar. Ken Gadd y Luca Szalay presentan un procedimiento usado en la industria –y adaptado para alumnos de escuela- para medir el nivel de ácido cítrico en la goma de mascar.
¿Cuán ácida es la goma de mascar?

¿Cuánta gente conoces que masquen chicle? ¿Por qué lo hacen? Podrías probar con una encuesta pero la respuesta más probable será por el sabor. La goma de mascar consiste en una base de goma, insoluble en agua e ingredientes solubles en agua tales como saborizantes y edulcorantes (endulzantes). Cuando la masticas, los saborizantes y los endulzantes se liberan , se disuelven y se traban (esperamos que la goma quede retenida en la boca). Una vez que el sabor se ha extraido, la goma (el chicle) se descarta. Desafortunadamente se pega fuertemente a superficies duras como el concreto y es muy difícil de remover.
Hay evidencia suficiente de esto si miras los pavimentos sobre los que caminas. Pero volvamos al sabor…
Un ingrediente común en el chicle (goma de mascar) y en otras confituras es el ácido cítrico. Es el que da ese agudo, refrescante sabor cítrico que “ataca” la lengua. El envase te dirá cuánto ácido cítrico hay en la goma de mascar. Es el rol de un químico analítico en el laboratorio control de calidad investigarlo. El método que se indica debajo se basa en un procedimiento estándar usado por una compañía que fabrica varios sabores de goma de mascar y de chicles para hacer globos (un tipo de goma de mascar). Ha sido adaptado para usar en escuelas y universidades de tal manera que tus estudiantes puedan imitar un auténtico lugar de trabajo.
Aquí se presentan algunas preguntas que podrían usarse para que los alumnos piensen:
- ¿Cuantas personas conoces que masquen chicles (goma de mascar)?
- ¿Cuántos años tienen?
- ¿Qué hace diferente a los chicles para hacer globos de los otros tipos de goma de mascar?
- ¿Cómo puedes remover un chicle de la tela?
- ¿Cómo puedes remover un chicle de la tela?
- ¿Cómo podrías determinar cuánto ácido hay en un chicle?
El proyecto StandardBase
El proyecto StandardBase ha producido 72 procedimientos analíticos usados en la industria y adaptado para uso de estudiantes en la escuela y en la universidad a los que se puede acceder por Internet. Para mayor información acerca del proyecto, vea “Standardbase: un proyecto piloto de Leonardo da Vinci para la educación práctica y el entrenamiento en química” en este número de Science in School.
El procedimiento: la determinación de ácido cítrico en Hubba Bubba® goma de mascar usada en una titulación ácido base
| Duración |
Una hora |
|---|---|
| Instrumentos analíticos usados | Material volumétrico |
| Especificaciones de la meustra | Goma de mascar (para hacer globos) Hubba Bubba® sabor naranja |
| Provista en |
La mayoría de los negocios de golosinas y supermercados |
| Componente a determinar | Ácido cítrico |
| Método(s) |
Titulación ácido base |
| Campo | Alimento y bebidas |
Antes de comenzar el práctico, los docentes pueden querer que sus alumnos comprendan la química del análisis. Para evaluar si ellos tienen un conocimiento apropiado, los estudiantes podrían probar el test interactivo en el standarbase websitew1. Para ayudar con su trabajo, los estudiantes también pueden bajar un archivo sobre titulaciónw2.
Alcance
El objetivo de este procedimiento analítico es determinar el contenido de ácido cítrico en el chicle Hubba Bubba®. Este chicle para hacer globos está disponible en el Reino Unido y en la mayor parte de Europa. Está hecho por Wrigleyw3, en Plymouth, Reino Unido. El método descripto aquí se basa en un procedimiento analítico usado por Wrigley, en sus laboratorios de Plymouth.
Principio
La determinación se basa en una reacción ácido base entre el ácido cítrico en la goma de mascar una solución estándar de hidróxido de sodio. El contenido de ácido cítrico de la goma de mascar se puede calcular de los resultados de la titulación.
Equipamiento
- Palo de amazar de repostería
- Matraz cónico de 250 cm3
- Matraz graduado de 250 cm3
- Matraz graduado de 100 cm3
- Agitador magnético y buzo o barra magnética (también conocido como “pulga”)
- Bureta de 10 cm3 (lectura a la 0,02 de cm3)
- Balanza analítica
- Bloque de madera
- Cuchillo tijeras
Materiales y sus números de registro (Chemical Abstracts Service, CAS)w4
- Hubba Bubba® sabor naranja
- Hidróxido de sodio (número de registro, 1310-73-29)
- Fenolftaleína (número de registro, 77-09-8)
Soluciones de reactivos
- Solución estándar 0,1 M. Si esto no estuviera disponible, disuelva 1 g de hidróxido de sodio en aproximadamente 100 cm3 de agua pura. Diluya cuidadosamente a un matraz de 250 cm3y lleve a volumen. Homogeinice la solución. Estandandarice por medio de la titulación con 0,1 M de ácido clorhídrico, estandarizado frente a bicarbonato de potasio sólido (KHCO3).
- Indicador: fenolftaleína. Pesar 0,2 g de fenolftaleína y disolverla en alrededor de 50 cm3 de alcohol metílico. Transferir la solución a un matraz aforado de 100 cm3, llevar a volumen con alcohol y homogeneizar la solución.
Procedimiento
- Tomar un chicle sabor naranja Hubba Bubba®, quitarle el envoltorio y colocarlo sobre el bloque de madera.
- Con el rodillo, enrolle el chicle goma en una tira muy delgada de 160 x 30 x 0.5 mm.
- Corte la delgada tira en pequeños trozos de alrededor de la longitud de un grano de arroz.
- Pese trozos de alrededor de 1 g de chicle Hubba Bubba®.
- Agregue alrededor de 100 cm3 de agua pura contenida en un frasco cónico de tipo Erlenmeyer. Ubíquelo sobre el agitador magnético y coloque el “buzo”.
- Agite vigorosamente por 30 minutos y asegúrese que los trozos de goma de mascar no se aglutinen.
- Agreguen 0.50 cm3 de fenolftaleína y titulen con 0.10 mol dm-3 hidróxido de sodio dentro de una bureta de 10 cm3. En el punto final, el color es rosa.
- Repitan dos veces más y promedien los tres resultados. Titulación promedio = V cm3.
Cálculos
Use lo siguiente para calcular el porcentaje en masa de ácido cítrico monohidrato presente en el chicle Hubba Bubba®:
- Cada centímero cúbido de solución de hidróxido de sodio 0.10 mol dm-3es equivalente a 7 mg de ácido cítrico monohidrato
- %en masa de ácido cítrico monohidrato: 0,7V
Nota: es necesario un factor de corrección si el hidróxido de sodio no es exactamente 0.10 mol dm-3.
Expresión de resultados
Indique la masa de ácido cítrico monohidrato en el chicle Hubba Bubba® en porcentaje en masa (masa de ácido cítrico monohidrato en 100 g de chicle de mascar) El rango permitido en la fabricación es 1,9 a 2,1 % en masa.
Precisión
La precisión del análisis se determina por la lectura en las buretas. Un estudiante poco experimentado podría leer una bureta con una precisión de ± 0.05 cm3. Estudiantes con más experiencia podrían llegar a leer hasta ± 0.02 cm3.
El gráfico
El gráfico debajo muestra el resultado obtenido por estudiantes en otros países europeos (preciso al tiempo de ir a prensa). Si sus estudiantes están interesados en hallar nuestra último estado, ellos pueden ver la mayoría de los resultados hasta la fecha en líneaw5.
Si sus estudiantes quieren adicionar sus resultados al gráfico escríbale a Luca Szalay (luca@chem.elte.hu). Ud. obtendrá un nombre de usuario y una password para usar esta función de la base de datos. Luego Ud puede registrar a los alumnos, lo cual les permitirá a ellos subir sus nombres sobre el gráfico.
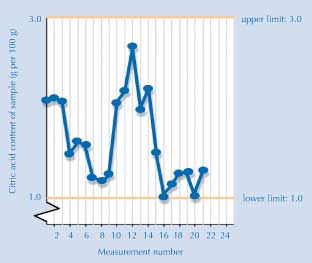
Imagen cortesía de Luca Szalay
Web References
- w1 – Los profesores podrían conseguir que sus alumnos probaran un test interacivo en el sitio web Estandard Base: www.vapro-ovp.com/applications/toetsing/vraag.asp?toetsID=29
- w2 – Un archivo sobre titulación podría bajarse desde el sitio Estándar Base, web es www.standardbase.com/tech/uk-voltech.pdf
- w3 – Para más información acerca delos productos Hubba Bubba® vea www.wrigley.co.uk/index.cfm?articleid=138
- w4 – El registro CAS, el mayor y más consultado registro de o de la información de las sustancias en el mundo. Véase: www.cas.org/expertise/cascontent/registry/regsys.html
- w5 – Un gráfico de los resultados previos de estos análisis se pueden ver y bajar aquí: http://standardbase.live.ism.nl/sbase/maindetails.asp?expid=3362#
Review
Este artículo ofrece una aproximación interesante a las reacciones ácido base y titulación ácido base, dos tópicos que usualmente son considerados como pesados y aburridos. ¿Recuerda cuando era un estudiante?
Comenzando con un objeto familiar (la goma de mascar) con sus características y problemas prácticos, los autores presentan el procedimiento (determinación del ácido acético en el chiclo Hubba Bubba ®, extendiéndose el sujeto a aspectos teóricos con la ayuda de las referencias de la web. Los profesores de Química podrían usar el artículo para discutir la importancia de los procedimientos analíticos estándar , además para los temas de reacciones ácido base y titulación. La propuesta de análisis le da la oportunidad de un tratamiento matemático y compartir los datos obtenidos, además relacionar química con estadísticas y el idioma inglés.
Para relacionar con un trabajo de laboratorio de control de calidad, la riqueza de los materiales didácticos en el sitio StandardBase (test preliminares, teoría, gráficos y protocolos) hacen de Mascando favores un recurso útil para los profesores de química y los estudianes . Podría ser usado para discutir el rol de los químicos analíticos en el contexto de una industria y la investigación y/o para preparar una visita a una fábrica o un laboratorio.
El artículo podría ser útil en un secundario superior o escuelas vocacionales en Italia, no sólo para probar la actividad propuesta sino también otros procedimientos del proyecto StandardBase que están disponibles en el sitio web. La posibilidad de unir el proyecto es otro rasgo del artículo.
A los profesores les podrían gustar las siguientes preguntas de comprensión:
La sustancia que le da el sabor a naranja a Hubba Bubba® es:
a) ácido málico
b) ácido cítrico
c) ácido ascorbico
d) ácido clorhídrico
La concentración de la solución titulante usada en el procedimiento es:
a) 0.10 g dm-3
b) 1.00 % de la mole
c) 0.10 mol dm-3
d) 1.00 mol dm-3
Siguiendo las sugerencias de los autores, encontraría interesante continuar con aspectos químicos de la remoción de la goma de mascar de diferentes superficies y telas.
Giulia Realdon, Italia





