Από τους ρωμαϊκούς δρόμους, τους σιδηρόδρομους και τους επιθεωρητές: οι πρόσφατες ανακαλύψεις στην έρευνα για το RNA Understand article
Μετάφραση Αργυρώ Βεργανελάκη (Argyro Verganelaki). Το RNA είναι ένα κρίσιμο βιολογικό μακρομόριο που σπάνια αναφέρεται λεπτομερώς στα εγχειρίδια. Στο πρώτο άρθρο μιας…

Florian Raible αναζητώντας
το πιο γρήγορα και πιο
αργά εξελισσόμενο είδος
Χορηγία εικόνας από EMBL
Photolab
Φανταστείτε έναν Ρωμαίο στους αρχαίους χρόνους, να στέκεται σε μια κορυφή, εξερευνώντας το τοπίο, καθώς σχεδιάζει την πορεία ενός νέου δρόμου. Δύο χιλιάδες έτη αργότερα οι δρόμοι του είναι ακόμα ορατοί καθώς διασχίζουν τις ευρωπαϊκές πόλεις και την επαρχία, τόσο ευθείες όσο μπορεί να σχεδιάσει ένας χάρακας, παρεκκλίνοντας μόνο από τα πιο επίμονα εμπόδια. Στις δεκαετίες του ’50 και του ’60, οι επιστήμονες χάραξαν μία παρόμοια διαδρομή για τη βιολογία, καθώς περιέγραψαν τις σχέσεις μεταξύ των διαφορετικών τύπων μορίων στο κύτταρο.
Το σχέδιό τους είναι γνωστό ως κεντρικό δόγμα της μοριακής βιολογίας: “Το DNA σχηματίζει το RNA, το οποίο σχηματίζει τις πρωτεΐνες,” όπως κατέγραψε ο James Watson σε ένα από τα σημειωματάριά του, όταν αυτός και ο Francis Crick άρχισαν την έρευνά τους στη δομή του DNA. Με το δόγμα, οι δύο ερευνητές πρότειναν μια νέα σχέση μεταξύ των πιο σημαντικών κυτταρικών μακρομορίων – μια μονόδρομη ροή των πληροφοριών από τα νουκλεϊκά οξέα στις πρωτεΐνες. Σύντομα μετά από την ανακάλυψη της διπλής έλικας, ο Crick έδωσε διαλέξεις στις οποίες παρουσίασε το δόγμα ως ένα μεγάλο ερευνητικό σχέδιο για τη μοριακή βιολογία (Crick, 1970): οι επιστήμονες πρέπει να αφιερωθούν στην αποκάλυψη των κυτταρικών μηχανισμών που κρύβονται πίσω από αυτούς τους μετασχηματισμούς.
Μέχρι τη δεκαετία του ’70, είχαν γίνει κατανοητά τα βασικά στοιχεία για το πώς δημιουργήθηκαν τα RNAs και οι πρωτεΐνες, αλλά ήταν προφανές ότι ένας μόνο ευθύς δρόμος δεν θα μπορούσε να περιγράψει τη χημεία του κυττάρου. Ακριβώς όπως οι σύγχρονες διακλαδώσεις σε εκείνους τους αρχαίους ρωμαϊκούς δρόμους, πολλές αποκλίσεις έχουν βρεθεί στη διαδρομή μεταξύ των γονιδίων και των πρωτεϊνών. Στην αρχή φάνηκαν να είναι σπάνιες εξαιρέσεις στο δόγμα, ταυτόχρονα όμως είχαν αναγνωριστεί ως κοινές και κρίσιμες στις περισσότερες βιολογικές διαδικασίες στους σύνθετους οργανισμούς. Μερικά από τα συμπεράσματα είναι τόσο νέα, που δεν υπάρχουν ακόμη στα εγχειρίδια και μπορεί να είναι άγνωστα στους καθηγητές. Αυτό το άρθρο είναι το πρώτο μιας σειράς για το περιοδικό “Επιστήμη στο σχολείο” (Science in school), που θα συζητήσει ένα μέρος από αυτήν την πρόσφατη έρευνα.
Μερικά από τα πιο συναρπαστικά συμπεράσματα αφορούν το RNA, το οποίο κάποτε θεωρούταν να παίζει τον έσχατο ρόλο στην κατασκευή των πρωτεϊνών. Την τελευταία δεκαετία, όμως, αυτά τα μόρια βρέθηκαν να παίζουν κρίσιμο ρόλο στον έλεγχο της γονιδιακής πληροφορίας και έκφρασης. Η κατανόηση της λειτουργίας των RNAs, έχει οδηγήσει στην βαθύτερη γνώση πολλών ασθενειών και στην ανακάλυψη νέων ειδών βιοτεχνολογίας, συμπεριλαμβανομένων των προσπαθειών να χρησιμοποιηθεί το RNA στη θεραπεία ασθενειών, που οφείλονται σε ελαττωματικά γονίδια.
Εναλλακτική ωρίμανση
Το RNA του κεντρικού δόγματος είναι το αγγελιαφόρο RNA (mRNA), το οποίο χρησιμεύει ως μήτρα για την κατασκευή των πρωτεϊνών. Στα ευκαρυωτικά κύτταρα, τα πρόδρομα mRNAs συνήθως πρέπει να υποβληθούν σε επεξεργασία πριν γίνουν ώριμα mRNA. Τα πρόδρομα mRNAs είναι όπως τα μακριά τρένα με πολλά βαγόνια, των οποίων το φορτίο πρέπει να ταξινομηθεί για να ανταποκριθεί στις ανάγκες των διαφορετικών πελατών. Τα κενά βαγόνια αποσυνδέονται και αυτά που είναι εκατέρωθεν επανασυνδέονται. Οι κυτταρικές σειρές με τα άδεια βαγόνια, ονομάζονται εσώνια , μεγάλες περιοχές μέσα στα γονίδια που δεν μεταφράζονται σε πρωτεΐνες. Οι αλληλουχίες του DNA που μεταφράζονται λέγονται εξώνια. Συχνά ένα εξώνιο περιέχει τη συνταγή για μία μονάδα μιας πρωτεΐνης. Ακόμη και αυτά δεν χρησιμοποιούνται πολλές φορές. Μπορεί ένας πελάτης να μην θελήσει όλα τα εμπορεύματα σε ένα τρένο, έτσι μερικά από τα βαγόνια που περιέχουν φορτίο, μπορεί να αφαιρεθούν μαζί με τα κενά. Και ένα κύτταρο μπορεί να μην χρειαστεί όλες τις μονάδες μιας συγκεκριμένης πρωτεΐνης, οπότε διάφορα εξώνια μπορούν να συνδυαστούν για να παράγουν διαφορετικές μορφές.
Αυτή η διαδικασία, αποκαλούμενη ως εναλλακτική ωρίμανση, ανακαλύφθηκε ανεξάρτητα το 1977 από τους Richard Roberts της New England Biolabs, ΗΠΑ, και Phillip Sharp του Massachussetts Institute of Technology, ΗΠΑ (Berget et al., 2000). Η ανακάλυψη ήταν τόσο σημαντική που τους έδωσε το βραβείο Νόμπελ στη Φυσιολογία ή Ιατρική το 1993w1. Την εποχή που η διαδικασία της ωρίμανσης θεωρούταν σπάνια, ο Sharp υπολόγιζε ότι μόνο το 5% περίπου των ανθρώπινων γονιδίων ήταν πιθανό να υποβληθούν σε εναλλακτική ωρίμανση. Η χαρτογράφηση του ανθρώπινου γονιδιώματος αποκάλυψε ότι το μέσο γονίδιο περιέχει 8,4 εσώνια, όλα από τα οποία πρέπει να αφαιρεθούν κατά την ωρίμανση. Αν και μερικά ανθρώπινα RNAs πιθανώς πάντα να ωριμάζουν με τον ίδιο τρόπο, οι επιστήμονες τώρα υπολογίζουν ότι τουλάχιστον το 75% υποβάλλονται σε εναλλακτική ωρίμανση.

Χορηγία εικόνας από EMBL Photolab
Τα ανθρώπινα γονίδια έχουν περισσότερα εσώνια από εκείνα των άλλων οργανισμών. Ο μέσος όρος στις μύγες και σε άλλα έντομα βρίσκεται μεταξύ 2,4 και 5,4 εσώνια ανά γονίδιο. (Ακόμα κι έτσι, ο σημερινός κάτοχος του ρεκόρ στην εναλλακτική ωρίμανση είναι ένα γονίδιο στη μύγα φρούτων αποκαλούμενο dscam, το οποίο μπορεί να παραγάγει 38.016 διαφορετικές πρωτεΐνες.) Μερικοί ερευνητές θεώρησαν ότι ο υψηλός αριθμός των ανθρώπινων εσωνίων, σήμαινε ότι τα γονίδια γίνονταν όλο και πιο σύνθετα με τα χρόνια. Παρόλα αυτά, μια πρόσφατη μελέτη από τις ομάδες Detlev Arendt και Peer Bork στο Eυρωπαϊκό Mοριακό Eργαστήριο της Bιολογίας (EMBL) στη Χαϋδελβέργη, Γερμανία, δείχνει ότι ο αρχαίος κοινός πρόγονος των εντόμων και των σπονδυλωτών σχεδόν βέβαια είχε γονίδια σαν αυτά των ανθρώπων, με περισσότερα εσώνια (Raible et al., 2005). Τα γονίδια έχουν σμικρυνθεί περισσότερο κατά τη διάρκεια της εξέλιξης στις μύγες και σε άλλα είδη που αναπαράγονται με μεγαλύτερο ρυθμό.
Υπάρχουν επίσης ενδιαφέρουσες διαφορές μεταξύ των ειδών, σχετικά με το συνολικό μήκος των εσωνίων σε σχέση με αυτό των εξωνίων μέσα στα γονίδια. Στα γονίδια του σκουληκιού Caenorhabditis elegans και πολλών άλλων ειδών, τα εσώνια και τα εξώνια περιέχουν σχεδόν τον ίδιο αριθμό ‘γραμμάτων ` (νουκλεοτίδια). Η κατάσταση στους ανθρώπους είναι πολύ διαφορετική: τα εσώνια σε ένα ενιαίο γονίδιο συνολικά συμπληρώνουν δεκάδες χιλιάδων νουκλεοτιδίων και είναι, κατά μέσον όρο, πέντε φορές το μήκος των εξωνίων. Αυτό μπορεί να ασκεί κάποια επίδραση στην εξέλιξη των ανθρώπινων γονιδίων, όπως αποκαλύφτηκε σε μια μελέτη από τους Cristian Castillo-Davis του Πανεπιστημίου του Χάρβαρντ, των ΗΠΑ, και Eugene Koonin και Fyodor Kondrashov του Εθνικού Κέντρου Πληροφοριών Βιοτεχνολογίας, ΗΠΑ (Castillo-Davis et al., 2002). Η μεταγραφή του RNA είναι μια αργή και απαιτητική σε ενέργεια διαδικασία: η παραγωγή των RNAs από ένα ενιαίο γονίδιο με τεράστια εσώνια, μπορεί να απαιτήσει μερικά λεπτά και χιλιάδες μόρια ATPs. Οι συντάκτες διαπίστωσαν ότι τα εσώνια των συχνά χρησιμοποιούμενων γονιδίων είναι κατά μέσον όρο 14 φορές μικρότερα από εκείνα των σπάνια χρησιμοποιούμενων γονιδίων. Το συμπέρασμά τους: η φυσική επιλογή έχει μικρύνει τα εσώνια στα πιο κοινά γονίδια, κερδίζοντας χρόνο και ενέργεια.
Καθώς η κυτταρική μηχανή που εκτελεί την εναλλακτική ωρίμανση εξελίχθηκε, θα μπορούσε να χρησιμοποιείται με διαφορετικούς τρόπους. Το ανακάτεμα και το ταίριασμα των μονάδων παράγει πρωτεΐνες που συμπεριφέρονται διαφορετικά. Βοηθούν στην κυτταρική διαφοροποίηση και στην ανάπτυξη των διαφορετικών ιστών. Η ενναλακτική ωρίμανση ενός RNA αποκαλούμενου Slo στο αυτί του κοτόπουλου, βελτιώνει την ακοή του πουλιού καθώς του παρέχει κύτταρα ευαίσθητα σε διαφορετικές συχνότητες ήχου. Στις μύγες, τρεις κρίσιμες πρωτεΐνες ωριμάζουν διαφορετικά στα αρσενικά και τα θηλυκά, δημιουργώντας σημαντικές διαφορές μεταξύ των φύλων. Αν και τα θηλυκά έχουν δύο Χ χρωμοσώματα ενώ τα αρσενικά μόνο ένα, τα θηλυκά δεν παράγουν δύο φορές την ποσότητα των πρωτεϊνών από τα γονίδια που εδράζονται στο χρωμόσωμα, χάρη στις διαφορές μεταξύ αυτών των πρωτεϊνών. Η Diane Lipscombe και οι συνάδελφοί της στο Πανεπιστήμιο Brown (Rhode Island, ΗΠΑ) έχουν διαπιστώσει ότι η εναλλακτική ωρίμανση είναι ιδιαίτερα κοινή στον εγκέφαλο των ποντικιών και άλλων θηλαστικών (Lipscombe, 2005). Μερικά από τα μόρια είναι σημαντικά για τη μνήμη και τη μάθηση.
Η ωρίμανση αποτελεί σημαντικό παράγοντα σε ένα ευρύ φάσμα ασθενειών. Οι μισοί από τους ανθρώπους που πάσχουν από νευροϊνωμάτωση, μια σοβαρή γενετική ασθένεια στην οποία οι όγκοι αναπτύσσονται παράλληλα με τα νεύρα και άλλους ιστούς, έχουν μεταλλάξεις που αλλάζουν την ωρίμανση των RNAs που παράγονται από το γονίδιο της νευροϊνωματίνης. Οι ασθενείς με β-θαλασσαιμία πάσχουν από αναιμία ως αποτέλεσμα των μη λειτουργικών βήτα-αλυσίδων των αιμοσφαιρινών στα ερυθρά αιμοσφαίριά τους˙ αυτή η σοβαρή ασθένεια προκαλείται από ελαττωματική ωρίμανση του αρμόδιου γονιδίου. Άλλα παραδείγματα είναι αλλαγές στο γονίδιο BRCA1 (που συνδέονται με τον καρκίνο του μαστού) και στο γονίδιο CFTR (που οδηγούν στην κυστική ίνωση). Υπολογίζεται ότι περίπου 50% των σχετικών με την ασθένεια μεταλλάξεων στα εξώνια, έχουν επιπτώσεις στον τρόπο που ωριμάζουν τα RNAs. Οι όγκοι και οι νευρο-εκφυλιστικές ασθένειες συνοδεύονται συχνά από κατά ασυνήθιστο τρόπο ωριμασμένα RNAs, που δεν βρίσκονται φυσιολογικά στους υγιείς ιστούς.
Ποιοτικός έλεγχος
Το 1979, οι Regine Losson και Franηois Lacroute από το CNRS στο Στρασβούργο, Γαλλία, ανακάλυψαν ότι το κύτταρο έχει ένα σύστημα να επιθεωρεί τα RNAs και να πραγματοποιεί ποιοτικό έλεγχο (Losson & Lacroute, 1979). Σχεδόν τρεις δεκαετίες έρευνας έδειξαν ότι το σύστημα δεν είναι τέλειο, αλλά κατορθώνει να προστατεύει τα ευκαρυωτικά κύτταρα από τα επικίνδυνα αποτελέσματα των περισσότερων μεταλλάξεων. Οι αλλαγές στα γονίδια που αλλάζουν τη μορφή, τη δομή ή τις λειτουργίες μιας πρωτεΐνης, έχουν συνήθως αρνητικά αποτελέσματα στο κύτταρο. Τα λάθη στην ωρίμανση μπορούν επίσης να παράγουν τέτοια μόρια, γι’ αυτό το σύστημα επιθεώρησης – αποκαλούμενο αποσύνθεση των χωρίς-νόημα mRNAs(nonsense–mediatedmRNAdecay, NMD)-πρέπει να είναι συνέχεια σε επιφυλακή.
Το NMD πραγματοποιείται όταν ένα RNA εισέρχεται στο κυτταρόπλασμα, αλλά οι επιστήμονες το έχουν συνδέσει με την ωρίμανση, που πραγματοποιείται πριν το RNA φύγει από τον πυρήνα (Sun et al., 2000). Το κύτταρο συνδέει μια συστάδα πρωτεϊνών στις περιοχές όπου αφαιρούνται τα εσώνια, σαν να τοποθετούμε ένα σημάδι πάνω σε ένα βαγόνι, που δείχνει ότι μερικά από τα ακόλουθα βαγόνια έχουν αφαιρεθεί. Η συστάδα αποτελείται από τουλάχιστον έξι πρωτεΐνες και καλείται σύμπλοκο σύνδεσης εξωνίων (ΣΣΕ)(exonjunctioncomplex, EJC). Αυτό το σύμπλοκο τοποθετείται στα σημεία κοψίματος και η θέση του παίζει μεγάλη σημασία στη μοίρα του RNA.
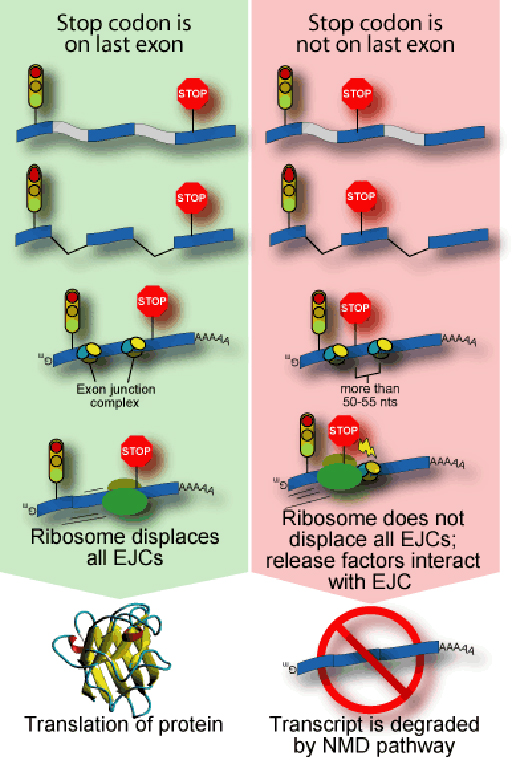
Η μετάφραση ενός RNA σε πρωτεΐνη πραγματοποιείται από μια μοριακή μηχανή που ονομάζεται ριβόσωμα που αγκυροβολεί πάνω σε ένα m-RNA, διαβάζει τον κώδικά του και συγκεντρώνει μια αλυσίδα αμινοξέων που ταιριάζει με την ακολουθία. Οποιαδήποτε ΣΣΕ υπάρχουν στο μόριο απομακρύνονται. Στο τέλος του αναγνωστικού πλαισίου, το ριβόσωμα αναγνωρίζει ένα σήμα τριών νουκλεοτιδίων, αποκαλούμενο κωδικόνιο λήξης και απελευθερώνει την τελειωμένη πρωτεΐνη. Οι μεταλλάξεις συχνά αλλάζουν την αλληλουχία ενός RNA, έτσι ώστε το κωδικόνιο λήξης να εμφανίζεται κάπου στη μέση του μορίου. Αυτό δημιουργεί έναν κώδικα μέσα στο RNA, που δεν έχει νόημα για το κύτταρο (το ‘nonsense’ στο NMD) και μπορεί να επιτρέψει την παραμονή ενός ΣΣΕ στο RNA, το οποίο προάγει την αποσύνθεση (NMD) (δείτε το σχήμα).
Για να αποτρέψει την παραγωγή βλαβερών πρωτεϊνών, το NMD αναγνωρίζει τα ΣΣΕ που βρίσκονται περίπου 50 νουκλεοτίδια μετά από το κωδικόνιο λήξης. Η διαδικασία της μετάφρασης διακόπτεται, και άλλα μόρια έρχονται να απομακρύνουν και να καταστρέψουν το RNA.
Αλλά κάποια RNAs διαφεύγουν της αποσύνθεσης (NMD)και παράγουν βλαβερές πρωτεΐνες που μπορούν να οδηγήσουν σε ασθένεια. Ακόμα και όταν λειτουργεί το NMD, το αποτέλεσμα μπορεί να είναι ασθένεια, επειδή το NMD μπορεί να καταστρέψει ένα RNA που είναι χαλασμένο αλλά εντούτοις απαραίτητο. Το 1989, το εργαστήριο της Lynne Maquat στο Roswell Park Memorial Institute (Νέα Υόρκη, ΗΠΑ) έδειξε ότι το NMD συμβάλλει στην β-θαλασσαιμία, η πιό κοινή γενετική ασθένεια στο Δυτικό κόσμο. Η β-θαλασσαιμία μειώνει την παραγωγή της αιμοσφαιρίνης, η οποία απαιτείται για να μεταφέρει το οξυγόνο μέσω του αίματος. Η ασθένεια προκύπτει σε ανθρώπους που κληρονομούν μια μεταλλαγμένη μορφή του γονιδίου που παράγει τη βήτα-αλυσίδα της αιμοσφαιρίνης˙ το NMD αναγνωρίζει τη μετάλλαξη και το σώμα καταστρέφει το RNA της β-αλυσίδας – αφαιρώντας ένα σημαντικό μόριο. Σε αυτήν την περίπτωση, ένας προοριζόμενος μηχανισμός ασφάλειας επιτίθεται πραγματικά στο ίδιο το σώμα.
Μέχρι πρόσφατα, το NMD θεωρήθηκε ότι είναι κάτι περισσότερο από μία παγίδα των RNAs που έχουν λάθη˙ Τώρα είναι γνωστό ότι είναι ένα γενικότερο εργαλείο που χρησιμοποιεί το κύτταρο για να ελέγξει την ποσότητα και την ποιότητα ορισμένων μορίων. Αυτό συμβαίνει επειδή η κανονική διαδικασία της εναλλακτική ωρίμανσης, παράγει μερικές φορές RNAs με κωδικόνια χωρίς νόημα˙ για κάποιο λόγο η λειτουργία αποκοπής και συγκόλλησης παράγει ένα κώδικα χωρίς νόημα στη μέση ενός RNA. Το 2004, οι R. Tyler Hillman, Richard Green και Steven Brenner του Πανεπιστημίου της Καλιφόρνια, Μπέρκλεϋ, ΗΠΑ, πραγματοποίησαν μια ανάλυση με υπολογιστή, που έδειξε ότι για το ένα τρίτο των περιπτώσεων, η εναλλακτική ωρίμανση τοποθετεί ένα κωδικόνιο λήξης 50 νουκλεοτίδια μπροστά από μια περιοχή αποκοπής. Αυτό ενεργοποιεί το NMD, που καταστρέφει το μεγαλύτερο μέρος του RNA πριν προλάβει να μεταφραστεί σε πρωτεΐνες (Hillman et al., 2004).
Το ίδιο έτος, η ομάδα του Harry Dietz στο John Hopkins University School της Ιατρικής (Μέρυλαντ, ΗΠΑ) μελέτησε αυτήν την επίδραση στα κύτταρα των θηλαστικών. Αυτά διακόπτουν τη λειτουργία των NMD με την αφαίρεση μιας πρωτεΐνης ονομαζόμενης Upf1, η οποία είναι σημαντική για τη διαδικασία. Αυτό άλλαξε τη συμπεριφορά ενός τεράστιου αριθμού γονιδίων: περίπου το 10% των γονιδίων που μελέτησαν, έγινε παραγωγικότερο, πιθανώς επειδή οι ώριμες μορφές που κανονικά θα καταστρέφονταν από το NMD γλίτωναν της διαδικασίας (Mendell et al., 2004).
Αυτό σημαίνει ότι το NMD, όπως στην εναλλακτική ωρίμανση, είναι μία συχνά χρησιμοποιούμενη διακλάδωση στο κεντρικό δρόμο μεταξύ των γονιδίων και των πρωτεϊνών. Υπάρχουν πολύ περισσότερα, μερικα από τα οποία θα συζητηθούν σε ένα μελλοντικό τεύχος τουScienceinSchool. Εάν η αγωνία σας είναι πολύ μεγάλη, εδώ είναι ένα αίνιγμα για να σας κρατήσει απασχολημένους: το χρώμα της πορφυρής πετούνιας οφείλεται σε ένα μοναδικό αντίγραφο ενός συγκεκριμένου γονιδίου. Τι θα συμβεί στο χρώμα της πετούνιας, εάν προσθέσετε ένα δεύτερο αντίγραφο εκείνου του γονιδίου.
References
- Berget SM, Moore C, Sharp PA (2000). Spliced segments at the 5’ terminus of adenovirus 2 late mRNA. Reviews in Medical Virology 10: 355-371
- Castillo-Davis CI, Mekhedov SL, Hartl DL, Koonin EV, Kondrashov FA (2002) Selection for short introns in highly expressed genes. Nature Genetics 31: 415-418. doi:10.1038/ng940
- Crick F (1970) Central Dogma of Molecular Biology. Nature 227: 561-563
- Hillman RT, Green RE, Brenner SE (2004) An unappreciated role for RNA surveillance. Genome Biology 5: R8. doi:10.1186/gb-2004-5-2-r8
- Lim S, Mullins JJ, Chen CM, Gross KW, Maquat LE (1989) Novel metabolism of several beta zero-thalassemic beta-globin mRNAs in the erythroid tissues of transgenic mice. The EMBO Journal 8(9): 2613-2619
- Lipscombe D (2005) Neuronal proteins custom designed by alternative splicing. Current Opinion in Neurobiology 15: 358-363. doi:10.1016/j.conb.2005.04.002
- Losson R, Lacroute F (1979) Interference of nonsense mutations with eukaryotic messenger RNA stability. Proceedings of the National Academy of Sciences USA 76: 5134-5137
- Mendell JT, Sharifi NA, Meyers JL, Martinez-Murillo F, Dietz HC (2004) Nonsense surveillance regulates expression of diverse classes of mammalian transcripts and mutes genomic noise. Nature Genetics 36: 1073-1078. doi:10.1038/ng1429
- Raible F et al. (2005) Vertebrate-type intron-rich genes in the marine annelid. Platynereis dumerilii. Science 310: 1325-1326. doi:10.1126/science.1119089
- Sun X, Moriarty PM, Maquat LE (2000) Nonsense-mediated decay of glutathione peroxidase 1 mRNA in the cytoplasm depends on intron position. EMBO Journal 19: 4734-4744. doi:10.1093/emboj/19.17.4734
Web References
- w1 – Το αντίγραφο της διάλεξης του Νομπελίστα Philip Sharp για την εναλλακτική ωρίμανση, ‘Διακεκομένα γονίδια και ωρίμανση του RNA’, είναι διαθέσιμο στο διαδίκτυο.
- Μια συνοπτική επισκόπηση της έρευνας των Richard Roberts και Philip Sharp δίνεται στο δελτίο τύπου που αναγγέλλει το βραβείο Νόμπελ τους.
- Για περισσότερες πληροφορίες για το βραβείο Νόμπελ, συμπεριλαμβανομένων των βιογραφιών των νικητών, δείτε εδώ.
Resources
-
Πολλά έγγραφα του Creek είναι διαθέσιμα στον ιστοχώρο του περιοδικού Nature.
Institutions
Review
Η πρόοδος στη βιοτεχνολογία κατά τη διάρκεια των τελευταίων 40 ετών έχει αντίκτυπο σε τομείς όπως η γεωργία, η επιστήμη τροφίμων και η ιατρική. Η χρήση του κεντρικού δόγματος της μοριακής βιολογίας σε χρήσιμες εφαρμογές, ειδικά στην έρευνα των ασθενειών και νέων θεραπειών, απαιτεί μια πιο λεπτομερή κατανόηση των λειτουργιών των μορίων της ζωής.
Αυτή η σειρά θα εισάγει τις προόδους και τις νέες θεωρίες που μπορεί να είναι πάρα πολύ πρόσφατες για να εμφανιστούν στα εγχειρίδια. Θα επεξηγήσει επίσης τη διεθνή και καθολική ανάγκη για την γνώση της λειτουργίας των μορίων της ζωής.
Αυτό το άρθρο παρέχει άριστο γνωστικό υπόβαθρο και τα μέρη του θα μπορούσαν να χρησιμοποιηθούν για να αυξήσουν και να εξετάσουν την κατανόηση του κεντρικού δόγματος από τους μαθητές, των ιδιοτήτων του RNA ή της πρωτεϊνοσύνθεσης. Ειδικότερα, το άρθρο θα ήταν κατάλληλο για την αναγνώριση των χρήσεων της βιοτεχνολογίας, της σημασίας της τρέχουσας έρευνας και της επιστημονικής προσπάθειας.
Marie Walsh, Δημοκρατία της Ιρλανδίας





